健康・医療一般用医薬品のリスク区分変更に関する要望受付について
令和8年4月1日
厚生労働省 医薬局 医薬安全対策課
定期的な再検討が行われずに長年第1類医薬品に留まっている医薬品があることを踏まえ、規制改革実施計画(令和7年6月13日閣議決定)、「強い経済」を実現する総合経済対策(令和7年11月21日閣議決定)において、販売区分の変更の要否を定期的に検討する仕組みの検討が求められていました。
これを受け、令和8年3月6日に開催された医薬品等安全対策部会において審議を行い、一般用医薬品のリスク区分の変更の要否を定期的に検討する仕組みを設けることとし、令和8年4月1日から要望を受け付けることとしました。
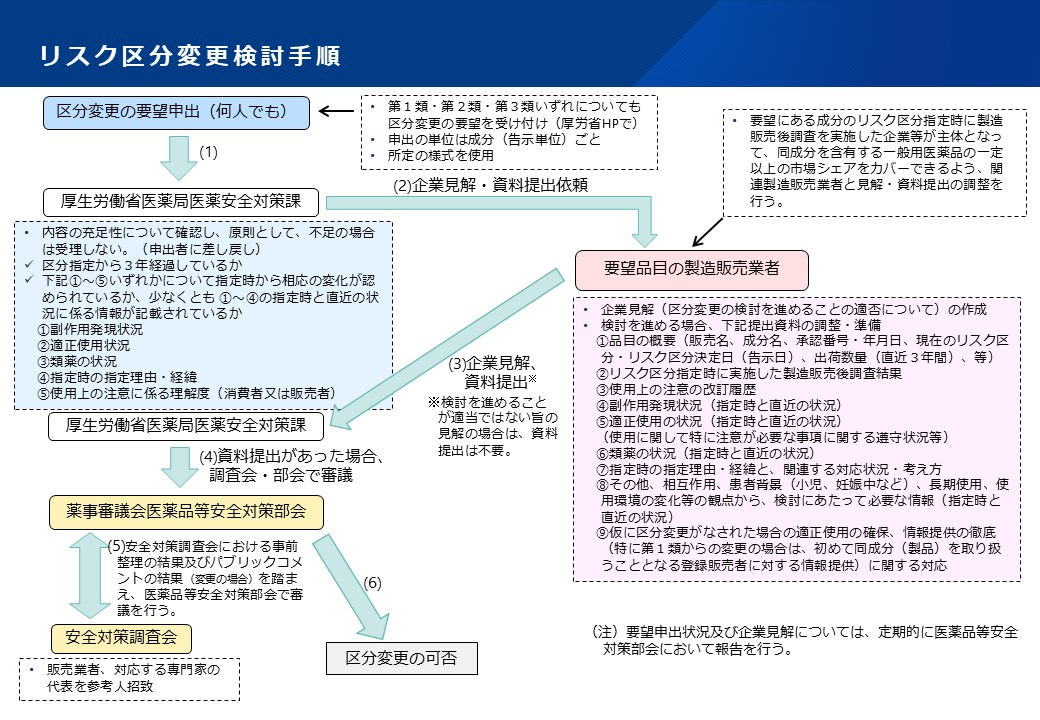
要望申出がなされたものについては、内容の充足性を確認した上で、製造販売業者に当該要望を伝えるとともに、要望に対する製造販売業者の見解・審議に必要な資料提出の依頼を行い、資料が提出されたものから順次、薬事審議会医薬品等安全対策部会 安全対策調査会で審議することとしています(下記「リスク区分変更検討手順」参照)。
なお、要望対象の要件を満たさない申出については、受付の対象外として取扱いますので、あらかじめご了承ください。また、要望受付に関する基本的な方針については、以下をご参照ください。
1.受付内容
一般用医薬品(第1類医薬品、第2類医薬品、第3類医薬品)のうち、リスク区分の変更を希望する成分。
【留意点】
・リスク区分指定日から、3年以上経過した成分であること。
・指定時における状況と比較し、下記のいずれかについて相応の変化が認められているものであること。
1.副作用発現状況
2.適正使用状況
3.類薬の状況
4.指定時の指定理由・経緯
5.使用上の注意に係る理解度(販売者又は購入者)
2.受付時期
随時
3.要望作成方法
別添様式「区分変更の要望申出様式」に必要事項を記入してください。作成にあたっては、「要望する成分の申出様式の作成に係る補足事項」を参照してください。
▶別添様式「区分変更の要望申出様式」[28KB]
▶要望する成分の申出様式の作成に係る補足事項(令和8年5月7日更新)[510KB]
なお、要望提出に際し以下の資料も参考にしてください。
▶一般用医薬品のリスク区分の変更の要否を定期的に検討する仕組みについて
<注意事項>
・別添様式の記載内容が十分ではないと認められた場合には、追記又は修正を依頼しますが、それでも十分な内容を満たさないと、受理しないことありますので、ご留意ください。
4.提出方法
電子メールで以下の提出先に提出してください。電子メールでの提出が困難な場合には、データを収録したCD-R(RW)又はDVD-R(RW)を同封の上、郵送にて提出してください。
電子メールで提出する際には、必ず「件名」を「成分名:リスク区分変更」としてください。
- 提出先
- 電子メールの場合
メールアドレス ISEANZEN□mhlw.go.jp
厚生労働省 医薬局 医薬安全対策課 - 郵送の場合
〒100-8916 東京都千代田区霞が関1-2-2
厚生労働省 医薬局 医薬安全対策課
「一般用医薬品のリスク区分変更」担当者宛
- 電子メールの場合
※迷惑メール防止のため、メールアドレスの一部を変えています。「□」を「@」に置き換えてください。
5.要望申出状況等
要望申出状況及び要望に対する製造販売業者の見解については、定期的に医薬品等安全対策部会において報告を行います。
製造販売業者から資料が提出されたものについて、順次、安全対策調査会で審議を行います。
要望の一覧等については、定期的に厚生労働省のホームページで公表いたします。
なお、受け付けた要望に関する対応状況を個別に要望申出者にお伝えすることはいたしません。
製造販売業者の皆様へ
受理した要望に関しては、要望成分のリスク区分指定時に製造販売後調査を実施した製造販売業者(承継等が行われている場合は承継後の製造販売業者等)等に対して、区分変更の検討を進めることの適否に係る見解及び審議に必要な資料提出の依頼を行います。
※ 製造販売後調査を実施した製造販売業者が不明な場合等は、最も早期に承認を取得した製造販売業者に依頼を行います。
依頼を受けた製造販売業者におかれましては、関連する他の製造販売業者と、見解・資料提出の調整をお願いいたします。検討を進めることが適当ではない旨の見解の場合は、資料の提出は不要です。
調整後、以下のものを医薬安全対策課あてに提出してください。
●要望に対する製造販売業者の見解
調整を行った製造販売業者名(ある場合)、シェアがわかる資料等を添付し、厚生労働省より依頼を受けた製造販売業者が、医薬安全対策課にメールで提出してください。作成にあたっては、下記様式をご活用ください。メールの「件名」は、「企業見解(成分名、企業名)」としてください。
※ 区分変更の検討を進める場合は、見解・資料提出企業の製品において、同成分を含有する一般用医薬品の一定以上(概ね3分の2以上)の市場シェアが必要です。検討を進めない場合は、概ね3分の2以上のシェアは必要ありませんが、見解提出企業のシェアが概ね3分の1以下である場合は、他の製造販売業者にあらためて依頼を行う場合があります。
●審議を行うための資料
各製造販売業者が、医薬安全対策課にメールで提出してください。作成にあたっては、下記様式をご活用ください。「件名」は、「資料提出(成分名、企業名)」としてください。
提出資料に不備・不明点等がある場合は、医薬安全対策課から照会等を行いますので、照会先の情報(ご担当者、連絡先等)を記載してください。
なお、要望申出状況及び製造販売業者の見解については、定期的に医薬品等安全対策部会において報告することとしており、見解に記載されている内容をそのまま用いる予定です。
【提出先】
厚生労働省医薬局医薬安全対策課 一般用医薬品担当 ISEANZEN□mhlw.go.jp
※ 迷惑メール防止のため、メールアドレスの一部を変えています。「□」を「@」に置き換えてください。
【様式】
▶区分変更の検討を進めることの適否に係る製造販売業者の見解[16KB]
▶リスク区分変更の検討に関する資料[28KB]



