特定用途医薬品の指定制度について
本制度は、小児に対する用法又は用量が設定されていないなど、医療上のニーズが著しく充足されていない医薬品の研究開発の促進に寄与することを目的とするものです。
指定要件
(1)小児の疾病の診断、治療又は予防を用途とするものであって、以下のア、イの要件を満たすもの
- ア対象とする用途の需要が著しく充足していないこと
- 以下のいずれかに該当するものであること
- ①既存の治療法、予防法又は診断法(以下「治療法等」という。)がないもの(医薬品を用いるもの以外に標準的な治療法等がない場合であって、小児に対する用法及び用量が設定された医薬品がない場合を含む)
- ②小児にとっての有効性、安全性又は肉体的・精神的な患者若しくは介護者負担の観点から、既存の治療法等より医療上の有用性の高い治療法、予防法又は診断法が必要とされているもの
- イ対象とする用途に対して特に優れた使用価値を有すること
- 以下の①及び②の両方を満たすものであること
- ①適応疾患が重篤である、又は重篤な疾患に対して支持的に用いるもの
- ②既存の治療法等として十分ではなく、製造販売の承認が与えられるとしたならば、その用途に関し、治療等の選択肢となりうるもの(小児に適した剤形や規格の製剤開発を要するもの、国際的なガイドライン等で標準的な治療法として確立しているもの、又はランダム化比較試験の結果等で高いエビデンスが得られているもの
(2)薬剤耐性を有する病原体による疾病の診断、治療又は予防を用途とするものであって、1)又は2)の場合に、それぞれア、イの要件を満たすもの
1)薬剤耐性を有する病原体を対象とする薬剤の場合
- ア対象とする用途の需要が著しく充足していないこと
- 以下の①及び②の両方を満たすものであること
- ①現在主として用いられている薬剤に耐性を有する(又は有することとなる可能性がある)病原体を対象とするものであること
- ②当該主として用いられている薬剤以外に対象とする病原体による疾患に対して承認された医薬品がないこと
- イ対象とする用途に対して特に優れた使用価値を有すること
- 以下の①及び②の両方を満たすものであること
- ①対象とする薬剤耐性を有する病原体の感染力、当該病原体による疾患の重篤性等の総合的な観点から、医薬品の必要性が高いこと
- ②国際的なガイドライン等で標準的な治療法として確立しているもの、又はランダム化比較試験の結果等で高いエビデンスが得られているもの
2)薬剤耐性を有する病原体の発生を抑制するための薬剤の場合
- ア対象とする用途の需要が著しく充足していないこと
- 以下①又は②のいずれかに該当するものであること
- ①既承認の用法及び用量で使用すると、対象となる疾患の原因となる病原体に対して薬剤耐性を生じさせることとなるおそれがあること
- ②国際的なガイドライン等で標準的な治療法として確立しているにもかかわらず、対象とする疾患に対する効能又は効果を有していないこと
- イ対象とする用途に対して特に優れた使用価値を有すること
- 以下の①及び②の両方を満たすものであること
- ①対象とする薬剤耐性を有する病原体の感染力、当該病原体による疾患の重篤性等の総合的な観点から、医薬品の必要性が高いこと
- ②国際的なガイドライン等で標準的な治療法として確立しているもの、又はランダム化比較試験の結果等で高いエビデンスが得られているもの
特定用途医薬品の指定手続きについて
厚生労働省は、特定用途医薬品の候補について、開発要望を募集し、医療上の必要性の高い未承認薬・適応外薬検討会議において、応募された要望の特定用途医薬品への該当性評価を行います。厚生労働省は、検討会議の該当性評価結果を、要望・提案された医薬品の製造販売業者へ通知し、当該製造販売業者が特定用途医薬品の指定を希望する場合、当該製造販売業者は特定用途医薬品への指定を申請します。特定用途医薬品の指定については、薬事審議会の意見を聴いて行います。
なお、指定した医薬品については、指定年月日、医薬品の名称、対象となる用途及び疾病並びに申請者の氏名及び住所を厚生労働省のホームページに掲載します。
※令和8年5月1日より、製造販売業者による特定用途医薬品指定相談については、医療上の必要性の高い未承認薬・適応外薬検討会議における該当性評価は行わないこととなりました。HP下部の「指定相談の事前準備について」の項をご確認いただき、必要な資料をご準備の上、ご相談ください。
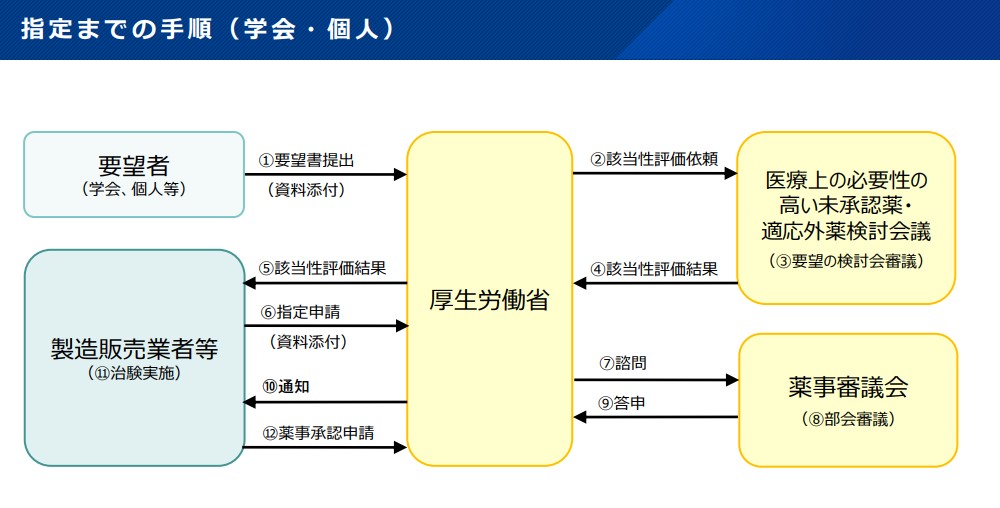
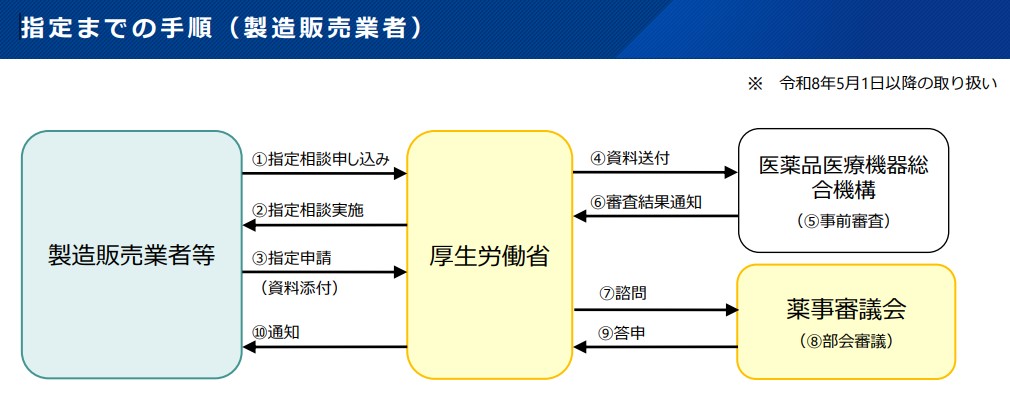
要望・提案書の提出(学会・個人)
(1)要望・提案の作成について
開発を要望する場合、「要望書作成の留意事項」に従って、要望対象の区分に応じた様式を用い、要望書を作成してください。また、総括表を作成して下さい。
- 要望・提案書作成の留意事項(PDF形式[412KB])[389KB]
- 様式
- (1)小児の疾病の診断、治療又は予防(様式:Word形式[39KB][36KB])
- (2)薬剤耐性を有する病原体による疾病の診断、治療又は予防
- 1)薬剤耐性を有する病原体を対象とする薬剤の場合(様式:Word形式[39KB][36KB])
- 2)薬剤耐性を有する病原体の発生を抑制するための薬剤の場合(様式:Word形式[39KB])[35KB]
- 総括表(様式:Excel形式[27KB])[27KB]
(2)要望・提案書の提出について
- 提出資料
- ・要望・提案書
- ・要望・提案が募集対象の範囲内である根拠となる文献及びその他の参考文献
- ・総括表
- 提出先
- 〒100-8916 東京都千代田区霞が関1-2-2
- 厚生労働省医薬局医薬品審査管理課
- 特定用途医薬品指定制度担当宛て
- アドレス:kaihatsuyoubou@mhlw.go.jp
指定相談の事前準備について(製造販売業者)
- 特定用途医薬品の指定を希望する企業等(以下「相談者」という)からの相談の申し込みについては随時受け付けを行っています。
- 相談は、厚生労働省医薬局医薬品審査管理課の指定業務相談者に申し込んでください。
- 申込みについては、電子メール等※で行ってください。
- 申請様式
- ・特定用途医薬品指定申請書(様式:Word形式[27KB][27KB])
- ※tokutei_iyakuhin@mhlw.go.jpにご連絡ください。
- 相談の申込みは日本語により行ってください。
3.相談の実施方法
-
指定相談は指定申請を行う前に行います。
-
指定相談は厚生労働省医薬局医薬品審査管理課にて行います。
-
相談時間は原則として、30分から1時間としてください。
-
相談人数の制限については特に規定しませんが、内容に応じた適切な人数としてください。
-
対面のほか、Web会議も活用可能です。
4.相談時の注意事項
- 指定申請に必要な資料の案又は指定申請を行う品目について説明が可能な資料を事前に準備してください。
- 必要に応じ資料に参考文献等を添付してください。
- 指定業務担当者の指示に従い、資料の事前送付等に対応してください
指定申請
1.指定申請に関する手続きについて
・指定相談実施後、特段の問題がなければ、指定業務担当者の指示に従い、指定申請書を提出してください。
・厚生労働省で指定申請書を受理した後、PMDAにおける事前評価が行われます。
・事前評価の結果、指定して差し支えないとの判断がなされた場合には、薬事審議会に諮問を行います。
・薬事審議会での審議で、指定しても差し支えないとの答申が得られた場合には、指定を行います。
・諸手続が終了後、指定書を申請者に郵送します。
2.指定申請資料について
- 申請資料
- ・特定用途医薬品指定申請書(様式:Word形式[27KB][27KB])
- ・申請書の添付資料
- ア対象とする用途に対する需要の充足状況に関する資料
- 上記2における開発要望・提案及び該当性評価の概要
- イ当該医薬品を使用する理論的根拠となる資料
- 規則第40条第1項第1号掲げる資料のうち申請時において入手可能な資料の概要
- ウ開発計画
- 予定している試験項目、試験期間など開発計画の概要を説明する資料
- エ特定用途医薬品の概要(様式1:Word形式[40KB][40KB]、様式2:Word形式[43KB][43KB])
- 部会説明用資料及び公表用資料として、様式1又は様式2に従って作成した概要
- ア対象とする用途に対する需要の充足状況に関する資料
- 資料の提出は可能な限り、Gateway経由で申請を行うこと。Gateway経由での申請が困難な場合は、以下に郵送をすること。
- 郵送先
- 〒100-8916 東京都千代田区霞が関1-2-2
- 厚生労働省医薬局医薬品審査管理課
- 特定用途医薬品指定制度担当宛て
指定された医薬品の優先的な取扱い
優先相談
優先審査
特定用途医薬品の指定取消しについて
試験研究等の中止
法第77条の2第3項の規定による指定を受けた者(以下「指定者」という。)は、当該指定に係る特定用途医薬品の試験研究、製造販売又は製造を中止しようとするときは、法第77条の5の規定に基づき、速やかに厚生労働大臣に届け出ることとされています。
なお、中止の届出は、以下の資料を提出してください。
- 届出資料
- ・特定用途医薬品の試験研究・製造販売・製造中止届書(様式:Word形式[37KB][37KB])
- ・指定申請書の写し
指定の取消
法第77条の5の規定による中止の届出があったときは、法第77条の6第1項の規定に基づき、厚生労働大臣は、指定の取り消しを行うとされています。また、同条第2項の規定に基づき、次のいずれかに該当するときは、指定を取り消すことがあります。
- ア他の医薬品等が承認されたことなどにより、指定要件のア又はイの要件を欠くと認められるとき。
- イ指定申請書の虚偽記載等不正があったと認められるとき。
- ウ正当な理由なく特定用途医薬品の試験研究又は製造販売が行われないとき。
- エ指定者について法その他薬事に関する法令で定めるもの又はこれに基づく処分に違反する行為があったとき。
承継の取扱い
指定者から、他の者(以下「承継者」という。)に本邦での開発権を譲渡する場合、指定者及び承継者は、以下の資料を提出してください。ただし、指定者が当該指定を受けた時点から、変更が生じている場合には、変更部分について、承継時点でも指定要件を充足することを示す資料も併せて提出してください。また、承継は指定者宛に発出する取消通知書及び承継者宛に発出する指定書を以て認めるものとします。なお、承継を検討している指定者は事前に医薬品審査管理課へ相談してください。
- 指定者及び承継者の連名で提出する資料
- ・承継の経緯等が把握できる資料
- 指定者が提出する資料
- ・特定用途医薬品の試験研究・製造販売・製造中止届書(様式:Word形式[37KB][37KB])
- ・指定申請書の写し
- 承継者が提出する資料
- ・特定用途医薬品指定申請書(様式:Word形式[27KB][27KB])
- ・申請書の添付資料
- ア対象とする用途に対する需要の充足状況に関する資料
- 上記2における開発要望・提案及び該当性評価の概要
- イ当該医薬品を使用する理論的根拠となる資料
- 規則第40条第1項第1号掲げる資料のうち申請時において入手可能な資料の概要
- ウ開発計画
- 予定している試験項目、試験期間など開発計画の概要を説明する資料
- エ特定用途医薬品の概要(様式1:Word形式[40KB][40KB]、様式2:Word形式[43KB][43KB])
- 部会説明用資料及び公表用資料として、様式1又は様式2に従って作成した概要
情報公開
特定用途医薬品
問い合わせ
厚生労働省医薬局医薬品審査管理課
特定用途医薬品指定制度担当者
TEL:03-5253-1111(内線:4181)
FAX:03-3597-9535



