|
PDFファイルを見るためには、Adobe Readerというソフトが必要です。 Adobe Readerは無料で配布されています。 (次のアイコンをクリックしてください。) |
| 1 | 趣旨 がんの治療法として、学会等でも複数の抗がん剤の併用療法が有効であるとされています。しかしながら、薬事法で承認された抗がん剤であっても、がんの種類等によっては効能が承認されていないため、事実上、併用療法に用いることができない状況にある問題を解決するため、「抗がん剤併用療法に関する検討委員会」を設置し、併用療法に必要な抗がん剤の効能の取得を迅速に進めるものです。 |
| 2 | 新しい仕組みについて
|
| 3 | 公表する報告書
|
| 4 | ご注意 抗がん剤の併用療法等を行う場合には、患者の安全確保を第一に考え、治療に伴い想定される死亡等の重篤な副作用の発生を可能な限り未然に防ぐための適正使用の確保が重要であることから、以下の点に注意するようお願いします。
|
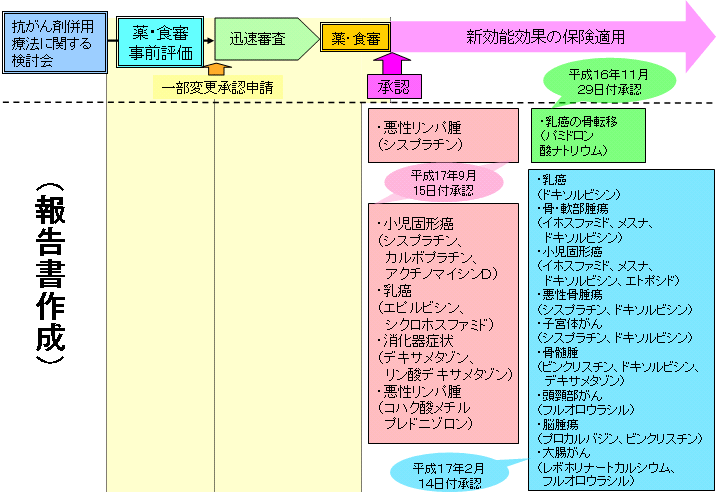
| 5 | 事前評価を受けた報告書に関する承認申請の進捗状況 薬事・食品衛生審議会医薬品第二部会において一定の根拠として適当であると評価を受けた報告書に関して、適応拡大のスキームにおける進捗状況を示しております。報告書がとりまとめられた抗がん剤については、平成17年9月までに、当該適応外使用に係る効能追加の承認を取得しています。(進捗状況) |
| 資料1 | ドキソルビシン(PDF:50KB)(→平成17年2月承認取得)及びシクロホスファミド(乳癌AC療法)(PDF:20KB)(→平成17年9月承認取得) |
| 資料2 | パミドロネート(乳癌)(PDF:58KB)→平成16年11月承認取得 |
| 資料3 | イホスファミド(骨・軟部腫瘍)(PDF:64KB) →平成17年2月承認取得 |
| 資料4 | ドキソルビシン(骨・軟部腫瘍)(PDF:95KB) →平成17年2月承認取得 |
| 資料5 | ドキソルビシン(小児)(PDF:67KB) →平成17年2月承認取得 |
| 資料6 | エトポシド(小児)(PDF:111KB) →平成17年2月承認取得 |
| 資料7 | イホスファミド(小児)(PDF:90KB) →平成17年2月承認取得 |
(平成16年8月27日開催の薬事・食品衛生審議会医薬品第二部会)
| 資料8 | シスプラチン(悪性骨腫瘍)(PDF:61KB) →平成17年2月承認取得 |
| 資料9 | シスプラチン及びドキソルビシン(子宮体がんAP療法)(PDF:93KB) →平成17年2月承認取得 |
| 資料10 | シスプラチン(PDF:251KB)及びメチルプレドニゾロン(悪性リンパ腫)(PDF:15KB) |
| 資料11 | ビンクリスチン、ドキソルビシン及びデキサメタゾン(骨髄腫VAD療法)(PDF:27KB) →平成17年2月承認取得 |
| 資料12 | フルオロウラシル(頭頸部がん)(PDF:51KB) →平成17年2月承認取得 |
| 資料13 | プロカルバジン(脳腫瘍)(PDF:42KB) →平成17年2月承認取得 |
| 資料14 | ビンクリスチン(脳腫瘍)(PDF:41KB) →平成17年2月承認取得 |
| 資料15 | フルオロウラシル及びアイソボリン(大腸がん)(PDF:40KB) →平成17年2月承認取得 |
(平成17年1月21日開催の薬事・食品衛生審議会医薬品第二部会)
| 資料16 | シスプラチン(小児)(PDF:261KB) →平成17年9月承認取得 |
| 資料17 | カルボプラチン(小児)(PDF:250KB) →平成17年9月承認取得 |
| 資料18 | アクチノマイシンD(小児)(PDF:118KB) →平成17年9月承認取得 |
| 資料19 | エピルビシン(PDF:246KB)及びシクロホスファミド(乳癌)(PDF:20KB) →平成17年9月承認取得 |
| 資料20 | デキサメタゾン及びリン酸デキサメタゾン(抗悪性腫瘍薬投与に伴う消化器症状)(PDF:86KB) →平成17年9月承認取得 |
| (照会先) |
厚生労働省医政局研究開発振興課 03−3595−2430(ダイヤルイン) 厚生労働省医薬食品局審査管理課 03−3595−2431(ダイヤルイン) |
|
PDFファイルを見るためには、Adobe Readerというソフトが必要です。 Adobe Readerは無料で配布されています。 (次のアイコンをクリックしてください。) |
| 抗がん剤併用療法の適応拡大のスキーム |
併用療法に係る抗がん剤の適応拡大を早めるため、
|
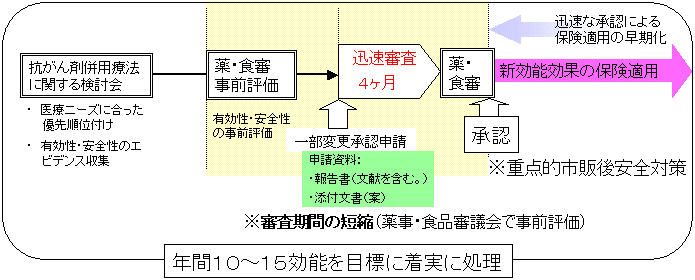
| 抗がん剤併用療法の適応拡大スキーム進捗状況(平成17年9月15日現在) |