 |
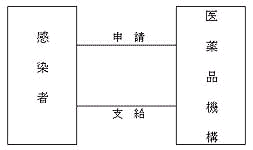 |
I丏堛栻昳丒堛椕婡婍丒寣塼摍懳嶔
| 丂崱斒偺栻帠朄摍偺夵惓偵傛傝丄岤惗徣偺怰嵏懱惂傪廩幚偝偣傞偲偲傕偵丄堛栻昳婡峔傪妶梡偟丄墷暷彅崙暲傒偺悈弨偺懱惂惍旛傪峴偄丄帯尡偐傜彸擣怰嵏丄巗斕屻懳嶔偵帄傞傑偱偺憤崌揑側埨慡惈妋曐懳嶔偺廩幚嫮壔傪恾傞丅 丂幘昦峔憿偺曄壔傗寬峃堄幆偺岦忋側偳堛栻昳摍傪庢傝姫偔娐嫬偼戝偒偔曄壔偟偰偒偰偍傝丄愭抂媄弍傪墳梡偟偨怴栻奐敪傊偺崙柉偺婜懸偑傑偡傑偡崅傑偰偄傞偙偲偐傜丄憂栻偵寢傃偮偔婎慴尋媶丄婎斦媄弍偺尋媶傪廩幚嫮壔偟丄偵偡偖傟偨堛栻昳丄堛椕梡嬶偺奐敪傪恾傞丅 丂堛椕偵偍偗傞栻嵻巘偺愑柋偑崅傑偭偰偄傞偙偲偐傜丄幚柋尋廋帠嬈傪廩幚偟丄栻嵻巘偺帒幙岦忋傪恾傞丅傑偨丄堛栻暘嬈傪堦憌悇恑偡傞偨傔丄堛栻暘寁夋嶔掕巜恓偵婎偯偒丄奺搒摴晎導偵偍偄偰丄堛栻暘嬈寁夋傪嶔掕偡傞丅 丂寣塼帠嬈偵偮偄偰偼丄寣塼惢嵻巊梡揔惓壔帠嬈傪悇恑偡傞偲偲傕偵丄寣塼惢嵻偺埨慡惈妋曐偺偨傔丄俫俬倁僂僀儖僗偺峈懱専弌晄擻婜娫偺抁弅偺偨傔偺嵏朄偺奐敪傗恖岺寣塼摍偺尋媶奐敪傪峴偆丅 丂僄僀僘慽徸偵娭偟偰偼丄枹採慽幰摍偺憗婜榓夝傪悇恑偡傞丅傑偨丄俫俬倁姶愼幰偺寬峃娗棟旓梡偺奼廩傪恾傞偲偲傕偵丄僄僀僘姵幰偺堚懓摍憡択帠嬈傪巤偡傞丅 |
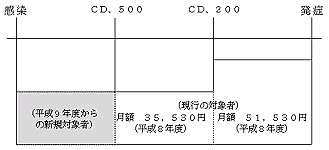
| 侾.堛栻昳摍偺桳岠惈媦傃埨慡惈偺妋曐 | 昐枩墌 侾,侾俋俇 |
仺 | 昐枩墌 侾,俀俇俋 |
| (1) 帯尡僨乕僞儀乕僗惍旛帠嬈 | 俋 | 仺 | 俀俆 |
| (2) 俧俠俹晛媦孾敪帠嬈 | 侽 | 仺 | 侾侽 |
| (3) 怴栻彸擣怰嵏嬈柋揹巕壔帠嬈旓 | 侾俀 | 仺 | 俁侽 |
| (4) 堛栻昳摍彸擣帠柋嫮壔旓 | 俁俋 | 仺 | 俈俇 |
| (5) 嵞昡壙奣梫嶌惉旓 | 侽 | 仺 | 係 |
| (6) 俧俹俵俽俹懳嶔旓 | 俀 | 仺 | 侾侾 |
| (7) 堛栻昳埨慡惈忣曬摑崌壔僔僗僥儉惍旛旓 | 侽 | 仺 | 俉俈 |
| (8) 堛栻昳暃嶌梡忣曬廂廤旓 | 侽 | 仺 | 俁俇 |
| (9) 俧俵俹摍嵏嶡惍崌惈妋曐帠嬈旓 | 侽 | 仺 | 俁侾 |
| (10) 俧俵俹崅搙壔懳墳婎斦惍旛帠嬈旓 | 侽 | 仺 | 侾俆 |
| 俀.堛栻昳摍偺尋媶奐敪媦傃嫙媼妋曐 | 昐枩墌 係,俉俈俉 |
仺 | 昐枩墌 俇,俋俁俇 |
|
| (1) 婎慴尋媶悇恑弌帒摍帠嬈旓 | 侾,侽侾俇 | 俀,俋俆俈 |
| (2) 僄僀僘堛栻昳摍偺尋媶奐敪偺悇恑 | 侾,侾係俋 | 仺 | 侾,侾係俋 |
| (3) 婓彮幘昦梡堛栻昳摍奐敪尋媶旓 | 俇俈侾 | 仺 | 俇俈侾 |
| (4) 崅搙愭抂堛椕尋媶宱旓乮堛椕婡婍奐敪暘栰乯乮岤惗壢妛壽寁忋乯 | 侽 | 仺 | 俆俈俆 |
| (5) 弌梈帒帠嬈乮嶻嬈搳帒摿暿夛寁乯 |
| 丂 | 俀俀壄墌 | 仺 | 俀俀壄墌 |
| 堛栻昳丄堛椕婡婍摍偺尋媶奐敪偵懳偡傞弌梈帒惂搙 |
| 俁.堛栻暘嬈偺悇恑 | 昐枩墌 俋俁 |
仺 | 昐枩墌 侾俀俋 |
| (1) 栻嵻巘幚柋尋廋帠嬈 | 侽 | 仺 | 俇侾 |
| (2) 堛栻暘嬈寁夋嶔掕帠嬈 | 侽 | 仺 | 俀侽 |
| 係.寣塼懳嶔 | 昐枩墌 侾,俉侾係 |
仺 | 昐枩墌 侾,俋俇侽 |
| (1) 寣塼惢嵻偺揔惓巊梡偺悇恑 | 係俇 | 仺 | 係俀 |
| (2) 崅搙愭抂堛椕尋媶宱旓乮恖岺寣塼奐敪尋媶暘栰乯 | 侽 | 仺 | 係俈俆 |
| (3) 俫俬倁専嵏媄弍丒婡婍奐敪偵敽偆媄弍昡壙帠嬈 | 俆俉 | 仺 | 俆係 |
| 俆.僄僀僘慽徸偺榓夝偺悇恑 | 昐枩墌 係俉侽 |
仺 | 昐枩墌 俆,俋俀俇 |
| (1) 榓夝偺憗婜棜峴 | 侽 | 仺 | 俆,侽係侾 |
| (2) 寣塼惢嵻偵傛傞俫俬倁姶愼幰偺挷嵏尋媶帠嬈摍 | 係俉侽 | 仺 | 俉係俆 |
| (3) 僄僀僘姵幰偺堚懓摍憡択帠嬈 | 侽 | 仺 | 係侽 |
II丏杻栻丒妎偣偄嵻摍懳嶔
| 丂崙楢杻栻棎梡杘柵侾侽擭偺巟墖帠嬈偲偟偰乽僟儊丅僛僢僞僀丅晛媦帠嬈乿傪堷偒懕偒幚巤偡傞側偳丄栻暔棎梡偺枹慠杊巭妶摦偺廩幚傪恾傞偲偲傕偵杻栻丒妎偣偄嵻帠斊庢掲傝懱惂偺嫮壔傪恾傞丅 |
| 侾.孾敪妶摦偺揙掙 | 昐枩墌 俀俋俁 |
仺 | 昐枩墌 俀俋俁 |
| 惵彮擭栻暔棎梡杊巭摿暿懳嶔旓 | 侽 | 仺 | 侾俁 |
| 俀.庢掲懱惂偺廩幚摍 | 昐枩墌 俀,俇侾係 |
仺 | 昐枩墌 俀,俇俇侾 |
| 杻栻庢掲姱帠柋強宱旓 | 侾,俋俁俋 | 仺 | 侾,俋俈係 |
| 乮娪掕丄憑嵏婡婍偺惍旛廩幚摍乯 |
乮扨埵丗愮墌乯
| 壢丂丂丂丂栚 | 暯惉俉擭搙 梊丂嶼丂妟 |
暯惉俋擭搙 梊丂嶼丂埬 |
懳慜擭搙斾 妑憹仮尭妟 |
強娗壽柤 | 旛丂丂丂峫 |
乮慻怐乯岤惗杮徣 丂 丂乮崁乯岤惗杮徣 丂 丂丂乮栚乯堛栻暘嬈悇恑帠嬈埾戸旓 丂 丂丂丂丂乮愊嶼撪栿乯 丂 丂丂丂丂丂堛栻暘嬈寁夋嶔掕巜恓専摙帠嬈旓 丂 丂丂乮栚乯栻帠宱嵪挷嵏埾戸旓 丂 丂丂丂丂乮愊嶼撪栿乯 丂 丂丂丂丂丂堛栻昳摍壙奿挷嵏旓 丂 丂丂丂丂丂乮宱帪曄摦摍挷嵏旓乯 丂 丂丂丂丂丂乮堦斒梡堛栻昳壙奿摦岦摍挷嵏旓乯 丂 丂丂丂丂丂堛栻昳摍嫙媼摦岦挷嵏旓 丂 丂丂丂丂丂堛栻昳嶻嬈摍幚懺挷嵏旓 丂 丂丂丂丂丂乮堛栻昳嶻嬈幚懺挷嵏旓乯 丂 丂丂丂丂丂乮堛椕婡婍嶻嬈怳嫽挷嵏旓乯 丂 丂丂乮栚乯専掕専嵏帠柋摍埾戸旓 丂 丂丂丂乮栚嵶乯堛栻昳専掕帠柋摍埾戸旓 丂 丂丂丂丂乮愊嶼撪栿乯 丂 丂丂丂丂丂堛栻昳摍惢憿嬈嫋壜彸擣帠柋旓 丂 丂丂丂丂丂乮栻帠朄巤峴娭學宱旓乯 丂 丂丂丂丂丂乮撆暔寑暔塩嬈幰搊榐摍僔僗僥儉 丂丂丂丂丂丂奐敪旓乯 丂 丂丂丂丂丂乮堛栻昳摍怰嵏僔僗僥儉奐敪旓乯 丂 丂丂丂丂丂乮揹巕彸擣乮嫋壜乯怽惪僔僗僥儉 丂丂丂丂丂丂奐敪旓乯 丂 丂丂丂丂丂桝塼惢嵻懳嶔旓 丂 丂丂丂丂丂堛椕梡嬶摍摿暿娔帇旓 丂 丂丂丂丂丂丂堛椕梡嬶摍摿暿娔帇旓 丂 丂丂丂丂丂丂乮堛椕梡嬶摿暿娔帇旓乯 丂 丂丂丂丂丂丂乮柍彸擣柍嫋壜堛栻昳娔帇巜摫婎 丂 丂丂丂丂丂丂丂弨摍嶌惉旓乯 丂丂丂丂丂丂堛栻昳摍俧俵俹懳嶔旓 丂 丂丂丂丂丂丂乮俧俵俹徹柧惂搙懳嶔旓乯 丂 丂丂丂丂丂丂乮俧俵俹摍嵏嶡惍崌惈妋曐帠嬈旓乯 丂 丂丂丂丂丂丂乮俧俵俹巜摫懳嶔旓乯 丂 丂丂丂丂丂丂乮俧俵俹崅搙壔懳墳婎斦惍旛帠嬈乯 丂 丂丂丂丂丂丂堛栻昳崙壠専掕旓 丂 丂丂丂丂丂丂乮崙壠専掕専嵏旓乯 丂 丂丂丂丂丂丂乮堦惸庢掲旓乯 丂 丂丂乮栚乯寣塼惢嵻巊梡揔惓壔晛媦埾戸旓 丂 丂丂乮栚乯杻栻庢掲堳旓摍岎晅嬥 丂 丂丂丂乮栚嵶乯杻栻庢掲堳旓岎晅嬥 丂 丂丂丂乮栚嵶乯偁傊傫庢掲帠柋旓岎晅嬥 丂 丂乮崁乯曐寬塹惗彅旓 丂 丂丂乮栚乯寣塼妋曐帠嬈摍曗彆嬥 丂 丂丂丂丂乮愊嶼撪栿乯 丂 丂丂丂丂丂專寣悇恑婎斦惍旛帠嬈旓 丂 丂丂丂丂丂乮專寣惂搙悇恑儌僨儖帠嬈旓乯 丂 丂丂乮栚乯曐寬帠嬈旓摍曗彆嬥 丂 丂丂丂乮栚嵶乯幘昦梊杊帠嬈旓摍曗彆嬥 丂 丂丂丂丂乮堛栻暘嬈掕拝懀恑専摙帠嬈旓乯 丂 丂乮崁乯惛恄曐寬旓 丂 丂丂乮栚乯惛恄曐寬懳嶔旓摍曗彆嬥 丂 丂丂丂乮栚嵶乯杻栻摍懳嶔悇恑旓曗彆嬥 丂 丂丂丂丂乮愊嶼撪栿乯 丂 丂丂丂丂丂杻栻懳嶔旓 丂 丂丂丂丂丂妎偣偄嵻懳嶔旓 丂 丂 丂 丂 丂 丂 丂 丂 丂丂乮栚乯惛恄忈奞幰慬抲擖堾旓摍晧扴嬥 丂 丂丂丂乮栚嵶乯杻栻拞撆幰擖堾慬抲旓晧扴嬥 |
1,088,527 丂 805,300 丂 丂 丂 6,712 丂 74,888 丂 17,595 丂 15,881 丂 1,714 丂 55,735 丂 1,558 丂 327 丂 1,231 丂 丂 201,119 丂 96,776 丂 4,681 丂 10,968 丂 67,843 丂 13,284 丂 1,980 丂 88,782 丂 5,880 丂 4,302 丂 1,578 丂 82,902 丂 4,147 丂 0 丂 78,755 丂 0 丂 13,581 丂 7,885 丂 5,696 丂 44,457 丂 478,124 丂 477,988 丂 136 138,282 丂 丂 丂 丂 100,000 丂 丂 丂 38,282 丂 144,945 丂 丂 144,478 丂 10,785 丂 133,693 丂 丂 丂 丂 丂 丂 丂 丂 丂 467 |
913,043 丂 657,002 丂 丂 丂 0 丂 69,884 丂 17,600 丂 15,885 丂 1,715 丂 50,864 丂 1,420 丂 295 丂 1,125 丂 丂 63,450 丂 4,711 丂 4,711 丂 0 丂 0 丂 0 丂 1,980 丂 43,178 丂 5,880 丂 4,302 丂 1,578 丂 37,298 丂 4,228 丂 17,923 丂 0 丂 15,147 丂 13,581 丂 7,885 丂 5,696 丂 40,218 丂 483,450 丂 483,314 丂 136 丂 124,454 丂 丂 丂 丂 90,000 丂 丂 丂 34,454 丂 131,587 丂 丂 131,120 丂 10,785 丂 120,335 丂 丂 丂 丂 丂 丂 丂 丂 丂 467 |
仮 175,484 丂 仮 148,298 丂 丂 丂 仮 6,712 丂 仮 5,004 丂 5 丂 4 丂 1 丂 仮 4,871 丂 仮 138 丂 仮 32 丂 仮 106 丂 丂 仮 137,669 丂 仮 92,065 丂 30 丂 仮 10,968 丂 仮 67,843 丂 仮 13,284 丂 0 丂 仮 45,604 丂 0 丂 0 丂 0 丂 仮 45,604 丂 81 丂 17,923 丂 仮 78,755 丂 15,147 丂 0 丂 0 丂 0 丂 4,239 丂 5,326 丂 5,326 丂 0 丂 仮 13,828 丂 丂 丂 丂 仮 10,000 丂 丂 丂 仮 3,828 丂 仮 13,358 丂 丂 仮 13,358 丂 0 丂 仮 13,358 丂 丂 丂 丂 丂 丂 丂 丂 丂 0 |
丂 丂 丂 丂 丂 丂 婇夋壽 丂 丂 丂 丂 宱嵪壽 乂 乂 丂 乂 堛椕婡婍 奐敪壽丂 丂 丂 丂 丂 怰嵏壽 埨慡壽 丂 怰嵏壽 堛椕婡婍 奐敪壽丂 丂 丂 丂 娔帇巜摫壽 乂 丂 丂 乂 乂 丂 乂 丂 乂 乂 丂 婇夋壽 丂 丂 杻栻壽 乂 丂 丂 丂 丂 丂 丂 婇夋壽 丂 丂 丂 乂 丂 丂 丂 丂 丂 丂 杻栻壽 乂 丂 丂 丂 丂 丂 丂 丂 丂 丂 杻栻壽 |
丂 丂 丂 丂 丂 丂 丂 丂 丂 丂 丂 慡搒摴晎導偵埾戸 丂丂丂丂乂 丂丂丂丂乂 丂 丂丂丂丂乂 丂丂丂丂乂 丂 丂 丂 丂 丂 慡搒摴晎導偵埾戸 丂 丂 丂 丂 丂 丂 丂 丂 慡搒摴晎導偵埾戸 俈搒摴晎導偵埾戸 丂 丂 奩摉搒摴晎導偵埾戸 慡搒摴晎導偵埾戸 丂 俁晎導偵埾戸 丂 慡搒摴晎導偵埾戸 丂丂丂丂乂 丂 慡搒摴晎導偵埾戸 丂 丂 慡搒摴晎導偵岎晅 奩摉搒摴晎導偵岎晅 丂 丂 丂 丂 丂 丂 俆搒摴晎導丄侾侽巗偵曗彆 丂 丂 丂 奩摉搒摴晎導乮惌椷巗丄摿暿嬫 傪娷傓乯偵曗彆 丂 丂 丂 丂 丂 侾侽搒晎導偵曗彆 丂 1.妎偣偄嵻棎梡杊巭悇恑堳旓 丂丂慡搒摴晎導偵曗彆 2.曐寬強偵偍偗傞憡択憢岥 丂丂慡搒摴晎導偵曗彆 3.妎偣偄嵻棎梡杊巭悇恑堳抧嬫 丂嫤媍夛塣塩旓曗彆 丂丂俀俁搒摴晎導偵曗彆 丂 丂 奩摉搒摴晎導偵晧扴 |
| 擭搙 | 張曽偣傫敪峴枃悢 | 仏 暘嬈棪 |
栻嬊悢 | 曐尟栻嬊悢 | |
| 懳慜擭搙斾 | |||||
俇侾 俇俀 俇俁 尦 俀 俁 係 俆 俇 俈 |
枩枃 侾侾丆俀俆係 侾侾丆俋係係 侾俀丆俇俋俋 侾俁丆俈侽侽 侾係丆俇侽侾 侾俇丆侽係俋 侾俈丆俉俋俈 俀侽丆侾係俋 俀俁丆俆侾俇 俀俇丆俆俁係 |
亾 侾侽俇丏侽 侾侽俇丏侾 侾侽俇丏俁 侾侽俈丏俋 侾侽俇丏俇 侾侽俋丏俋 侾侾侾丏俆 侾侾俀丏俇 侾侾俇丏俈 侾侾俀丏俉 |
亾 俋丏俈 侾侽丏侾 侾侽丏俇 侾侾丏俁 侾俀丏侽 侾俀丏俉 侾係丏侾 侾俆丏俉 侾俉丏侾 俀侽丏俁 |
俁俆丆俈俉俁 俁俆丆俋侾俆 俁俇丆侾係俀 俁俇丆俇俈侽 俁俇丆俋俉侾 俁俇丆俋俈俋 俁俈丆俆俁俀 俁俉丆侽俈俈 俁俉丆俈俈俁 俁俋丆係俁俁 |
俁侽丆俁俉俋 俁侽丆俆俀俁 俁侽丆俇俀俀 俁侽丆俉俉係 俁侾丆俁俁侾 俁侾丆係侽俀 俁侾丆俈俇侾 俁俀丆俆俋係 俁係丆俉俀俉 俁俆丆俋侾俆 |
暯惉俉擭1寧亅12寧
| 丂 搒摴晎導 | 惉暘專寣丂丂 | 係侽侽倣倢專寣丂丂 | 俀侽侽倣倢專寣丂丂 | 崌寁丂丂 | ||||||||
| 丂 | 峔惉斾 | 慜擭斾 | 丂 | 峔惉斾 | 慜擭斾 | 丂 | 峔惉斾 | 慜擭斾 | 丂 | 峔惉斾 | 慜擭斾 | |
| 丂 | 恖 | 亾 | 亾 | 恖 | 亾 | 亾 | 恖 | 亾 | 亾 | 恖 | 亾 | 亾 |
| 杒奀摴 惵怷 娾庤 媨忛 廐揷 | 56,151 9,499 17,650 18,975 10,248 | 14.7 13.4 24.8 19.1 17.0 | 92.4 90.0 97.6 85.7 76.9 | 189,050 27,523 27,994 39,743 25,855 | 49.6 38.9 39.4 40.0 42.9 | 101.0 97.8 98.7 88.0 122.1 | 135,986 33,703 25,465 40,755 24,183 | 35.7 47.7 35.8 41.0 40.1 | 101.9 87.8 87.2 97.0 73.4 | 381,187 70,725 71,109 99,473 60,286 | 100.0 100.0 100.0 100.0 100.0 | 99.9 91.8 94.0 91.0 89.4 |
| 嶳宍 暉搰 堬忛 撊栘 孮攏 | 7,738 20,540 17,743 21,977 17,180 | 15.5 20.1 15.5 24.6 19.1 | 80.8 93.4 116.2 93.4 87.3 | 23,415 40,870 42,782 35,519 37,025 | 46.9 40.1 37.3 39.7 41.1 | 105.2 100.1 102.1 90.2 99.7 | 18,769 40.582 54.093 31.957 35.813 | 37.6 39.8 47.2 35.7 39.8 | 80.3 87.0 96.6 91.3 104.0 | 49.922 101,992 114,618 89,453 90,018 | 100.0 100.0 100.0 100.0 100.0 | 90.4 93.2 101.3 91.4 98.7 |
| 嶉嬍 愮梩 搶嫗 恄撧愳 怴妰 | 50,915 40,021 130,135 68,266 24,796 | 19.9 19.5 21.9 22.1 24.0 | 84.1 94.7 98.7 87.1 91.0 | 102,292 88,187 284,932 145,261 47,495 | 39.9 43.0 48.0 46.9 45.9 | 104.9 104.9 95.9 99.2 100.2 | 103,089 77,076 178,057 95,934 31,179 | 40.2 37.5 30.0 31.0 30.1 | 84.6 93.6 101.6 86.3 91.9 | 256,296 205,284 593,124 309,461 103,470 | 100.0 100.0 100.0 100.0 100.0 | 91.6 98.4 98.2 92.1 95.3 |
| 晉嶳 愇愳 暉堜 嶳棞 挿栰 | 14,075 14,402 8,428 7,464 18,285 | 22.5 20.1 20.4 16.8 18.1 | 107.6 97.4 106.6 98.2 82.9 | 25,200 27,510 19,403 17,711 44,141 | 40.2 38.3 47.0 39.8 43.8 | 102.7 107.7 100.4 97.3 112.4 | 23,386 29,906 13,441 19,323 38,432 | 37.3 41.6 32.6 43.4 38.1 | 82.0 90.6 77.9 99.3 74.0 | 62,661 71,818 41,272 44,498 100,858 | 100.0 100.0 100.0 100.0 100.0 | 94.7 97.9 92.8 98.3 89.1 |
| 婒晫 惷壀 垽抦 嶰廳 帬夑 | 23,214 37,230 74,414 18,418 11,154 | 28.8 22.3 22.7 20.8 19.7 | 88.1 102.6 95.0 86.4 100.2 | 27,428 58,870 124,677 33,970 23,796 | 34.0 35.2 38.1 38.5 42.0 | 98.5 95.1 101.5 112.3 110.1 | 30,067 71,095 128,339 35,949 21,748 | 37.3 42.5 39.2 40.7 38.4 | 88.7 89.7 91.6 93.0 74.8 | 80,709 167,195 327,430 88,337 56,698 | 100.0 100.0 100.0 100.0 100.0 | 91.6 94.2 95.9 97.9 91.7 |
| 嫗搒 戝嶃 暫屔 撧椙 榓壧嶳 | 28,194 79,457 38,644 12,073 10,011 | 23.7 17.4 15.6 18.8 18.9 | 91.8 86.8 108.9 78.9 83.1 | 63,701 198,341 101,148 28,898 27,548 | 53.5 43.4 40.9 44.9 52.1 | 99.2 101.2 118.8 101.2 121.1 | 27,073 179,483 107,801 23,414 15,288 | 22.8 39.3 43.5 36.4 28.9 | 84.7 90.3 101.2 77.7 62.9 | 118,968 457,281 247,593 64,385 52,847 | 100.0 100.0 100.0 100.0 100.0 | 93.7 94.0 109.0 87.0 89.4 |
| 捁庢 搰崻 壀嶳 峀搰 嶳岥 | 7,451 12,306 20,445 30,305 15,749 | 21.1 26.7 21.0 21.6 17.7 | 98.3 97.5 96.2 85.6 107.8 | 13,754 17,724 42,507 60,165 45,480 | 38.9 38.4 43.7 43.0 51.0 | 115.3 114.5 92.7 93.2 93.5 | 14,130 16,115 34,330 49,567 27,998 | 40.0 34.9 35.3 35.4 31.4 | 95.7 77.1 102.8 86.4 86.4 | 35,335 46,145 97,282 140,037 89,227 | 100.0 100.0 100.0 100.0 100.0 | 103.1 94.2 96.8 89.0 93.3 |
| 摽搰 崄愳 垽昋 崅抦 暉壀 | 10,660 13,163 19,767 7,647 52,810 | 22.3 20.4 24.4 18.1 20.7 | 86.7 95.0 89.1 95.9 105.6 | 17,866 23,480 30,568 15,531 154,051 | 37.3 36.3 37.7 36.8 60.4 | 92.9 97.6 98.3 102.1 100.1 | 19,316 27,989 30,661 19,001 48,301 | 40.4 43.3 37.9 45.0 18.9 | 95.5 90.6 88.3 81.5 125.4 | 47,842 64,632 80,996 42,179 255,162 | 100.0 100.0 100.0 100.0 100.0 | 92.4 94.0 92.1 90.7 105.2 |
| 嵅夑 挿嶈 孎杮 戝暘 媨嶈 | 7,486 23,723 32,000 14,448 14,003 | 18.5 23.9 25.2 21.2 21.8 | 88.0 98.5 96.0 91.7 95.4 | 21,308 50,261 50,836 31,330 28,769 | 52.7 50.6 40.0 46.0 44.8 | 101.0 100.2 101.0 99.0 98.8 | 11,514 25,266 44,205 22,299 21,439 | 28.7 25.5 34.8 32.8 33.4 | 91.3 98.1 102.1 111.0 89.1 | 40,408 99,250 127,041 68,077 64,231 | 100.0 100.0 100.0 100.0 100.0 | 95.5 99.3 100.1 100.9 94.6 |
| 幁帣搰 壂撽 | 18,010 15,375 | 17.5 25.7 | 84.5 98.7 | 50,240 27,558 | 48.9 46.1 | 99.3 100.6 | 34,540 16,858 | 33.6 28.2 | 92.4 95.6 | 102,790 59,791 | 100.0 100.0 | 94.0 98.7 |
| 崌寁 | 1,222,645 | 20.2 | 93.3 | 2,661,733 | 44.1 | 100.7 | 2,155,015 | 35.7 | 91.8 | 6,039,393 | 100.0 | 95.9 |
俇丏僄僀僘慽徸偺榓夝摍
俬丏僄僀僘慽徸偺榓夝偵偮偄偰
 |
 |
| -------- |
|
| -------- |
|
| -------- |
|
| -------- |
|
| -------- |
|
| 変偑崙堛栻昳嶻嬈慡懱偱偼丄尋媶奐敪椡丄崙嵺嫞憟椡摍崙嵺揑偵偼傑偩晄廫暘 (1)尋媶奐敪偺悇恑丄(2)崙嵺揑側帠嬈妶摦偺揥奐丄(3)棳捠嬤戙壔偑摉柺偺廳梫壽 |
侾丏堛栻昳巗応婯柾乮1993擭乯 俀丏惢栻儊乕僇乕偺崙嵺斾妑乮1995擭丄100枩僪儖乯
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
俉丏僄僀僘帯椕栻偺奼戝帯尡偵偮偄偰
乮侾乯奼戝帯尡偺懳徾堛栻昳
| 惉丂暘丂柤 乮棯崋摍乯 |
夛丂幮丂柤 | 嶌丂梡 | 奜崙偵偍偗傞忬嫷 | 旛丂丂峫 |
| 僗僞僽僕儞 乮倓係俿乯 |
僽儕僗僩儖儅僀儎乕僘僗僋僀僽 | 媡揮幨峺慺慾奞嵻 | 暷崙偱彸擣嵪傒 | 俫俈擭搙巜掕 |
| 儔儈僽僕儞 乮俁俿俠乯 |
擔杮僂僄儖僇儉 | 媡揮幨峺慺慾奞嵻 | 暷崙偱彸擣嵪傒 1995.11.17 |
俫俉擭搙巜掕 |
| 儕僩僫價儖 | 僟僀僫儃僢僩 | 僾儘僥傾乕僛慾奞嵻 | 暷崙偱彸擣嵪傒 1996.3.1 |
俫俉擭搙巜掕 |
| 棸巁僀儞僕僫價儖 | 漭桳惢栻 | 僾儘僥傾乕僛慾奞嵻 | 暷崙偱彸擣嵪傒 1996.3.14 |
俫俉擭搙巜掕 |
| 儊僔儖巁僒僉僫價儖 | 擔杮儘僔儏 | 僾儘僥傾乕僛慾奞嵻 | 暷崙偱彸擣嵪傒 1995.12.6 |
俫俉擭搙巜掕 |
| 僱價儔僺儞 | 擔杮儀乕儕儞僈乕僀儞僎儖僴僀儉 | 媡揮幨峺慺慾奞嵻 | 暷崙偱彸擣嵪傒 1996.6. |
俫俉擭搙巜掕 帯尡弨旛拞 |
| 惉丂暘丂柤 乮棯崋摍乯 |
夛丂幮丂柤 | 岠擻丒岠壥 | 奜崙偵偍偗傞忬嫷 | 旛丂丂峫 |
| 僋儔儕僗儘儅僀僔儞 | 戝惓惢栻丒僟僀僫儃僢僩 | 屻揤惈柶塽晄慡徢岓孮偵偍偗傞攄庬惈儅僀僐僶僋僥儕僂儉姶愼徢 | 暷崙偱彸擣嵪傒 | 俫俇擭搙巜掕 |
| 僜儅僩儘僺儞 | 僙儘乕僲W儍僷儞 | 屻揤惈柶塽晄慡徢岓孮偺彍帀朾懱廳偺堐帩丒憹壛 | 暷崙偱彸擣嵪傒 1996.8.23 |
俫俈擭搙巜掕 |
| 儂僗僇儖僱僢僩僫僩儕僂儉 | 傾僗僩儔僕儍僷儞 | 屻揤惈柶塽晄慡徢岓孮偵偍偗傞僒僀僩儊僈儘僂僀儖僗栐枌墛 | 暷崙偱彸擣嵪傒 | 俫俈擭搙巜掕 |
| 僈儞僔僋儘價儖 乮宱岥嵻乯 |
揷曈惢栻 | 僒僀僩儊僈儘僂僀儖僗栐枌墛 | 暷崙偱彸擣嵪傒 | 俫俉擭搙巜掕 |
乮俀乯僄僀僘嫆揰昦堾
暯惉俉擭侾俀寧侾俇擔
| 杒奀摴丂乮19堛椕婡娭) |
|
|||
| 惵怷導丂乮 4堛椕婡娭) |
|
|||
| 娾庤導丂乮 4堛椕婡娭) |
|
|||
| 媨忛導丂乮 7堛椕婡娭) |
|
|||
| 廐揷導丂乮 2堛椕婡娭) |
|
|||
| 嶳宍導丂乮 8堛椕婡娭) |
|
|||
| 暉搰導丂乮11堛椕婡娭) |
|
|||
| 堬忛導丂乮 7堛椕婡娭) |
|
|||
| 撊栘導丂乮10堛椕婡娭) |
|
|||
| 孮攏導丂乮 4堛椕婡娭) |
|
|||
| 嶉嬍導丂乮 6堛椕婡娭) |
|
|||
| 愮梩導丂乮 5堛椕婡娭) |
|
|||
| 搶嫗搒丂乮29堛椕婡娭) |
|
|||
| 恄撧愳導乮 8堛椕婡娭) |
|
|||
| 怴妰導丂乮 4堛椕婡娭) |
|
|||
| 晉嶳導丂乮 2堛椕婡娭) |
|
|||
| 愇愳導丂乮 8堛椕婡娭) |
|
|||
| 暉堜導丂乮 4堛椕婡娭) |
|
|||
| 嶳棞導丂乮 9堛椕婡娭) |
|
|||
| 挿栰導丂乮 4堛椕婡娭) |
|
|||
| 婒晫導丂乮 7堛椕婡娭) |
|
|||
| 惷壀導丂乮20堛椕婡娭) |
|
|||
| 嶰廳導丂乮 4堛椕婡娭) |
|
|||
| 垽抦導丂乮14堛椕婡娭) |
|
|||
| 帬夑導丂乮 2堛椕婡娭) |
|
|||
| 嫗搒晎丂乮10堛椕婡娭) |
|
|||
| 戝嶃晎丂乮14堛椕婡娭) |
|
|||
| 暫屔導丂乮11堛椕婡娭) |
|
|||
| 撧椙導丂乮 1堛椕婡娭) |
|
|||
| 榓壧嶳導乮 2堛椕婡娭) |
|
|||
| 捁庢導丂乮 2堛椕婡娭) |
|
|||
| 搰崻導丂乮 5堛椕婡娭) |
|
|||
| 壀嶳導丂乮 6堛椕婡娭) |
|
|||
| 峀搰導丂乮 5堛椕婡娭) |
|
|||
| 嶳岥導丂乮 5堛椕婡娭) |
|
|||
| 摽搰導丂乮 2堛椕婡娭) |
|
|||
| 崄愳導丂乮 5堛椕婡娭) |
|
|||
| 垽昋導丂乮20堛椕婡娭) |
|
|||
| 崅抦導丂乮 6堛椕婡娭) |
|
|||
| 暉壀導丂乮 6堛椕婡娭) |
|
|||
| 嵅夑導丂乮 2堛椕婡娭) |
|
|||
| 挿嶈導丂乮 3堛椕婡娭) |
|
|||
| 孎杮導丂乮 3堛椕婡娭) |
|
|||
| 戝暘導丂乮 6堛椕婡娭) |
|
|||
| 媨嶈導丂乮 3堛椕婡娭) |
|
|||
| 幁帣搰導乮 2堛椕婡娭) |
|
|||
| 壂撽導丂乮 3堛椕婡娭) |
|
|||
| 係俈搒摴晎導 |
|
I 堛栻昳偺埨慡惈偵娭偡傞婎杮揑峫偊曽
II 嬶懱揑採尵
| 丂嵗挿丂 | 怷丂丂丂榡 堜懞丂桾晇 忋嶁丂搤巕 嶁忋丂惓摴 嶁杮丂棿旻 墡揷丂掄抝 壓嶳丂惓摽 悰扟丂丂擡 慡揷丂丂峗 崅媣丂巎枦 崅嫶丂懃峴 撪摗丂廃岾 拞栰丂廳峴 挿旜丂丂戱 椦丂丂桾憿 塖丂丂岶堦 岝愇丂拤宧 怷壀丂栁晇 桍揷丂朚抝 | 乮壢妛媄弍夛媍媍堳丂尦搶嫗戝妛憤挿乯 乮嫗搒戝妛妛挿乯 乮昡榑壠乯 乮擔杮堛巘夛暃夛挿乯乮暯惉8擭3寧傑偱乯 乮娐嫬塹惗嬥梈岞屔棟帠挿乯 乮宑墳媊弇戝妛嫵庼乯 乮崙棫柤屆壆昦堾挿乯 乮擔杮堛巘夛忢擟棟帠乯乮暯惉8擭4寧埲崀乯 乮怣廈戝妛堛妛晹嫵庼乯 乮帺帯堛壢戝妛妛挿乯 乮擔杮栻嵻巘夛暃夛挿乯 乮搶嫗掽怣昦堾嶲梌乯 乮戝暘堛壢戝妛嫵庼乯 乮搶嫗戝妛栻妛晹嫵庼乯 乮杒棦戝妛栻妛晹媞堳嫵庼乯 乮搶嫗搒棫戝妛柤梍嫵庼乯 乮曎岇巑乯 乮擔杮惢栻抍懱楢崌夛夛挿乯 乮昡榑壠乯 |
| 擭丂師 | 怴桳岠惉暘悢 | 丂寁丂 | |
| 惢丂憿 | 桝丂擖 | ||
| 丂1992擭 丂1993擭 丂1994擭 丂1995擭 丂1996擭 |
丂侾俋 丂俀侾 丂俀俁 丂侾係 丂丂俉 |
丂侾俀 丂侾俋 丂俀俀 丂侾俀 丂侾俇 |
丂俁侾 丂係侽 丂係俆 丂俀俆仏 丂俀係 |
| 楌 擭 |
嬫丂暘 | 惢憿乮桝擖乯彸擣娭學 | 惢憿乮桝擖乯嫋壜娭學 | 崌丂寁 | |||||
| 怴婯彸擣 | 堦曄彸擣 | 寁 | 捛壛丒曄峏 | 嬈嫋壜 | 峏怴嫋壜 | 寁 | |||
| 暯 惉 俇 擭 |
堛丂栻丂昳 堛栻晹奜昳 壔丂徬丂昳 堛椕梡嬶 丂崌丂寁 |
3,545 4,175 980 2,645 11,345 |
1,716 370 5 2,170 4,261 |
5,261 4,545 985 4,815 15,606 |
6,008 5,741 12,455 8,327 32,531 |
159 76 208 425 868 |
1,376 625 473 1,065 3,539 |
7,543 6,442 12,982 9,817 36,784 |
12,804 10,987 13,967 14,632 52,390 |
| 暯 惉 俈 擭 |
堛丂栻丂昳 堛栻晹奜昳 壔丂徬丂昳 堛椕梡嬶 丂崌丂寁 |
1,883 2,150 1,378 2,622 8,033 |
2,040 441 246 1,925 4,652 |
3,923 2,591 1,624 4,547 12,685 |
* 2,715 * 2,343 * 905 8,988 14,951 |
* 69 * 43 * 104 369 585 |
* 353 * 131 * 171 962 1,617 |
* 3 137 * 2,517 * 1,180 10,319 17,153 |
7,060 5,108 2,804 14,866 29,838 |
| 暯 惉 俉 擭 |
堛丂栻丂昳 堛栻晹奜昳 壔丂徬丂昳 堛椕梡嬶 丂 丂崌丂寁 |
2,440 1,932 828 2,027 |
1,473 212 432 1,904 |
3,913 2,144 1,260 3,931 |
* 1,200 * 21 0 4,142 (56) |
* 10 0 0 2,993 (2,616) |
* 56 0 0 1,077 |
* 1,266 * 21 0 8,212 (2,672) |
5,179 2,165 1,260 16,285 |
侾俀丏堛椕婡婍嶻嬈偺尰忬
仜惗嶻妟丄桝弌擖妟摍偺悇堏
| 擭 | 惗丂嶻丂妟 | 慜擭斾 | 桝丂弌丂妟 | 桝丂擖丂妟 | 崙撪弌壸妟 |
| 俀擭 | 1挍 2,742壄墌 | 4.5% | 2,898壄墌 | 2,887壄墌 | 1挍 2,639壄墌 |
| 俁擭 | 1挍 2,976壄墌 | 1.8% | 3,176壄墌 | 3,315壄墌 | 1挍 2,964壄墌 |
| 係擭 | 1挍 3,659壄墌 | 5.3% | 3,316壄墌 | 3,943壄墌 | 1挍 4,154壄墌 |
| 俆擭 | 1挍 3,348壄墌 | -2.3% | 3,032壄墌 | 4,567壄墌 | 1挍 4,710壄墌 |
| 俇擭 | 1挍 3,177壄墌 | -1.3% | 2,857壄墌 | 5,012壄墌 | 1挍 5,498壄墌 |
| 俈擭 | 1挍 3,366壄墌 | 1.4% | 2,689壄墌 | 5,887壄墌 | 1挍 6,330壄墌 |
仜庡梫暘椶暿惗嶻嬥妟乮暯惉俈擭乯[扨埵丗壄墌丄亾]
| 丂 | 暘丂丂椶 | 惗嶻嬥妟 | 峔惉斾 | 戙丂昞丂椺 |
| 侾 | 夋憸恌抐梡憰抲 | 2,633 | 19.7 | 恌抐梡倃慄憰抲丄俵俼俬 |
| 俀 | 張抲梡婡夿婍嬶 | 1,453 | 10.9 | 拲幩婍丄僠儏乕僽丄僇僥乕僥儖 |
| 俁 | 惗懱婡擻曗彆丒戙峴婍 | 1,438 | 10.8 | 恖岺恡憻丄儁乕僗儊乕僇乕 |
| 係 | 壠掚梡帯椕婍 | 1,181 | 8.8 | 壠掚梡掅廃攇帯椕婍丄帴婥帯椕婍 |
| 俆 | 堛梡曻幩慄娭楢憰抲媦傃惢昳 | 1,037 | 7.8 | 倃慄僼傿儖儉丄杊岇梡嬶 |
| 俇 | 娽壢梡昳媦傃娭楢惢昳 | 1,036 | 7.7 | 娽嬀丄僐儞僞僋僩儗儞僘丄娽撪儗儞僘 |
| 俈 | 帟壢嵽椏 | 792 | 5.9 | 帟壢梡嬥懏丄帟壢梡報徾嵽椏 |
| 俉 | 堛梡専懱専嵏婡婍 | 704 | 5.3 | 椪彴壔妛専嵏梡婡婍丄寣塼専嵏婡婍 |
| 俋 | 恌抐梡婡夿婍嬶 | 665 | 5.0 | 僼傽僀僶乕僗僐乕僾丄娽嶣塭憰抲丄挳恌婍 |
| 10 | 偦偺懠 | 2,428 | 18.2 | 帟壢梡帯椕戜丄揹巕幃寣埑寁丄僐儞僪乕儉丄庤弍戜徴寕攇寢愇攋嵱憰抲丄屇媧婡擻専嵏婡婍丄儊僗摍 |
| 丂 | 寁 | 13,366 | 100.0 | 丂 |
仜庡梫暘椶暿桝弌擖妟乮暯惉俈擭乯[扨埵丗昐枩墌丄亾]
丒桝 弌
|
丒桝 擖
|
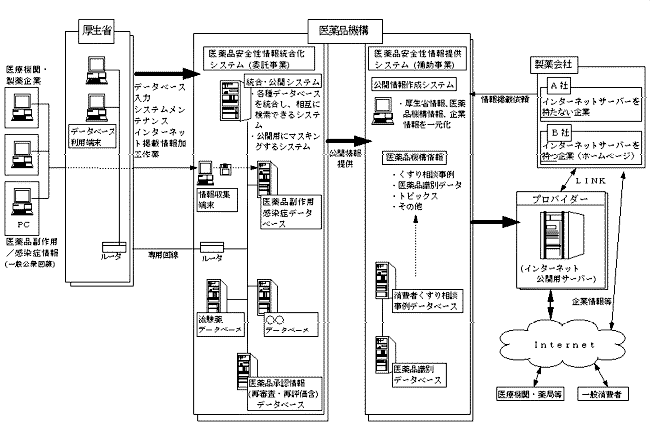
| 丂 | 丂 | 乽僟儊丅僛僢僞僀丅乿 崙楢巟墖曞嬥 1993擭搙曞嬥妟 | 乽僟儊丅僛僢僞僀丅乿 崙楢巟墖曞嬥 1994擭搙曞嬥妟 | 乽僟儊丅僛僢僞僀丅 乿崙楢巟墖曞嬥 1995擭搙曞嬥妟 | 乽僟儊丅僛僢僞僀丅乿 崙楢巟墖曞嬥 1996擭搙曞嬥妟 | 儎儞僌 戝巊 攈尛擭 |
| 1 | 杒奀摴 | 1,870,925 | 1,471,733 | 2,107,563 | 1,343,946 | 96/3 |
| 2 | 惵怷 | 932,088 | 1,211,623 | 1,180,540 | 1,368,780 | 丂 |
| 3 | 娾庤 | 660,649 | 921,582 | 1,807,450 | 830,708 | 丂 |
| 4 | 媨忛 | 2,507,485 | 4,344,159 | 4,048,585 | 4,005,398 | 95/3 |
| 5 | 廐揷 | 1,848,796 | 1,103,813 | 1,340,454 | 1,374,245 | 97/3 |
| 6 | 嶳宍 | 613,354 | 781,125 | 951,715 | 781,766 | 丂 |
| 7 | 暉搰 | 3,053,659 | 3,896,437 | 4,887,781 | 5,537,684 | 94丒96/3 |
| 8 | 堬忛 | 5,120,016 | 3,341,491 | 3,460,261 | 3,948,368 | 94/3 |
| 9 | 撊栘 | 2,000,312 | 1,991,461 | 2,752,273 | 2,979,682 | 97/3 |
| 10 | 孮攏 | 725,111 | 1,338,493 | 872,842 | 1,298,819 | 丂 |
| 11 | 嶉嬍 | 2,519,464 | 3,558,830 | 2,672,957 | 2,987,745 | 95/3 |
| 12 | 愮梩 | 1,679,245 | 1,711,031 | 2,509,216 | 2,201,672 | 丂 |
| 13 | 搶嫗 | 4,053,342 | 4,253,919 | 3,495,294 | 4,674,183 | 丂 |
| 14 | 恄撧愳 | 1,149,557 | 1,088,589 | 1,536,695 | 3,221,390 | 丂 |
| 15 | 怴妰 | 1,017,652 | 1,324,023 | 1,030,486 | 1,408,607 | 丂 |
| 16 | 挿栰 | 1,568,938 | 2,943,076 | 3,690,143 | 3,357,494 | 96/3 |
| 17 | 嶳棞 | 1,730,036 | 2,711,599 | 2,352,186 | 2,299,059 | 97/3 |
| 18 | 惷壀 | 1,088,305 | 1,894,925 | 2,812,070 | 3,041,397 | 95/3 |
| 19 | 垽抦 | 2,243,253 | 811,155 | 4,232,586 | 3,211,868 | 94/3 |
| 20 | 婒晫 | 1,481,103 | 1,387,813 | 1,555,716 | 1,222,336 | 97/3 |
| 21 | 嶰廳 | 436,934 | 593,976 | 1,170,738 | 932,290 | 丂 |
| 22 | 晉嶳 | 1,340,268 | 1,438,762 | 1,668,641 | 1,991,494 | 96/3 |
| 23 | 愇愳 | 685,658 | 1,567,679 | 1,386,287 | 1,215,680 | 丂 |
| 24 | 暉堜 | 815,057 | 1,189,034 | 1,434,333 | 1,357,000 | 丂 |
| 25 | 帬夑 | 977,968 | 926,286 | 973,820 | 708,582 | 96/3 |
| 26 | 嫗搒 | 616,769 | 1,403,894 | 1,107,642 | 852,513 | 95/3 |
| 27 | 戝嶃 | 1,297,474 | 3,784,502 | 4,281,739 | 6,231,198 | 94丒97/3 |
| 28 | 暫屔 | 730,003 | 1,464,193 | 1,052,269 | 1,569,118 | 97/3 |
| 29 | 撧椙 | 117,429 | 191,382 | 467,599 | 651,920 | 丂 |
| 30 | 榓壧嶳 | 281,217 | 1,050,455 | 1,113,089 | 1,659,814 | 丂 |
| 31 | 捁庢 | 613,908 | 851,407 | 1,030,187 | 940,600 | 丂 |
| 32 | 搰崻 | 1,997,089 | 1,563,210 | 1,549,906 | 1,598,789 | 97/3 |
| 33 | 壀嶳 | 1,638,098 | 1,961,008 | 3,645,643 | 3,206,039 | 96/3 |
| 34 | 峀搰 | 2,050,123 | 2,618,712 | 3,184,857 | 2,761,266 | 95/3 |
| 35 | 嶳岥 | 2,643,382 | 4,675,380 | 4,571,036 | 3,744,510 | 94/3 |
| 36 | 摽搰 | 730,239 | 1,176,885 | 1,342,016 | 1,790,949 | 丂 |
| 37 | 崄愳 | 62,015 | 197,255 | 461,063 | 498,347 | 丂 |
| 38 | 垽昋 | 77,120 | 2,134,170 | 2,313,294 | 2,778,330 | 96/3 |
| 39 | 崅抦 | 627,423 | 2,539,461 | 1,488,384 | 1,405,939 | 95/3 |
| 40 | 暉壀 | 73,549 | 476,381 | 890,141 | 1,525,092 | 丂 |
| 41 | 嵅夑 | 1,325,002 | 1,611,441 | 1,389,474 | 1,379,347 | 丂 |
| 42 | 挿嶈 | 65,850 | 2,275,515 | 1,901,875 | 1,554,907 | 丂 |
| 43 | 孎杮 | 427,731 | 4,980,207 | 3,274,701 | 3,124,423 | 95/3 |
| 44 | 戝暘 | 2,281,148 | 2,555,132 | 2,449,063 | 2,785,606 | 97/3 |
| 45 | 媨嶈 | 527,610 | 892,125 | 814,697 | 652,373 | 丂 |
| 46 | 幁帣搰 | 3,472,396 | 4,287,427 | 3,364,314 | 3,147,722 | 94/3 |
| 47 | 壂撽 | 2,136,369 | 2,541,201 | 3,041,522 | 2,682,666 | 96/3 |
| 崌 寁丂 | 65,911,119 | 93,033,955 | 100,665,143 | 103,841,661 | 29恖 | |