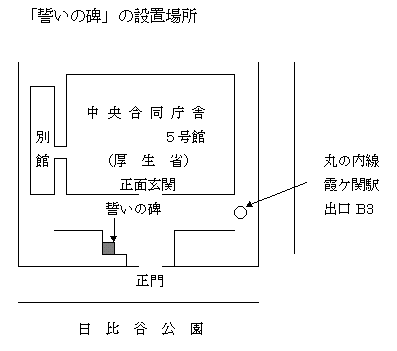
堛栻昳偵傛傞寬峃旐奞偺杊巭嶔
丂岤惗徣偵偍偒傑偟偰偼丄堛栻昳偺桳岠惈丒埨慡惈偺妋曐偺偨傔偺奺斒偵傢偨傞巤嶔傪悇恑偟丄堛栻昳偵傛傞寬峃旐奞偺杊巭偵枩慡傪婜偟偰偄傞偲偙傠偱偡丅
偙偺傛偆側拞偱暯惉11擭俉寧24擔偵偼丄俫俬倁慽徸偺榓夝偵婎偯偔捔嵃丒堅楈偺慬抲偲偟偰丄HIV姶愼偺傛偆側堛栻昳偵傛傞斶嶴側旐奞傪嵞傃敪惗偝偣傞偙偲偺側偄傛偆堛栻昳偺桳岠惈丒埨慡惈偺妋曐偵嵟慞偺搘椡傪廳偹傞寛堄傪柫婰偟偨乽惥偄偺旇乿傪岤惗徣慜掚偵寶棫偟偨偲偙傠偱偡丅
杮儂乕儉儁乕僕偱偼丄偙偺傛偆側岤惗徣偵偍偗傞堛栻昳偵傛傞寬峃旐奞偺杊巭嶔偵偮偄偰徯夘偟傑偡丅
乮徠夛愭乯
岤惗徣堛栻埨慡嬊婇夋壽
堛栻昳暃嶌梡旐奞懳嶔幒
丂嶰丂怷乮撪慄俀俈侾俈乯
堛栻昳偺桳岠惈丄埨慡惈偺妋曐偺偨傔偺庢慻
乣堛栻昳偵傛傞寬峃旐奞偺杊巭嶔乣
侾. 堛栻昳偺彸擣怰嵏懱惂偺廩幚摍
- 仜 堛栻昳堛椕婡婍怰嵏僙儞僞乕偺愝抲
- 丂堛栻昳摍偺彸擣怰嵏偵偮偄偰偼丄暯惉俋擭俈寧偵彸擣怰嵏帠柋傪愱栧揑偵峴偆乽堛栻昳堛椕婡婍怰嵏僙儞僞乕乿傪愝抲偟丄廬棃偺栻妛丄堛妛偵壛偊丄廱堛妛丄摑寁妛摍傪愱栧偲偡傞怰嵏姱傪壛偊偨乽僠乕儉怰嵏乿偺幚巤傗丄怰嵏曬崘彂偺嶌惉傪捠偠偰丄怰嵏偺幙偺岦忋傗愑擟偺柧妋壔傪恾傞側偳帠柋嬊偺怰嵏懱惂偺嫮壔傪恾偭偨丅
- 仜 怰嵏姱摍偺攞憹
- 丂暯惉俋擭搙偐傜俁擭娫偱岤惗杮徣丄堛栻昳堛椕婡婍怰嵏僙儞僞乕丄堛栻昳暃嶌梡旐奞媬嵪丒尋媶怳嫽挷嵏婡峔偺怰嵏姱摍偺攞憹傗懱惂偺惍旛傪恑傔偰偒偨偲偙傠偱偁傝丄崱屻偲傕壢妛媄弍偺恑曕摍偺忬嫷偺曄壔偵墳偠偰丄昁梫側懱惂偺惍旛摍偵庢傝慻傓丅
- 仜 帯尡偺廩幚
- 丂暯惉俉擭偺栻帠朄夵惓偵傛傝丄暯惉10擭係寧傛傝乽堛栻昳偺椪彴帋尡偺幚巤偺婎弨乿乮俧俠俹乯偺弲庣傪堛栻昳惢憿嬈幰丄帯尡幚巤堛椕婡娭摍偵媊柋晅偗傞偲偲傕偵丄暯惉俋擭係寧傛傝堛栻昳婡峔偵傛傞怽惪帒椏偺婎弨揔崌惈挷嵏傪幚巤偟偰偄傞丅
- 仜 拞墰栻帠怰媍夛偺尒捈偟
- 丂暯惉11擭11寧偵丄拞墰栻帠怰媍夛偵偮偄偰丄傛傝岠棪揑偐偮廫暘側怰嵏傪峴偆娤揰偐傜丄怴栻摍偺彸擣怰嵏偵學傞晹夛偺奐嵜夞悢偺憹壛摍傪恾傞偲偲傕偵丄堛栻昳堛椕婡婍怰嵏僙儞僞乕偺僠乕儉怰嵏偵愱栧埾堳偑嶲夋偡傞愱栧嫤媍曽幃傪摫擖偟偨丅
俀丏堛栻昳埨慡惈忣曬偺廂廤丒昡壙懱惂偺嫮壔
- 仜 堛栻昳惢憿嬈幰摍偐傜偺忣曬廂廤
- 丂暯惉俉擭偺栻帠朄夵惓偵傛傝丄岤惗戝恇傊偺暃嶌梡丒姶愼徢曬崘傪堛栻昳惢憿嬈幰摍偺媊柋偲偟偰婯掕偡傞偲偲傕偵丄堛椕梡堛栻昳偵偮偄偰偼丄惢憿嬈幰摍偵偍偗傞忣曬廂廤丒採嫙偺懱惂丄幮撪嫵堢摍傪婯掕偡傞乽堛栻昳偺巗斕屻挷嵏偺婎弨乿乮俧俹俵俽俹乯傪朄惂壔偟偨丅
- 仸 堛栻昳惢憿嬈幰摍偐傜偺曬崘審悢丟暯惉10擭搙 18,466審丄暯惉11擭搙 20,031審
- 仜 堛椕婡娭丒栻嬊偐傜偺忣曬廂廤
- 丂暯惉俋擭俈寧偐傜丄堛栻昳摍埨慡惈忣曬曬崘惂搙傪敪懌偝偣丄慡偰偺堛椕婡娭媦傃栻嬊偐傜丄岤惗徣偑捈愙堛栻昳偺暃嶌梡摍偺曬崘傪庴偗傞惂搙傪惍旛偟偨丅
- 仸 堛椕婡娭摍偐傜偺曬崘審悢丟暯惉10擭搙 4,882審丄暯惉11擭搙 5,502審
- 仜 奀奜忣曬偺廂廤
- 丂倂俫俷崙嵺堛栻昳儌僯僞儕儞僌惂搙丄惢憿嬈幰摍偐傜偺埨慡惈掕婜曬崘乮俹俽倀俼乯偵壛偊偰丄俥俢俙摍偺彅奜崙摉嬊偐傜偺忣曬廂廤儖乕僩偺惍旛摍偵傛傝丄奀奜忣曬傪恦懍丄揑妋偵擖庤偟偰偄傞丅
俁丏堛栻昳偵娭偡傞忣曬採嫙懱惂偺惍旛
- 仜 拞墰栻帠怰媍夛偺媍帠榐岞奐
- 丂拞墰栻帠怰媍夛偺媍帠榐偵偮偄偰偼丄暯惉俋擭俆寧傛傝丄屄恖偺旈枾丒婇嬈偺抦揑嵿嶻尃摍偵學傞晹暘傪彍偒丄彸擣屻岞奐偟偰偄傞丅
- 仜 堛栻昳忣曬採嫙僔僗僥儉偺峔抸
- 丂堛椕娭學幰摍偵懳偟偰堛栻昳偺埨慡惈偵娭偡傞忣曬傪採嫙偡傞偨傔丄堛栻昳婡峔傪嫆揰偵丄僀儞僞乕僱僢僩傪妶梡偟偨乽堛栻昳忣曬採嫙僔僗僥儉乿帠嬈傪暯惉11擭俆寧傛傝奐巒偟偨丅
傑偨丄暯惉12擭係寧傛傝丄栻帠朄偵婎偯偔偡傋偰偺堛栻昳丄堛椕梡嬶摍偺夞廂忣曬偵偮偄偰傕宖嵹偟偰偄傞丅
- 仜 怴栻忣曬彸擣廤偺嶌惉
- 丂怴栻偵娭偡傞忣曬偵偮偄偰偼丄暯惉俉擭10寧偐傜丄慡偰偺怴栻偵偮偄偰丄昳栚偛偲偵彸擣怰嵏偺宱夁丄昡壙寢壥媦傃偦偺崻嫆側偳傪傑偲傔偨怰嵏曬崘彂傪岞昞偟偰偒偰偄傞偲偙傠偱偁傞偑丄暯惉11擭11寧傛傝丄偙傟偵椪彴帋尡僨乕僞傪娷傓怽惪帒椏傪偲傝傑偲傔偨乽怴栻彸擣忣曬廤乿傪嶌惉偟丄彸擣屻偵岞昞偟偰偄傞丅
側偍丄乽堛栻昳忣曬採嫙僔僗僥儉乿偵偍偄偰傕丄偦偺撪梕傪僀儞僞乕僱僢僩偵傛傝忣曬採嫙偟偰偄傞丅
- 仜 乽堛栻忣曬幒乿偺怴愝
- 丂忣曬岞奐朄偺惂掕傪摜傑偊丄墌妸側忣曬岞奐偺幚巤傪恾傞娤揰偐傜丄杮擭係寧丄堛栻埨慡嬊婇夋壽偵乽堛栻忣曬幒乿傪愝抲偟偨丅
係丏婋婡娗棟懱惂偺峔抸
- 仜 乽堛栻昳摍寬峃婋婡娗棟幚巤梫椞乿偺嶔掕
- 丂岤惗徣偵偍偗傞婋婡娗棟懱惂偵偮偄偰偼丄暯惉俋擭侾寧偵乽岤惗徣寬峃婋婡娗棟婎杮巜恓乿傪嶔掕偡傞偲偲傕偵丄暯惉俋擭係寧偵乽堛栻昳摍寬峃婋婡娗棟幚巤梫椞乿傪掕傔丄埨慡懳嶔偺幚巤偵帄傞傑偱偺庤弴傗婎弨媦傃奺抜奒偵偍偗傞愑擟偺強嵼傪柧妋壔偟丄堛栻昳摍偵傛傞寬峃婋婡偵恦懍偐偮揔愗偵懳墳偟偰偄傞丅
俆丏惥偄偺旇偺寶棫
丂暯惉11擭俉寧偵丄堛栻昳偺埨慡惈媦傃桳岠惈偺妋曐偵嵟慞偺搘椡傪廳偹偰偄偔偙偲傪柫婰偡傞乽惥偄偺旇乿傪寶棫偟偨丅
俇丏寣塼帠嬈偺尒捈偟
- 仜 寣塼帠嬈朄乮壖徧乯偺惂掕
- 丂暯惉俋擭12寧偵乽寣塼峴惌偺嵼傝曽偵娭偡傞崸択夛偺曬崘彂乿偑庢傝傑偲傔傜傟丄暯惉10擭俁寧傛傝丄乽拞墰栻帠怰媍夛婇夋丒惂搙夵惓摿暿晹夛乿偵偍偄偰怰媍偑恑傔傜傟偰偄傞丅
- 仜 寣塼惢嵻偺埨慡惈偺妋曐
- 丂暯惉11擭10寧偵丄廬棃偺寣燋暘夋惢嵻偵壛偊偰桝寣梡寣塼惢嵻偵懳偟偰傕丄悽奅偵愭嬱偗偰丄俫俛倁丄俫俠倁丄俫俬倁偵學傞俶俙俿乮妀巁憹暆朄乯専嵏偺摫擖偑恾傜傟偨丅
- 仜 寣塼惢嵻偺揔惓巊梡偺悇恑
- 丂寣塼惢嵻偺揔惓巊梡偺悇恑傪恾傞偨傔丄暯惉11擭俇寧偵丄廬棃偺巊梡婎弨摍傪尒捈偟丄怴偨偵乽寣塼惢嵻偺巊梡巜恓乿媦傃乽桝寣椕朄偺幚巤偵娭偡傞巜恓乿傪嶔掕偟偨丅
- 仸 侾恖摉偨傝偺惢嵻偺巊梡忬嫷;傾儖僽儈儞惢嵻 暯惉俆擭搙 98g仺暯惉10擭搙 54g
乽惥偄偺旇乿偵偮偄偰
|
惥偄偺旇
柦偺懜偝傪怱偵崗傒僒儕僪儅僀僪丄僗儌儞丄俫俬倁姶愼偺傛偆側堛栻昳偵傛傞斶嶴側旐奞傪嵞傃敪惗偝偣傞偙偲偺側偄傛偆堛栻昳偺埨慡惈丒桳岠惈偺妋曐偵嵟慞偺搘椡傪廳偹偰偄偔偙偲傪偙偙偵柫婰偡傞
愮悢昐柤傕偺姶愼幰傪弌偟偨乽栻奞僄僀僘乿帠審
偙偺傛偆側帠審偺敪惗傪斀徣偟偙偺旇傪寶棫偟偨
暯惉侾侾擭俉寧 岤惗徣
|
仜 俧俠俹丗Good Clinical Practice乮堛栻昳偺椪彴帋尡偺幚巤偺婎弨乯
丂
堛栻昳偺奐敪偺嵟廔抜奒偵偍偄偰偼丄僸僩傪懳徾偲偟偨椪彴帋尡乮帯尡乯偵傛傞栻暔偺椪彴揑側昡壙偑昁梫晄壜寚偱偁傝丄偙偙偱廂廤偝傟偨帒椏摍偵婎偯偒堛栻昳偺惢憿枖偼桝擖偺偨傔偺彸擣怽惪偑峴傢傟傞丅偙偺帯尡偺幚巤偵摉偨偭偰偼丄旐尡幰偺恖尃偲埨慡偵偮偄偰廫暘側攝椂偑側偝傟傞偙偲傪慜採偲偟偰丄帯尡偺壢妛揑側幙偲惉愌偺怣棅惈偑妋曐偝傟偰偄傞偙偲偑昁恵偲側傞丅
丂偙偺傛偆側娤揰偐傜嶔掕偝傟偨婎弨偑乽堛栻昳偺椪彴帋尡偺幚巤偺婎弨乮俧俠俹乯乿偱偁傝丄変偑崙偵偍偄偰偼丄暯惉尦擭偵栻柋嬊挿捠抦偵傛傞峴惌巜摫偲偟偰嵟弶偺俧俠俹偑掕傔傜傟偨丅
丂 偦偺屻丄帯尡偺傛傝堦憌偺揔惓側幚巤丄峏偵偼墷暷偲偺娫偱俧俠俹偺崙嵺揑挷榓傪恾傞娤揰偐傜丄俧俠俹偺撪梕傪夵掕偡傞偲偲傕偵丄暯惉俉擭俇寧偺栻帠朄夵惓偵傛傝俧俠俹偺崻嫆婯掕傪惍旛偟丄帯尡傪埶棅偡傞帯尡埶棅幰乮惢栻婇嬈乯偺傒側傜偢丄帯尡傪幚巤偡傞堛椕婡娭媦傃帯尡傪扴摉偡傞幰偵懳偟偰丄偦偺弲庣傪媊柋晅偗傞偙偲偲側偭偨丅
丂婎弨偺撪梕偵偮偄偰偼丄暯惉俋擭俁寧偵乽堛栻昳偺椪彴帋尡偺幚巤偺婎弨偵娭偡傞徣椷乮暯惉俋擭俁寧岤惗徣椷戞俀俉崋乯乿偵傛傝掕傔傜傟丄暯惉侾侽擭係寧偐傜慡柺巤峴偝傟偰偄傞丅
仜 俧俠俹偺撪梕
丂暯惉侾侽擭係寧偐傜慡柺巤峴偝傟偨俧俠俹偼丄埲慜偺俧俠俹偵斾傋師偺摿挜傪桳偡傞丅
乮侾乯旐尡幰偲側傞傋偒幰偵懳偡傞帯尡偵娭偡傞暥彂偵傛傞愢柧偲摨堄偺庢摼
乮俀乯帯尡憤妵堛巘惂搙偺攑巭
乮俁乯帯尡埶棅幰偺愑擟斖埻偺奼戝偲嫮壔
- 傾丏嬈柋庤弴彂丄帯尡幚巤寁夋彂丄帯尡栻奣梫彂摍偺嶌惉媊柋
僀丏儌僯僞儕儞僌丒娔嵏摍偺帯尡娗棟偺幚巤
僂丏帯尡憤妵曬崘彂偺嶌惉
乮係乯帯尡怰嵏埾堳夛偺婡擻偺廩幚
- 傾丏奜晹埾堳丄旕愱栧壠埾堳偺嶲壛偺媊柋晅偗
僀丏怰嵏婡擻丄愑柋偺柧妋壔
乮俆乯帯尡愑擟堛巘偺愑擟偲嬈柋偺柧妋壔
乮俇乯堛椕婡娭偵偍偗傞帯尡帠柋嬊偺嫮壔
亂堛栻昳摍埨慡惈忣曬曬崘惂搙亃
丂
崙偑捈愙丄堛巘丄帟壢堛巘丄栻嵻巘摍偺堛椕娭學幰偐傜堛栻昳丄堛椕梡嬶摍偺暃嶌梡徢椺偺曬崘傪廂廤偡傞惂搙丅堛巘摍偺帺敪揑側曬崘傪廂廤偡傞傕偺偱丄偄傢備傞帺敪曬崘惂搙偱偁傞丅
丂曬崘審悢偺憹壛傪恾傞偨傔丄暯惉俋擭俈寧傛傝廬棃峴偭偰偒偨奺庬儌僯僞乕惂搙乮堛栻昳暃嶌梡儌僯僞乕惂搙丄堛椕梡嬶儌僯僞乕惂搙丄栻嬊儌僯僞乕惂搙乯傪摑崌丒奼戝偟偰丄偡傋偰偺堛椕婡娭媦傃栻嬊傪懳徾巤愝偵丄堛巘丄帟壢堛巘丄栻嵻巘傪曬崘幰偲偡傞乽堛栻昳摍埨慡惈忣曬曬崘惂搙乿傪敪懌偝偣偨丅
丂偙偺惂搙偱偼丄堦斒栻傪娷傓堛栻昳丄堛椕梡嬶偺巊梡偺寢壥傒偲傔傜傟偨暃嶌梡丄姶愼徢丄晄嬶崌偵娭偡傞忣曬乮堛栻昳摍偲偺場壥娭學偑柧妋偱側偄傕偺傪娷傔傞乯傪廂廤偡傞偙偲偲偟偰偄傞丅
| 擭 搙 |
儌僯僞乕曬崘丒
堛栻昳摍埨慡惈忣曬曬崘悢 |
| 暯惉俇擭搙 |
1,615審 |
| 暯惉俈擭搙 |
1,859審 |
| 暯惉俉擭搙 |
1,914審 |
| 暯惉俋擭搙 |
3,730審 |
| 暯惉10擭搙 |
4,882審 |