<照会先>厚生労働省雇用均等・児童家庭局母子保健課 電話:03−5253−1111(内線7939) |
生殖補助医療研究目的でのヒト受精胚の作成・利用について
<経緯>
○ 総合科学技術会議意見「ヒト胚の取扱いに関する基本的考え方」(平成16年7月)に基づき、平成17年、生殖補助医療研究目的でのヒト受精胚の作成・利用に関するガイドラインの作成に向け、文科・厚労の両省で検討を開始。
○ 平成21年1月26日、両省の合同による専門委員会※において、ガイドラインを作成する上で基本的考え方となる報告書(案)を取りまとめ。
※科学技術・学術審議会 生命倫理・安全部会 生殖補助医療研究専門委員会
厚生科学審議会 科学技術部会 ヒト胚研究に関する専門委員会
○ その後、科学技術・学術審議会生命倫理・安全部会及び厚生科学審議会科学技術部会における審議を経て、本報告書を最終的に取りまとめ。
○ 報告書(PDF:325KB)
<報告書のポイント>
(1)検討の対象
○ 生殖補助医療の向上に資する研究でヒト受精胚の作成を伴うもの。
(2)作成されるヒト受精胚の取扱い等
○ 取扱期間は、受精後14日以内(原始線条の形成前まで)。
○ 人又は動物への胎内移植は禁止。
○ 研究終了後は、速やかに廃棄。
○ 作成したヒト受精胚の他の機関への移送は禁止。
(3)研究に必要な配偶子(卵子、精子)の入手の在り方
○ 基本的考え方
・配偶子の提供は、無償とする。
・いわゆる「無償ボランティア」からの卵子の採取は、当面禁止
・自由意思によるインフォームド・コンセントの確保
・提供の際の、肉体的侵襲や精神的負担の最小化(特に卵子)
・提供者の個人情報の保護
○ 研究への提供が認められる卵子
(1)生殖補助医療に用いられない卵子(非受精卵や不要化した凍結卵子等)
(2)手術等により摘出された卵巣や卵巣切片から採取された卵子
(3)生殖補助医療目的で採取する卵子の一部※
−卵子の提供について、一般的な広報手段(ポスター等)により情報を入手した後に、本人から自発的な申し出があった場合
−採取する卵子の一部を研究に提供する機会があることについて、主治医等から患者に対して情報提供が行われた後に、本人から申し出があった場合
| ┌ │ │ │ │ │ │ └ |
※(3)については、次の事項を機関内倫理審査委員会が事前及び事後に確認することを条件に、提供を認める。 ・採取の際、提供者に本来の治療目的以上の侵襲を加えないこと。 ・排卵誘発剤の過剰な使用等の疑念が持たれないよう、その使用量など治療の詳細な記録を保存。 ・インフォームド・コンセントの際、結果として治療成績の低下につながる可能性があることを説明。 ・写真等による採取した卵子の数や形状等の記録。 |
┐ │ │ │ │ │ │ ┘ |
(4)インフォームド・コンセント
○ 卵子の提供について、具体的な研究内容が確定していない段階でのインフォームド・コンセントを禁止。(将来の研究利用のための保存についてのインフォームド・コンセントは可。)
○ インフォームド・コンセントは原則、いつでも撤回可能。
○ 提供者が医療の過程にある場合は、提供機関が「説明者」を配置。
○ 提供者が医療の過程にある場合、提供者の医療に直接関与せず、提供者保護を最優先に行う「説明者」から、インフォームド・コンセントの説明を行う。
○ その他、提供が認められる卵子等に応じた要件・手続。
(5)研究実施の要件
○ 提供機関と研究実施機関が別の場合、同一の場合、それぞれについて検討。
(1)研究実施機関
・研究実施機関の要件、研究実施機関の長の責務と要件、研究責任者の責務と要件、研究実施者の責務と要件
(2)提供機関
・提供機関の要件、提供機関の長の責務と要件
(3)機関内倫理審査委員会(構成員の要件、関係者の審査への参画の制限、議事内容の原則公開)
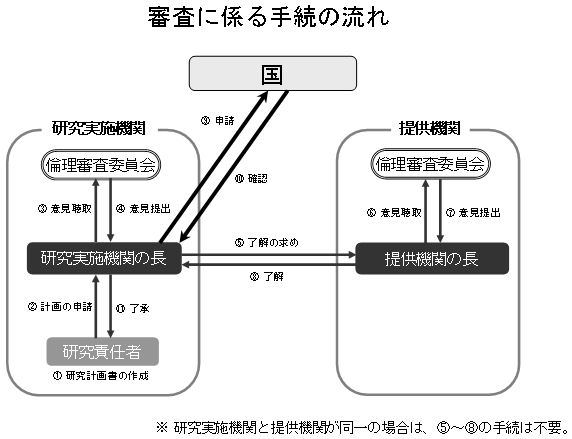
(6)研究実施の手続等
○ 研究計画の妥当性について、研究実施機関、提供機関それぞれの機関内倫理審査委員会において審査を行い、それぞれの機関の長の了承(了解)を得る。
○ 研究計画の指針適合性を国が確認。
○ 研究実施機関の長は、作成される受精胚の管理状況を定期的に国に報告。
(7)個人情報の保護等
○ 提供機関において、提供者の個人情報を匿名化。
○ 研究実施機関において、「個人情報管理者」(個人情報の管理を行う責任者)を設置。
○ その他、医学研究に関連する倫理指針と同様の措置を講ずる。
○ 研究成果は、原則公開。
PDFファイルを見るためには、Adobe Readerというソフトが必要です。
Adobe Readerは無料で配布されています。(次のアイコンをクリックしてください。) Get Adobe Reader
