|
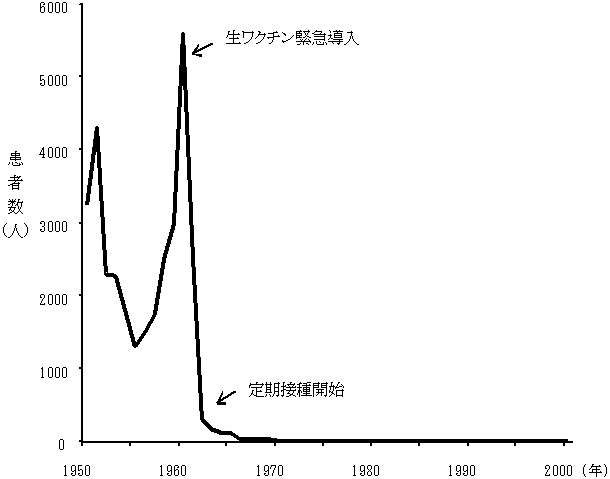
資料2−1 我が国のポリオ制圧の歩み
|
|
出典:厚生省 『伝染病統計』による。 |
資料2−2 生ポリオワクチンの副反応
生ポリオワクチンの副反応 (1970-2001)| 年 | 地域 | 年令 | 性別 | ワクチン | 型 | 材料 | |
| 1970 | 岩手 | 2Y1M | F | 無 | P2 | 糞便 | |
| 東京 | 7M | M | 有 (1) | P3 | 糞便 | ||
| 北海道 | 11M | F | 有 (1) | P2 | 糞便 | ||
| 1971 | 福岡 | 31Y | M | 無 | P2 | 糞便 | |
| 1972 | 愛知 | 1Y3M | M | 有 (1) | P2+P3 | 糞便 | |
| 北海道 | 9M | M | 無 | P2 | 糞便 | ||
| 1973 | 富山 | 8M | M | 有 (1) | P2 | 糞便 | |
| 北海道 | 5M | M | 無 | P2 | 糞便 | ||
| 北海道 | 3Y3M | M | 無 | P2 | 糞便1) | ||
| 群馬 | 1Y6M | M | 無 | P3 | 糞便2) | ||
| 広島 | 7M | M | 有 (1) | P2 | 糞便 | ||
| 1974 | 山梨 | 3Y11M | M | 無 | P2 | 糞便2) | |
| 神奈川 | 1Y2M | M | 無 | P2 | 糞便2) | ||
| 1975 | 福岡 | 10M | M | 有 (1) | P1+P2+P3 | 糞便 | |
| 1977 | 神奈川 | 1Y3M | M | 有 (1) | P2 | 糞便 | |
| 北海道 | 2Y10M | M | 免3) 有 (2) | P2 | 糞便 | ||
| 1978 | 福岡 | 10M | M | 有 (1) | P2+P3 | 糞便 | |
| 1979 | 広島 | 1Y2M | F | 免 有 (2) | P2 | 糞便1) | |
| 1980 | 大阪 | 8Y8M | F | 無 | P2 | 糞便 | |
| 熊本 | 5M | M | 無 | P2+P3 | 糞便 | ||
| 長崎 | 8M | M | 有 (1) | P2+P3 | 糞便 | ||
| 1981 | 愛知 | 8M | M | 有 (1) | P2 | 糞便 | |
| 富山 | 9M | M | 有 (1) | P2+P3 | 糞便 | ||
| 1983 | 北海道 | 1Y1M | M | 有 (1) | P2 | 糞便 | |
| 1985 | 東京 | 5M | M | 無 | P2 | 糞便 | |
| 1986 | 福岡 | 10M | M | 有 (1) | P3 | 糞便 | |
| 1991 | 大阪 | 9M | M | 有 (1) | P2+P3 | 糞便 | |
| 1992 | 福岡 | 8M | M | 有 (1) | P3 | 糞便 | |
| 神奈川 | 4M | M | 有 (1) | P3 | 糞便 | ||
| 1993 | 福岡 | 19Y | M | 無 | P3 | 糞便 | |
| 大分 | 9M | M | 無 | P2 | 糞便1) | ||
| 北海道 | 1Y6M | M | 無 | P2 | 糞便 | ||
| 1994 | 熊本 | 6M | M | 有 (1) | P1 | 糞便 | |
| 1998 | 北海道 | 36Y | M | 無 | P1 | 糞便 | |
| 京都 | 2Y1M | M | 有 (2) | P3 | 糞便 | ||
| 2000 | 宮崎 | 37Y | M | 無 | P3 | 糞便 | |
1) 髄液からも分離 |
資料2−3 我が国におけるポリオ対策の位置付け
| 年 | 感染症対策 | 予防接種 |
| 1954 | 伝染病予防法にて 届出伝染病に指定 |
|
| 1959 | 同法にて 指定伝染病に指定 |
|
| 1961 | 予防接種法にて 不活化ワクチンが定期接種に |
|
| 1964 | 同法にて 生ワクチンが定期接種に |
|
| 1999 | 感染症法にて 2類疾病に指定 |
資料3−1 世界におけるポリオ対策の歩み
| 1980年 | 日本で最後の野生株(輸入例と推定される)によるポリオ患者の発生 |
| 1991年 | 以降、WHOアメリカ地域事務局管内(南北アメリカ大陸)からの患者発生なし |
| 1994年 | WHOアメリカ地域で根絶宣言 |
| 1997年 | 以降、西太平洋地域(アジア・太平洋諸島・オセアニア)からの患者発生なし |
| 1998年 | 以降、ヨーロッパ地域からの患者発生なし |
| 2000年 | WHO西太平洋地域にて根絶宣言 |
| 2002年 | WHOヨーロッパ地域にて根絶宣言 |
資料3−2 世界におけるポリオワクチンの使用方法
| 使用中のワクチン | 投与回数 | 投与スケジュール | 変更時期 | 備考 | |
| アメリカ | IPV | 4 | 2M, 4M, 6〜18M, 4〜6Y |
2000 | OPVは特別の場合のみ |
| オーストリア | IPV | 4 | 2, 3, 4, 13M | ||
| フランス | IPV | 4 | 2, 3, 4, 16M | すべてIPV | |
| ドイツ | IPV | 4 | 2, 3, 4, 11M | すべてIPV | |
| スウェーデン デンマーク |
IPV | 4 | 3, 5, 12M, 5Y | 昔から | |
| ノルウェー | IPV | 4 | 3, 5, 11M, 6Y | ||
| イタリア | IPV/OPV併用 | 2+2 | IPV×2 (2, 4M) OPV×2 (10M, 2Y) |
IPV2回接種後 OPV2回接種 |
|
| イギリス | OPV→IPV | 2002年に OPV→IPV へ移行予定 |
|||
| スペイン | OPV→IPV | 2, 4, 6, 18M |
資料4-1 輸入例による最近のポリオ症例
| 地域 | 発生年 | 血清型 | 症例数 | 推定されている 輸出地域 |
| ケープ・ベルデ Cape Verde |
2000 | 1 | 56 | アンゴラ |
| ミャンマー Myanmar |
2000 | 1 | 44 | インド |
| イラン Iran |
2000 | 1 | 3 | インド |
| グルジア Georgia |
2001 | 1 | 1 | インド |
| ブルガリア Bulgaria |
2001 | 1 | 3 | インド |
| ザンビア Zambia |
2001 - 2002 | 1 | 3 | アンゴラ |
|
他にも、アルジェリア(2001)等の症例が輸入例と考えられている。 出典:1) MMWR, 2000; 49: 1070 2) MMWR. 2001; 50:1033 3) MMWR. 2002; 51:253 |
資料4-2
各国で報告されているワクチン関連マヒ例
| 国・地域 | 期間 | 例数 | 年間平均 発生数 |
106ドース あたり |
報告者 |
| Canada | 1965-1988 | 16 | 0.7 | 2.4 | Varughese, 19891) |
| Latin America | 1989-1991 | 139 | 46.3 | 2.2 | Andrus, 19952) |
| USA | 1980-1994 | 125 | 8.3 | 2.4 | CDC, 19963) |
| WHO European Region | 1993 | 21 | 21.0 | WHO, 19954) | |
| England & Wales | 1985-1991 | 13 | 1.9 | 1.4 | Joce, 19925) |
| Germany (FRG) | 1963-1984 | 27 | 1.2 | 3.4 | Maass, 19876) |
| Italy | 1981-1985 | 3 | 0.6 | 2.7 | Novello, 19877) |
| Romania | 1984-1992 | 93 | 10.3 | 0.2 | Strebel, 19948) |
| India | 1999 | 181 | 181.0 | 0.2 | Kohler, 20029) |
| Japan | 1971-2000 | 33 | 1.1 | 0.3 | Yoneyama, 200110) |
| WHO Collaborative study of 6 countries |
1980-1984 | 62 | 12.4 | 3.1 | Esteves, 198811) |
|
資料4-3 ワクチン由来株によるポリオ流行
|
||||||||||||||||
| 出典: 1) MMWR. 2001. 50: 41- 2) Science. 2002; 296: 356- 3) MMWR. 2001; 50: 874- |