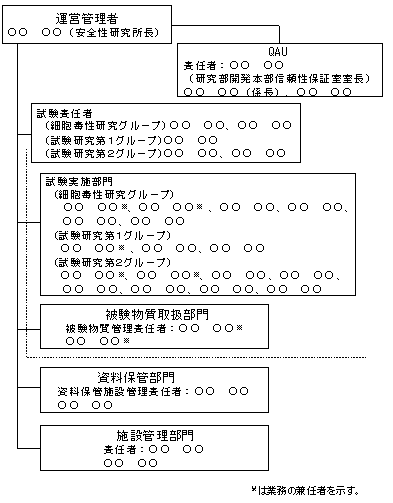
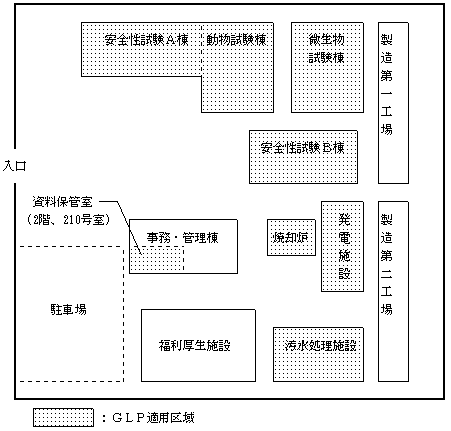
乮侾乯夛幮慻怐恾
| 丂仸 | 丂夛幮慻怐偲俧俴俹慻怐偲偺娭學偑暘偐傞傛偆偵偡傞偙偲丅 丂俧俴俹慻怐偵偮偄偰偼 丂俧俴俹慻怐庡梫怑堳偺夛幮慻怐忋媦傃俧俴俹慻怐忋偺怑柤傪婰嵹偡傞偙偲丅昁梫偵墳偠偰丄巵柤傪暪婰偡傞偙偲丅 丂暋悢応強帋尡傪幚巤偡傞応崌偼丄偦偺娭學傪婰嵹偡傞偙偲丅 |
| 乮椺乯 | 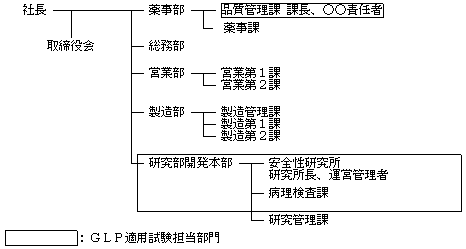 |
乮俀乯 俧俴俹慻怐恾
丂塣塩娗棟幰丄帋尡愑擟幰丄帋尡幚巤晹栧丄俻俙倀丄帒椏曐娗晹栧丄旐尡暔幙庢埖晹栧丄摦暔帞堢娗棟晹栧丄昦棟専嵏晹栧丄僔僗僥儉娗棟晹栧丄巤愝娗棟晹栧摍偵偮偄偰嬈柋婡擻偲柦椷宯摑偺傾僂僩儔僀儞偑暘傞傛偆側婰嵹偲偡傞偙偲丅偁傢偣偰丄奺愑擟幰偺巵柤丄奺晹栧偺恖堳偺巵柤傪婰嵹偡傞偙偲丅
| |||
| 乮椺乯
|
乮俁乯俧俴俹慻怐偺恖堳峔惉摍
| 丂(1) | 俧俴俹慻怐偺憤堳悢(攈尛怑堳丄椪帪怑堳丄棷妛幰摍傪娷傓)
|
| 丂(2) | 俧俴俹慻怐怑堳偺弌恎妛晹摍丄妛埵丄帒奿摍偺撪栿
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 丂(3) | 俧俴俹慻怐怑堳偺奺晹栧暿偺恖堳峔惉
| ||||||||||||||||||||||||||||||||||||||