| 遺伝子組換え食品Q&A 厚生労働省医薬食品局食品安全部 (平成16年8月3日、改訂第8版) (平成16年8月3日、安全性審査に関する部分を更新しました。) (平成18年6月13日D遺伝子組換え食品の安全性の一部を変更しました) (平成18年6月14日D遺伝子組換え食品の安全性の一部を変更しました) (平成19年10月3日D遺伝子組換え食品の安全性の一部を変更しました) (平成19年10月24日F情報公開の一部を変更しました) |
<目次>
| A−1 「バイオテクノロジー」とはどういったものですか。 |
| A−2 DNAや遺伝子とはどのようなものですか。 |
| A−3 遺伝子組換え技術(組換えDNA技術)とはどのような技術ですか。 |
| A−4 遺伝子組換え技術と従来の品種改良との違いを教えてください。 |
| A−5 遺伝子組換え技術はどのような食品に応用されていますか。 |
| A−6 遺伝子組換え技術を応用して、組換え体そのものを食べない食品添加物を作る場合とは、どのようなものですか。 |
| B−1 除草剤で枯れない仕組みとは、どのようなものですか。 |
| B−2 雄性不稔性(ゆうせいふねんせい)、稔性回復性(ねんせいかいふくせい)とはどのような性質ですか。 |
| C−1 今までに安全性審査を経た遺伝子組み換え食品を教えてください。 |
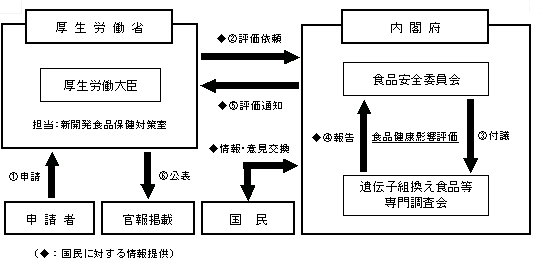
| C−2 遺伝子組換え食品の安全性審査はどのような手続きで行われるのですか。 |

| C−3 遺伝子組換え食品の安全性の審査はどのように行われるのですか。 |
| C−4 申請業者が作成した資料のみに基づいて審査を行っても大丈夫なのですか。 |
| C−5 遺伝子組換え食品の安全性評価基準は新しくなったのですか。 |
| C−6 安全性審査を受けずに遺伝子組換え食品を国内で販売することはできるのですか。 |
| C−7 安全性に問題があると判断された場合には、厚生労働省はどのような措置を取るのですか。 |
| D−1 「生産物が既存のものと同等と見なし得る」「実質的同等性」とは、どういうことですか。 |
| D−2 安全性評価のポイントは何ですか? |
| D−3 遺伝子組換え食品がアレルギーを引き起こすかどうかについては、どのような確認がされているのですか。 |
| (1) | 挿入遺伝子の供与体(抗生物質耐性マーカー遺伝子供与体を含む)のアレルギー誘発性(グルテン過敏性腸炎誘発性を含む。以下同じ。)に関する知見が明らかにされていること。 | ||||||||
| (2) | 遺伝子産物(タンパク質)についてそのアレルギー誘発性に関する知見が明らかにされていること。 | ||||||||
| (3) | 遺伝子産物(タンパク質)の物理化学的処理に対する感受性に関する事項 以下の(1)から(3)の処理によって、遺伝子産物(タンパク質)の分子量、酵素活性、免疫反応性等が変化するかどうかが明らかにされていること。分子量はSDSポリアクリルアミドゲル電気泳動によって示されていること。免疫反応性は処理前の遺伝子産物(タンパク質)に対するポリクローナル抗体を用いてウェスタンブロッティング法及びELISA法あるいはこれらと同等の方法によって示されていること。
|
||||||||
| (4) | 遺伝子産物(タンパク質)と既知のアレルゲン(グルテン過敏性腸疾患に関与するタンパク質を含む。以下アレルゲン等。)との構造相同性に関する事項 遺伝子産物(タンパク質)について、既知のアレルゲン等と一次構造を比較し、既知のアレルゲン等との構造相同性を有しないこと(抗原決定基(エピトープ)を示す可能性のある配列を明らかにするためには、アミノ酸配列に関する相同性検索などを実施する必要がある)。その際、用いたアレルゲンデータベースの名称、検索条件、検索方法、検索結果が明らかにすること。 |
||||||||
| (5) | 遺伝子産物のIgE結合能の検討 (1)から(4)までの事項等により、ヒトの健康を損なう恐れがないと判断できない時は、遺伝子産物(タンパク質)のIgE結合能を検討すること。 使用する患者血清の選択は、下記の(1)から(4)のいずれかで行う。
|
| D−4 遺伝子組換え食品でアレルギーを起こした例があると聞きましたが、本当ですか。 |
参考文献 "Identification of a Brazil-Nut Allergen in Transgenic Soybeans" (JULie A. Nordlee et al., The New England Journal of Medicine, VOL.334, No.11, March 14, 1996)→文献の概要(English only)
| D−5 毎日食べる食品に用いられる遺伝子組換え食品は、高い安全性を確保する必要がありますが、長期の毒性試験(慢性毒性試験)を行っていないのはなぜですか。 |
| D−6 作物中に新たな有害物質が作られることはありませんか。 |
| D−7 作物に含まれる既存の有害物質の量が増えることはありませんか。 |
| D−8 害虫抵抗性の遺伝子組換え食品には、害虫を殺す蛋白質が入っていると聞きましたが、ヒトが食べても問題はないのですか。 |
| D−9 英国で遺伝子組換えのジャガイモをラットに食べさせたところ、免疫力の低下が見られたという報告(パズタイ博士の報告)があったそうですが、本当ですか。 |
| D−10 在来植物など、環境への影響はないのですか。 |
| D−11 抗生物質耐性マーカー遺伝子が入っている作物があると聞きましたが、挿入された遺伝子についてはどのようなことが評価されるのですか。 |
| (1) | 挿入遺伝子のクローニング若しくは合成方法に関する事項 挿入遺伝子のクローニング若しくは合成方法が明らかであること。 |
||||||||
| (2) | 塩基数および塩基配列と制限酵素による切断地図に関する事項 宿主に導入しようとするDNA断片について、塩基数および塩基配列が明らかであること。また切断地図が明らかにされ、制限酵素の名称、断片の数、サイズなどが明らかにされていること。 |
||||||||
| (3) | 挿入遺伝子の機能に関する事項 挿入遺伝子の機能及び挿入遺伝子から産生される遺伝子産物(RNA及びタンパク質)の性質、機能等が明らかであり、そのタンパク質が有害作用をもたないと判断できる合理的な理由があること。なお、挿入遺伝子の転写・翻訳の後、生成されるタンパク質が植物細胞内で切断・消化される場合には、それらの生成物に関しても上記が明らかであること。挿入遺伝子から産生されるタンパク質と既知の毒性タンパク質との構造相同性に関する検索方法及び検索結果が明らかにされており、原則として、構造相同性がないこと。仮に構造相同性がある場合は、安全性に問題がないと判断できる合理的な理由があること。 |
||||||||
| (4) | 抗生物質耐性マーカー遺伝子に関する事項
|
| D−12 大腸菌由来の遺伝子が用いられていると聞きましたが、病原性大腸菌O(オー)157のような病原性はないのですか。 |
| D−13 害虫抵抗性のBtトウモロコシの花粉で目的とする害虫以外の昆虫が死んだという報告があったそうですが、本当ですか。 |
| (1) | 報告概要 米国コーネル大学の研究者、ジョン・E・ロゼイらは、Btタンパク質を導入した害虫抵抗性トウモロコシが、チョウに被害を及ぼす恐れがある、との研究結果を発表しました(英国科学誌ネイチャー1999年5月20日号)。 この実験の内容は、トウモロコシの花粉を振りかけたガガイモ科の植物のトウワタの葉を、チョウ(オオカバマダラ)の幼虫に摂食させたところ、4日間で幼虫の44%が死亡し、生き残った幼虫も発育不全になったというものです。 |
||||||||||||||||
| (2) | 研究結果に対する農林水産省の検討と見解 農林水産技術会議の組換え体利用専門委員会で検討した結果、以下の結論が得られました。
|
||||||||||||||||
| (3) | 評価事項の概要
|
||||||||||||||||
| (4) | カルタへナ法に基づく審査 カルタヘナ法に基づき遺伝子組換え生物等を使用する者は、事前に第一種使用規程を定め、それについて農林水産大臣・環境大臣の承認を受ける必要があります。承認にあたっては学識経験者の意見を聞いた上で生物多様性影響を生ずるおそれがないことを確認します。これまでの指針に基づくBtトウモロコシの影響評価は科学的に行われていましたので、カルタへナ法の下でも同様の考え方で評価が行われることとなります。 |
| D−14 トリプトファン事件の経緯やその後の経過、原因(遺伝子組換えであったことによるものなのか)などについて教えてください。 |
| D−15 食品安全委員会が新しい安全性評価基準を決定しましたが、薬事・食品衛生審議会において審査された遺伝子組換え食品は見直す必要があるのですか。 |
| D−16 安全性未審査の遺伝子組換えじゃがいもが混入していたスナック菓子が発見されていますが、調査結果を教えて下さい。 |
| D−17 遺伝子組換え大豆を食べたラットから生まれたラットで死亡率の上昇や成長阻害が見られたという報告があると聞きましたが、その事実関係を教えてください。 |
| 1. | 齧歯類(ネズミの類)に生の大豆を大量に食べさせると有害な影響が出ることが一般的に知られていて、遺伝子組換え大豆であるか否かとは関係なく、この実験においては与えられた生の大豆がラットへ有害事象を生じさせ得る。 |
| 2. | 各グループの餌の間で構成された栄養素、栄養量などが等価であったかの情報がない。 |
| 3. | 各ラットにおける大豆の消費量や従来型の餌の消費量のデータがない。 |
| 4. | 死亡したラットの死因に関するデータがない。 |
| 5. | マイコトキシン(カビ類が産生する毒素の総称)等、混入物の存在を否定する情報がない。 |
| E−1 諸外国での規制の状況はどのようになっているのですか。 |
| E−2 EUでは新たな遺伝子組換え食品の承認を凍結していますが、なぜですか。 |
| F−1 安全性審査に用いた資料等については公開されているのです か。 |
| G−1 国は安全性確保のために、モニタリング検査(抜き取り検査)をすべきではないでしょうか。 |
| G−2 国として、安全性確保のためにどのような研究を行っているのですか。 |
・厚生科学研究成果データベース