| 審議会議事録等 | HOME |
| 日 時: | 平成10年 4月28日(火) 13:00~15:00 |
| 場 所: | 中央合同庁舎共用第6会議室 |
1 開会
2 生活衛生局長挨拶
3 委員紹介及び事務局紹介
4 資料確認
5 議 題
内分泌かく乱化学物質の健康影響に関する今後の検討課題の整理検討
6 閉会
| 氏 名 | 所 属 機 関 及 び 役 職 |
| 青 山 博 昭 | (財)残留農薬研究所水海道研究所毒性部毒性第2研究室水海道分室主任 |
| 阿 部 薫 | 国立がんセンター総長 |
| 井 口 泰 泉 | 横浜市立大学理学部教授 |
| 伊 東 信 行 | 名古屋市立大学学長 |
| 井 上 達 | 国立医薬品食品衛生研究所安全性生物試験研究センター毒性部長 |
| 岩 本 晃 明 | 聖マリアンナ医科大学泌尿器科教授 |
| 押 尾 茂 | 帝京大学医学部泌尿器科講師 |
| 黒 川 雄 二 | 国立医薬品食品衛生研究所安全性生物試験研究センター長 |
| 紫 芝 良 昌 | 虎ノ門病院副院長・分院院長 |
| 鈴 木 勝 士 | 日本獣医畜産大学教授 |
| 鈴 木 継 美 | 元国立環境研究所所長 |
| 髙 杉 暹 (たかすぎ のぼる) |
横浜市教育委員長(前横浜市立大学学長) |
| 高 田 勗 (たかた つとむ) |
中央労働災害防止協会労働衛生検査センター所長 |
| 武 谷 雄 二 | 東京大学医学部教授 |
| 田 中 勝 | 国立公衆衛生院廃棄物工学部長 |
| 津 金 昌 一 郎 | 国立がんセンター研究所支所臨床疫学研究部長 |
| 寺 尾 允 男 | 国立医薬品食品衛生研究所所長 |
| 寺 田 雅 昭 | 国立がんセンター研究所所長 |
| 西 原 力 | 大阪大学大学院薬学研究科教授 |
| 藤 原 房 子 | 商品科学研究所所長 |
| 真 柄 泰 基 | 北海道大学大学院教授 |
| 松 尾 昌 季 | (社)日本化学工業協会エンドクリン・ワーキンググループ委員 |
| 安 田 峯 生 | 広島大学医学部教授 |
| 山 崎 幹 夫 | 千葉大学名誉教授 |
| 和 田 正 江 | 主婦連合会副会長 |
| 資料1 | 内分泌かく乱化学物質の健康影響に関する検討会の開催について |
| 資料2 | エンドクリン問題について |
| 資料3 | 内分泌かく乱作用に関する報告書等について |
| 資料3ー1 | 平成8年度厚生科学研究健康地球計画推進研究事業 「化学物質のクライスマネジメントに関する研究」総括研究報告書 主任研究者 瀬高守夫(帝京大学薬学部教授) |
| 資料3ー2 | 外因性内分泌かく乱化学物質問題に関する研究班(環境庁)の中間報告 |
| 資料3ー3 | 内分泌系に作用する化学物質に関する調査研究結果(通産省による(社)日本化学工業協会への委託調査) |
| 資料4 | 内分泌かく乱化学物質に関する国際機関の最近の動き |
| 資料4ー1 | OECDエンドクリンWGの公表資料(平成10年3月) |
| 資料5 | 内分泌かく乱化学物質に関する米国の動き |
| 資料5ー1 | 環境内分泌かく乱作用に関する特別報告:影響の評価と分析 (平成9年2月、米国環境保護庁)(抜粋) |
| 資料5ー2 | 内分泌かく乱化学物質のスクリーニングと検査の方法に関する諮問委員会の報告書案(平成10年3月)(抜粋) |
| 参考1 | 食品衛生調査会毒性・器具容器包装合同部会(平成10年3月13日開催)の資料 |
| 参考2 | 食品衛生調査会毒性・器具容器包装合同部会(平成10年3月13日開催)の議事録 |
(注)資料3ー1、3ー2及び3ー3、資料4ー1、資料5ー1及び5ー2、参考1及び2については添付を省略。
なお、資料3ー1、3ー2及び3ー3、資料4ー1、資料5ー1及び5ー2については厚生省行政相談室(3階)にて、参考1及び2については厚生省ホームページ(http://www.mhw.go.jp)にて入手可能です。
| 資料1 |
平成10年4月
1 開催の趣旨
一部の有機塩素系農薬、プラスチック容器の可塑剤、洗浄剤の界面活性剤等が内分泌かく乱作用を有する旨指摘されており、これら物質による人の健康への影響の懸念が指摘されている。本件については、人の健康への影響の有無、種類、程度等が未解明であり、国際的にその調査研究が進められている。
このような現状を踏まえ、これら化学物質の食品、水、大気等を介した暴露による健康影響の懸念に適切に対処するため、国際的な動向も踏まえ、今後の検討課題の整理、個別物質の具体的な調査検討等総合的な検討を行うことが必要である。
このため、生活衛生局長の私的検討会として、「内分泌かく乱化学物質の健康影響に関する検討会」を開催し、総合的、効率的な検討を行うこととする。
なお、検討の結果については、食品衛生調査会、生活環境審議会等関係の審議会に報告し、必要な措置を講じることとする。
2 検討課題
(1)今後の検討課題の整理検討
3 検討会の議事及び公開
4 その他
| 資料2 |
1.「エンドクリン問題」とは
化学物質の中には、生体内にとりこまれて内分泌機能(ホルモン機能)を中心に広範な影響を及ぼすものがあり、これがヒトをはじめとする生態系に深刻な影響を与えている可能性があると報告されている。この一連の議論が「エンドクリン問題」と言われている。
この問題は、これらの化学物質のヒトへの健康や生態系への影響について啓蒙的に著された「奪われし未来」の発刊により、多くの反響を呼んでいる。
なお、これらの化学物質は、環境ホルモン様物質、内分泌攪乱化学物質等と総称されているが、その明確な定
義は現時点では確立されていない。
| (注) | 「奪われし未来」(Our Stolen Future)の概要 内分泌機能等の影響が指摘されている化学物質について、ヒトの健康影響(女性の乳がん、男性の睾丸腫瘍の発生増加、精子数減少等)や野生生物への影響(ワニの生殖器奇形、鳥類の生殖行動異常等)の可能性を指摘。 |
2.内分泌攪乱化学物質と指摘されている化学物質
内分泌攪乱化学物質とそのヒトに対する影響は、現時点では明らかになっていないが、内分泌攪乱化学物質に相当するとの可能性が指摘されている化学物質の例として、以下のものがある。
| ・一部の農薬 ・一部の工業化学物質 ・その他 |
… … … |
DDT等 プラスチック可塑剤の一部、PCB等 ダイオキシン等 |
3.世界における最近の主な取組
| 1996年11月 | OECD(経済協力開発機構)において、エンドクリン問題を取り上げ、試験法の検討を開始 |
| 1996年12月 | 英国においてOECD主催により、エンドクリン問題のヒトへの健康及び野生生物への影響に関するワークショップが開催 |
| 1997年 1月 | 米国EPA等が世界各国から専門家を招き、エンドクリン問題に関するワークショップを開催 |
| 1997年 2月 | IFCS(化学物質安全性政府間フォーラム)において、緊急的課題として、国際的に取り組んでいくことを議論 |
| 1997年 5月 | G7環境大臣会合において「子供の環境保健」のテーマの中で、エンドクリン問題が取り上げられ、宣言書の中にも、これをふまえた記述あり。 |
| 1997年12月 | OECDナショナル・コーディネーター会合において試験方法等を検討。 専門のWGを設立し、議論していくことが決定。 |
| 1998年 3月 | OECD/IPCS(国際化学物質安全計画)合同会合において、関係する調査研究成績の収集及びその評価を2年間を目途に行うことに合意 |
| 1998年 3月 | OECD内分泌かく乱物質ワーキンググループ会合において、試験方法等について検討を開始。 |
4.我が国における主な取組
| 1996年 7月 | 通商産業省において、化学品業界への委託研究の形で、業所管の観点から本問題を検討。翌年3月に報告書をとりまとめ、公表。 |
| 1996年10月 | 厚生省において、平成8年度厚生科学研究班において、人体影響の観点から本問題を取り上げ、現状を把握。翌年3月に報告書をとりまとめ。 |
| 1997年 1月 | 環境庁、厚生省、通商産業省、農林水産省、労働省による情報連絡会を設けた。 |
| 1997年 3月 | 環境庁において研究班を発足させ、環境保全の観点から、本問題を検討。7月に中間報告書をとりまとめ、公表。 |
| 1997年10月 | 厚生省において、平成9年度厚生科学研究班を発足。8年度研究の結果、今後実施していく必要があるとされたメカニズム解明、男性精子数の測定等を進めていくこととされた。 |
| 1998年 3月 | 食品衛生調査会毒性・器具容器包装部会において、ポリカーボネート樹脂等の安全性について審議検討。 |
1.平成8・9年度
(1)化学物質のクライシスマネジメントに関する研究
| 研究概要: | 内分泌攪乱物質のヒトや生態系に与える影響等に関して、既存知見を中心に検討。 |
| 主任研究者: | 帝京大学教授 瀬高 守夫 |
| 研究期間: | 平成8年度(本研究成果を踏まえ、(2)の研究に着手) |
| 予 算: | 275万円 |
(2)内分泌攪乱化学物質に関する研究
| 研究概要: | 内分泌攪乱物質のヒトへの健康影響(作用メカニズム、健常男子の 精子数測定等)に関する研究 |
| 主任研究者: | 国立医薬品食品衛生研究所毒性部長 井上 達 |
| 研究期間: | 平成9年度 |
| 予 算: | 925万円 |
(3)農薬、食品添加物等のエストロジェン様作用等の検出と評価に関する研究(食品規制国際ハーモナイゼーション促進研究費の一課題)
| 研究概要: | エストロジェン様作用物質検出系の作製と評価方法の検討 | |
| 主任研究者: | 国立医薬品食品衛生研究所毒性部長 国立医薬品食品衛生研究所毒性部第二室 |
井上 達(平成8年度) 金子 豊蔵(平成9年度) |
| 研究期間: | 平成8年度及び9年度 | |
| 予 算: | 454万円(平成8年度)、694万円(平成9年度) | |
2.今後の研究課題
平成10年度においては、厚生科学研究費補助金の生活安全総合研究費(14億9865万円)の一部として予算案が決定されたところであり、内分泌攪乱物質については、およそ平成14年度までを目途に、ヒトへの健康影響に係る調査研究(健康影響調査、作用メカニズム解明、試験方法や評価方法の検討等)を推進していく予定。平成10年4月15日に公募する旨を告示。
| 資料3 |
○ 平成8年厚生科学研究健康地球計画推進事業「化学物質のクライスマネジメントに関する研究」総括研究報告書 主任研究者瀬高守夫(帝京大学薬学部 教授)(資料3-1)
内分泌かく乱作用のうち、エストロゲン様作用を中心に、欧米における検討状況と知見の把握、環境エストロゲン様物質と指摘されている30数種の化学物質に関する文献調査を行うとともに、今後の研究課題を整理している。
○ 外因性内分泌かく乱化学物質問題に関する研究班(環境庁)の中間報告(資料3-2)
内分泌かく乱化学物質問題のこれまでの報告、内分泌かく乱を生じるメカニズム、国際的取組の状況、現時点における内分泌かく乱化学物質問題の考え方をとりまとめるとともに、これまでに得られている知見からは、一般生活において内分泌かく乱化学物質が人に影響しているか否かを判断することは困難であるという立場に立って、今後の課題について整理報告している。
○ 内分泌系に作用する化学物質に関する調査研究結果(通産省による(社)日本化学工業会への委託調査)(資料3-3)
諸外国の取組状況等の情報収集、因果関係の解析等の技術的課題の検討、今後の対応案についての調査研究の委託に対する報告書である。専門的な検討(社)日本化学物質安全・情報センターで実施され、11種類の化学物質について、体内における各種ホルモンレセプターへの作用、哺乳動物体内での代謝・分解、発がん性、生殖・発生毒性、野外生態系に及ぼす影響等につき、内外の公表文献が具体的にまとめられている。
| 資 料 4 |
1.日時等
| 日時: | 1998年3月16~18日 |
| 主催: | 国際化学物質安全計画(IPCS)、経済開発協力機構(OECD) |
| 場所: | ワシントン(米国) |
2.背景と目的
1997年2月に開催された第2回化学物質の安全性に関する政府間会合(IFCS)において、内分泌かく乱化学物質による人及び生態系への影響に関して懸念が示された。また、世界保健機構(WHO)、国際労働機構(ILO)及び国連環境計画(UNEP)が参加して構成されている国際化学物質安全計画(IPCS)や経済開発協力機構(OECD)等に国際的な調整や試験法の開発を推進するよう勧告がなされた。
本会議は、上記の勧告を踏まえ、国際的な取組の調整を図るとともに、内分泌かく乱化学物質に関する研究状況の情報収集とその評価を行うことを目的としている。
具体的には、日、米、英、加、蘭等12名の専門家からなるステアリンググループが設けられている。日本からは、井上国立医薬品食品衛生研究所毒性部長がステアリンググループの委員として参加。
3.議事の概要
(1) 内分泌かく乱化学物質による潜在的な人や生態系への影響に係る現在行われている研究活動について、関係諸外国間において、相互に情報交換可能な体制を整備する。
(2) 内分泌かく乱化学物質に関する研究状況について、国際的な観点から評価するため、内分泌かく乱化学物質の人や生態系への影響に関する広範な研究をレビューし、要 約し、報告書を作成する。具体的には、2年程度を目途に、WHOの出版物として刊行することとし、その体制を早急に整備する。
4. 今後の予定
| 1998. 9: | 各国から進行中の研究計画の提出。 |
| 1999. 1: | 収集された情報の効率や効果を評価。不足データの把握。 |
| 1999.秋: | ステアリンググループが収集された情報や広範な研究の状況の評価を実施。 |
| 2000.春: | 報告書の公表 |
II.OECD内分泌かく乱化学物質検査及び評価ワーキンググループ(EDTA)会合
1. 日時等
| 日時: | 1998年3月10日、11日 |
| 主催: | OECD |
| 場所: | パリ(フランンス) |
2. 背景
OECD加盟国の多くは、内分泌かく乱化学物質についての調査・研究を推進している。
本ワーキンググループは、この問題についての加盟国のこれらの活動を調整し、内分泌かく乱化学物質の試験方法及びその評価方法を開発するために新しく設けられた。
我が国から、青山(財)残留農薬研究所主任、井口横浜市立大学教授、井上国立医薬品食品衛生研究所毒性部長、松尾(社)日本化学工業協会委員が参加。
3.議事の概要
(1) 内分泌かく乱化学物質の試験方法及びその評価の方法を開発するため、次の3点からなる基本的なフレームワークについて合意。
(2) 上記のフレームワークの各段階におけるエンドポイント(評価項目)の検討につ いて同意。また、試験法の開発の必要性及び既存のOECDテストガイドラインプログラムの強化に言及。
(3) 加盟各国及び国際的な業界団体が協力して、広範なバリデーション(検証)の計画を進めることに同意。
4.今後の予定
今秋にEDTAの次回会合を開催する。
| 資料5 |
1. 目 的
内分泌かく乱化学物質による人や生態系への影響等に関する科学的な報告をまとめるとともに、その暫定的な評価と分析等を行うことを目的としている。
(注:内分泌かく乱物質のより広範にわたる探求が米国学士院(NAS)で行われており、本報告はこれが完了するまでの暫定的な評価と分析のための資料として利用できる。)
2. 人の健康への影響
(1)女性生殖系、男性生殖系等への影響
(1)女性生殖系への影響
様々な化学物質が実験動物と人で、女性生殖機能を一生を通してかく乱することが示された(例:ジエチルスチルベストロール(DES))。これらの影響には、正常な性分化、卵巣機能(すなわち、卵胞成長、排卵、黄体形成およびその維持)、受精、着床および妊娠のかく乱等がある。成人では機能する多くのフィードバックメカニズムがなく、成人より低い用量で有害影響が示されることがありうるため、特に発生途中の暴露による健康影響が懸念される。
具体的に懸念される主な影響は次のとおり。
・ 少数例の赤毛ザルを用いた研究では、ダイオキシン暴露と子宮内膜症との関連が示唆されている。
・ 小規模のパイロットスタディでは、人の血清中ハロゲン化芳香族炭化水素(ダイオキシン等)の濃度と子宮内膜症の程度との間に相関関係は認められていない。
有機塩素系のある種の農薬、多環芳香族炭化水素の暴露が乳腺新生物の発症因子となっているとする仮説については、この仮説を証明する十分な証拠はない。
(2)男性生殖系への影響
齧歯類において、エストロゲン作用をもち、アンドロゲンレベルを低下させ、あるいは発生の間にアンドロゲン作用を妨害する化学物質の暴露により、精子生成能力が低下し、生殖管異常等の雄性生殖系の異常が引き起こされているという証拠がある。
人においては、DESに子宮内暴露した男性の観察から、外因性エストロゲンの発生中の生殖系かく乱作用は、齧歯類と比較して弱いことが実証されている。また、DES暴露集団における男性生殖系癌の発生率の増加は見られていない。
具体的に懸念される主な影響は以下のとおり。
過去50年にわたり人の精子生成量が減少したという説について論争が続いている。
人での精巣癌がデータ的に確かに増加していることや、他の信頼できそうな健康影響が明らかに発生していることから、この有害影響があったという考え、あるいは今でも続いているとう考え方は支持される。人でのこれらの影響が、環境中に排出されている化学物質の内分泌かく乱作用に起因すると考えられるかどうかは現時点で不明であり、原因の研究が必要とされる。
疫学調査において、除草剤が散布された土地と前立腺癌死との間に弱いが統計的に有意な関連が示唆されている。また、コークス炉従業員の職業調査では、前立腺癌による有意な死亡とコークス炉放出の関連が報告されている。しかしながら、除草剤または多環芳香族炭化水素の暴露が人前立腺癌の増加に寄与しているのか、そのメカニズムが内分泌かく乱によるものかどうかはまだ確認されていない。
(3)視床下部と下垂体への影響
発生中や成熟後の神経内分泌機能が、内分泌かく乱物質によって被害を受ける可能性がある。特に発生中の暴露は懸念される。
(4)甲状腺への影響
数多くの化学物質(例えば、尿素誘導体、ポリハロゲン化ビフェニル、塩化ジベンゾ-p-ダイオキシン)が、甲状腺ホルモンレベルを変えることが見いだされている。
(2)データの評価
人における発生、生殖への影響および癌の発生率の増加が内分泌かく乱作用をもつ環境中に排出された化学物質に起因するという作業仮説は、水生・野生生物種において類似の影響が観察されることから支持される(人と野生生物の両方の報告に共通のテーマとなっている)。
他方、この仮説は以下の事実によって問題となっている。
(1) ホルモンの分泌と排泄は体内で高度に調節され、ホルモンの適度な変動をコントロールするメカニズムは、ホルモン濃度の負のフィードバック制御によって適切になされている。そのため、食事からの吸収と、肝臓解毒後の環境ホルモンの小さな増加は、内分泌の恒常性をかく乱するに至らないと考えられる。
(2) 外因性化学物質のレセプターに対する結合親和性が低く、環境中濃度が低いことは、成体で有害反応を引き起こすにはおそらく不十分と考えられる。胎児と子供が内分泌環境に対する小さな変化を調節する能力があるかどうかは確かでない。
(3) 内分泌機能に影響を与える可能性がある化学物質の混合物でのデータは現時点では利用できない。同時に環境エストロゲンの場合、環境中の抗エストロゲンとの拮抗作用により、エストロゲン作用が弱まる可能性があることが知られている。
(3)結論
わずかな例外はあるが(例えば、DES)、内分泌かく乱メカニズムによって作用する人への有害影響と、特定の環境中に排出された化学物質との因果関係は確立されていない。
しかし、ある種の残留性化学物質が、内分泌かく乱作用によって生殖、発生への影響及び発癌の原因となっているという懸念を考慮し、新たに調査・研究を行う必要がある。
4. 生態学的な影響
多くの報告は、様々な化学物質が無脊椎動物、魚類および野生生物で内分泌系を変化させ、生殖と発生に影響を与えうることを示しているが、生体レベルでこれらの障害から、どの程度の有害な集団としての反応が生じたか、または生じ得たかを確立した例はほとんどない。
これまでに内分泌かく乱化学物質への暴露の結果として、著しい個体減少を示した信頼できる例は、中央フロリダのアリゲーターと、いくつかの海洋無脊椎動物種の局地集団について報告されたものである。
II.内分泌かく乱化学物質のスクリーニングと検査の方法に関する諮問委員会の報告書(案)
(平成10年3月)の概要
1.背景と目的
最近の多くの研究はある種の化学物質が人や野生生物の内分泌系などに悪影響を与えていることを示唆している。また、内分泌かく乱化学物質は発生、行動や生殖などに様々な問題を引き起こす可能性がある。
このような状況を踏まえ、アメリカでは1996年8月に食品品質保護法(FQPA)及び安全飲料水法(SDWA)が制定された。両法は、環境防護庁(EPA)が、
「適切に評価された試験系やその他の明らかな情報を利用し、ある物質が指摘されているような自然に存在するエストロゲンや他の内分泌効果によって生じる効果と類似した効果を持つかどうかを確認するため、スクリーニングプログラムを開発すること」
などを定めている。さらに、1999年8月にそのプログラムを実施し、2000年8月に議会にその報告をするよう求めている。
EPAは、これを踏まえ、これらの法案が審議中であった1996年5月にEDSTAC(Endocrine disruptor screening and testing advisory committee)を設置し、内分泌かく乱化学物質のスクリーニング及びテストプログラムの策定について助言を求めることとした。
EDSTACは39名の関係団体の代表者や専門家からなり、その下に4つの作業グループ(the Principle Work Group, the Priority Setting Work Group, the Screening and Testing Work Group and Outreach Work Group)が設置されている。
なお、本報告書(案)は平成10年3月に公表されたもの(インターネット http://www.epa.gov/opptintr/opptendo/whatsnew.htm により入手可能)。本案は、(1)紹介、(2)背景、(3)基本的考え方、(4)優先順位付け、(5)スクリーニングと検査の実施方法の提案、(6)コミュニケーション問題、(7)本計画実施のタイムテーブルに関係する主な事項の7章からなっている。
2. 米国の取組の経過
| 1995. 4: | EPA-first workshop(生態系保全のための戦略と研究)の開催 |
| 1995. 6: | EPA-second workshop(生態影響)の開催 |
| 1996. 5: | EDSTACの設置 |
| 1996. 8: | 食品品質保護法(FQPA)及び安全飲料水法(SDWA)の制定 |
| 1997. 2: | EPAが「環境内分泌かく乱作用に関する特別報告」を公表 |
3.定義(案)について
(1)“endocrine disruptor”
an exogenous chemical substance or mixture that alters the function(s) of the endocrine system and thereby causes adverse effects to an organism, its progeny, or (sub) populations.
(仮訳)
内分泌系の機能に変化を与え、それによって個体やその子孫あるいは集団(一部の亜集団)に有害な影響を引き起こす外因性の化学物質又は混合物
(2)“potential endocrine disruptor”
an exogenous chemical substances or mixture that alters endocrine system function(s) and may affect an organism , its progeny , or (sub)populations.
(仮訳)
内分泌系の機能に変化を与え、個体やその子孫あるいは集団(一部の亜集団)に影響を与える可能性のある外因性の化学物質又は混合物
4. スクリーニング及び検査計画案の概要(別紙参照)
(1)ハイスループット事前スクリーニング(High throughput pre-screening, HTPS)について
HTPSの目的は、比較的短期間に、多くの化学物質について、予備的な生物活性情報を得ることである。この情報は、(1)潜在的な内分泌かく乱物質の検出、(2)T1S(第1段階のスクリーニング)の対象となる品目の優先順位付けに有用である。具体的には、エストロゲン、アンドロゲン、甲状腺ホルモンのレセプター(受容体)に対する作用を検出するため、転写活性と(/または)レセプター結合親和性を指標とした試験管内の試験(in vitro assay)をハイスループット(自動化された分析装置)を用いて実施することが提案されている。なお、年間10,000ポンド(4.5トンに相当)(以上製造されている物質(約15,000物質)を対象に事前スクリーニングを行うことが提案されている。
(2)Tier 1 Screening(第1段階のスクリーニング、T1S)について
T1Sの目的は、内分泌かく乱作用を有する可能性のある物質であるか否かを分類するために必要な最小、かつ、十分なデータを得ることである。T1Sは、エストロゲン、アンドロゲン、甲状腺ホルモンに関連する作用を強める/模倣する/抑制する影響を検出するようにデザインされた一連の試験からなる。なお、これらの試験系で陽性と評価された物質はより高いプライオリティで引き続く試験(第2段階の試験、T2T)が行われることとなる。
T1Sの具体的な提案は次のとおりである。
(in vitro、試験管内)
(in vivo screens)
(3) Tier2Testing(第2段階の試験、T2T)について
T2Tの目的は、人と野生生物における内分泌かく乱の性質、可能性、用量-反応関係を性格付けることである。化学物質が内分泌かく乱化学物質であるかどうかを決定するとともに、その作用が直接か間接かを検討する。また、人及び野生生物に対するハザードアセスメント(危害分析)を行う上で有用な情報を得る。
陽性と評価された場合には、その物質についての危害分析が行われる。また、最終的な評価のため、必要に応じ、追加的な試験が求められる。
T2Tの具体的な提案は以下のとおりである。
(testing)
(4)危害分析について
(5)個々の化学物質のスクリーニング等の実施方法
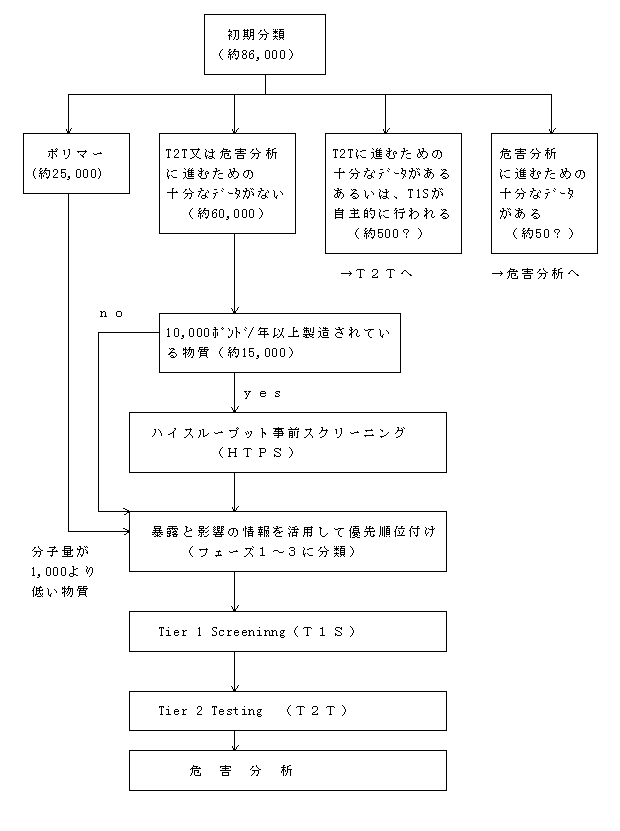
TSCA(Toxic Substances Control Act、毒性物質規制法)に登録されている約86,000物質を既存の情報をもとに以下の4つに分類した上、HTPS、T1S、T2T、危害分析を実施することが提案されている。
当面、分子量が1,000より低い物質について、暴露と影響の情報を活用して優先順位付けを行い、優先順位の高い物質から、順次、T1S、T2T、危害分析を行う。
年間10,000ポンド以上製造されている物質については、HTPSを行う。この結果を踏まえ、暴露と影響の情報を活用して優先順位付けを行い、優先順位の高い物質から、順次、 T1S、T2T、危害分析を行う。
データ、T1Sの結果を踏まえ、T2T,危害分析を行う。
危害分析を行う。
(1) EDSATCの最終報告書の公表 1998年8月
(2) HTPS
| ア 実施可能性の研究 イ 試料の収集 ウ HTPSの実施 |
1998年2月~7月 1998年7月~99年2月 1999年2月~4月 |
| ア | 食品品質保護法、安全飲料水法に基づく提案 | 1998年8月 |
| イ | HTPSの試験結果、T1S及びT2Tの優先順位 付け案等の公表 |
1999年11月 |
| ウ | T1S及びT2Tの検査結果等の公表 | 2000年11月 |
| エ | TSCA規制案等の公表 | 2002年第2四半期 |
| オ | TSCA規制の制定 | 2003年第3四半期 |
(4) T1S及びT2T
| ア | T1S及びT2Tの標準化及び検証 | 1998年8月~2000年7月 |
| イ | T1Sの第1相 | 2000年11月~2001年11月 |
| ウ | T1Sの第2相 | 2002年第3四半期以降 |
| エ | T2Tの第1相 | 2000年11月~2002年第2四半期 |
| オ | T2Tの第2相 | 2003年第1四半期以降 |

1. Tier 1 Screening(第1段階のスクリーニング、T1S)
(in vitro,試験管内)
(1) ER binding assay(エストロゲン受容体結合試験)
培養細胞等よりエストロゲンレセプター分子を調整し、そこに、一定濃度のラジオアイソトープ標識エストラジオールと、種々の濃度の被験物質を作用させる。未結合のエストラジオールと被験物質を取り除き、レセプター分子を回収し、その放射活性を測定する。これにより、如何なる濃度の被験物質によりエストラジオールがレセプター分子から排除されたか、すなわち結合の相対的な強度が計算される。
(1)’ER transcriptioal activation assay(エストロゲン転写活性試験)
エストロゲンレセプター分子とその応答遺伝子(酵素等をコードする)を細胞内に用意し、エストロゲンレセプター分子にホルモン作用のある物質が結合した際に転写がおこり、酵素等が合成される。その酵素活性等を測定し、遺伝子発現(転写)の程度を知ることが出来る。
(2) AR binding assay(アンドロゲン受容体結合試験)
培養細胞等よりアンドロゲンレセプター分子を調整し、そこに、一定濃度のラジオアイソトープ標識アンドロゲンと、種々の濃度の被験物質を作用させる。未結合のアンドロゲンと被験物質を取り除き、レセプター分子を回収し、その放射活性を測定する。これにより、如何なる濃度の被験物質によりアンドロゲンがレセプター分子から排除されたか、すなわち結合の相対的な強度が計算される。
(2)’AR transcriptioal activation assay(アンドロゲン転写活性試験)
アンドロゲンレセプター分子とその応答遺伝子(酵素等をコードする)を細胞内に用意 し、アンドロゲンレセプター分子にホルモン作用のある物質が結合した際に転写がおこり、酵素等が合成される。その酵素活性等を測定し、遺伝子発現(転写)の程度を知ることが出来る。
(3) Steroidgenesis assay with miced testis(精巣ミンチステロイド合成試験)
精巣をミンチし、培養系に移し、そのステロイド合成酵素(P450)の活性を評価する。
(in vivo screens,生体内)
(1)Rodent 3-day uterotrophic assay(齧歯類3日間子宮肥大試験)
卵巣摘出あるいは未熟ラットあるいはマウスに3日間、被験物質を投与し子宮重量の増加等から、そのホルモン作用を評価する。
(2) Rodent 20-day pubertal female assay(齧歯類20日間思春期雌試験)
21日齢の雌ラットに毎日(7日/週)被験物質を投与し、全例の膣開口が確認されるまで投与し続ける。膣開口の早晩で、agonist・antagonistを含め、ホルモン作用を評価し、合わせて、甲状腺などの種々の血清ホルモン値なども測定し、評価を行う。
(3) Rodent 5-7day Hershberger assay(齧歯類5-7日間Hershberger試験)
去勢雄ラットに、被験物質、あるいは、被験物質+テストステロンを5~7日間投与し、前立腺・精嚢腺などの副生殖器の重量などを測定し、アンドロゲン効果および抗アンドロゲン効果を評価する。
(4) Frog metamorphosis assay(蛙変態試験)
オタマジャクシの尾の吸収に甲状腺ホルモンが必要であることを利用した方法。オタマジャクシ期のアフリカツメガエルに被験物質を14日間暴露し、尾の吸収の遅・速をもって、甲状腺ホルモン効果および抗甲状腺ホルモン効果を評価する。
(5) Fish gonadal recrudesence assay(魚類生殖性復帰試験)
冬期を模倣した(短日照・低温)状態において魚の性腺や2次性徴が退縮し、日照時間を延長し、温度を上昇させると性腺や2次性徴が再び成長することを利用し、その際に投与した被験物質がそれらに及ぼす影響を評価する。
2. Tier 2 Testing (第2段階の試験、T2T)
(1) Mammalian reproductive toxicity study(ほ乳類をもちいた生殖毒性試験)
bobwhite quail(うずら)とmallard(まがも)を用いた生殖毒性試験。
(3) Fish life cycle (魚類ライフサイクル試験)
Fathead minnow(はや)を300日間にわたり被験物質に暴露する。
(4) Mysid life cycle(アミ類を用いた毒性試験)
(5) Amphibian development and reproduction(両生類発生生殖試験)
蛙のオタマジャクシに暴露した際の影響をみる。
照会先 生活衛生局 食品化学課 TEL:3595-2341
| 審議会議事録等 | HOME |