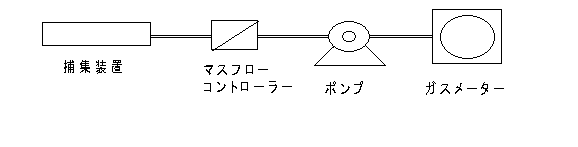
図1 試料採取装置
| 報道発表資料 | HOME |
平成12年12月22日
平成12年12月15日、第5回シックハウス(室内空気汚染)問題に関する検討会(座長:林 裕造 前北里大学客員教授)が開催され、別紙の通り、中間報告書-第4回~第5回のまとめが、とりまとめられた。
当中間報告書は以下の内容を含む。
|
中間報告書の主な内容
1. 個別の揮発性有機化合物(VOC)の指針値等について
2. 総揮発性有機化合物(TVOC)の空気質指針値策定の考え方について
3. 室内空気質指針値の適用範囲の在り方について
4. 室内空気中化学物質に関する機器等目録について
5. 測定・相談マニュアルの基本方針について
6. 次回以降予定する本検討会の課題
|
照 会 先 厚生省生活衛生局企画課 生活化学安全対策室 室 長 川原 章(内2421) 担 当 吉田 淳(内2423) 剣持 和弘(内2423) 平野 英之(内2424) 電 話 [現在ご利用いただけません]
平成12年12月15日
1. 個別の揮発性有機化合物(VOC)の指針値等について
今般、室内空気汚染に係るガイドラインとして、新たにエチルベンゼン、スチレン、クロルピリホス、フタル酸ジ-n-ブチルの室内濃度に関する指針値等をとりまとめたので、下記に概要を示す。
(1)室内濃度に関する指針値の概要(別添1)
ここに示した指針値は、現状において入手可能な科学的知見に基づき、人がその化学物質の示された濃度以下の暴露を一生涯受けたとしても、健康への有害な影響を受けないであろうとの判断により設定された値である。これらは、今後集積される新たな知見や、それらに基づく国際的な評価作業の進捗に伴い、将来必要があれば変更され得るものである。
今回指針値を策定した4物質(エチルベンゼン、スチレン、クロルピリホス、フタル酸ジ-n-ブチル)は、平成12年6月26日付本検討会中間報告書-第1回~第3回のまとめの3.指針値策定の今後の方針に基づいて選定されたものである。
これら物質の指針値は、いづれも長期間の暴露によって起こる毒性を指標として策定している。
指針値の策定によって、室内空気汚染の低減化が促進され、快適で健康な室内空間が確保されることを期待する。
| 揮発性有機化合物 | 毒性指標 | 室内濃度指針値* |
| ホルムアルデヒド | ヒト暴露における鼻咽頭粘膜への刺激 | 100μg/m3 (0.08ppm) |
| トルエン | ヒト暴露における神経行動機能及び生殖発生への影響 | 260μg/m3 (0.07ppm) |
| キシレン | 妊娠ラット暴露における出生児の中枢神経系発達への影響 | 870μg/m3 (0.20ppm) |
| パラジクロロベンゼン | ビーグル犬暴露における肝臓及び腎臓等への影響 | 240μg/ m3 (0.04ppm) |
| エチルベンゼン | マウス及びラット暴露における肝臓及び腎臓への影響 | 3800μg/ m3 (0.88ppm) |
| スチレン | ラット暴露における脳や肝臓への影響 | 220μg/ m3 (0.05ppm) |
| クロルピリホス | 母ラット暴露における新生児の神経発達への影響及び新生児脳への形態学的影響 | 1μg/ m3 (0.07ppb) 但し、小児の場合は、0.1μg/ m3 (0.007ppb) |
| フタル酸ジ-n-ブチル | 母ラット暴露における新生児の生殖器の構造異常等の影響 | 220μg/ m3 (0.02ppm) |
(2)採取方法と測定方法について(別添2)
2.総揮発性有機化合物(TVOC)の空気質指針値策定の考え方について(別添3)
(1) 室内空気質TVOC(暫定目標値)
個別VOC指針値とTVOC暫定目標値について
個別VOC指針値はリスク評価に基づいた健康指針値であり、その濃度以下であれば通常の場合そのVOCは健康への悪影響は起さないと推定された値である。しかしその濃度以下であればその空気質が快適で安全ということでは決してなく、実際には複数のVOCsが存在することから、他のVOCについても順次健康指針値を決めていかなければならない。しかしそれには多大な時間を有すること、またその間に指針値を決めていない有害物質による汚染の進行を未然に防ぐ目的から、VOC全体としての空気中濃度の目安を示して、個別VOC指針値を補足することが重要であると判断した。その際、TVOCとしてのリスク評価を行うにはデータが不足していることから、国内における室内VOC濃度の実態調査の結果を用いて、合理的に達成可能な限り低い範囲において暫定目標値を決定した次第である。従って個別VOC指針値とTVOC暫定目標値は、現時点ではそれぞれ独立して扱われるべきものである。
将来リスク評価に基づくTVOC指針値が設定された場合には、個別VOC濃度とTVOC濃度の双方がそれぞれの指針値を満たしていないと、その空気質は安全であるとは言えない。従って、関係者においては、暫定目標値が将来指針値として設定し直されたときのことを今から念頭におくと同時に、その間、暫定目標値を室内空気質の状態をモニタリングする際の目安として、是非とも快適で安全な室内空間の確保を目指していっそうの努力をしていただきたい。
測定結果の評価方法について
この暫定目標値は、竣工後居住を開始してある程度時間が経過した状態における目安であって、竣工後入居してしばらくの間は、暫定目標値を超える場合も予測される。
またTVOCに含まれる物質の全てに健康影響が懸念される訳ではないこと、またその中には日常の居住環境で用いられる発生源に由来する物質が含まれることに留意すべきである。
従って、測定されたTVOC値が暫定目標値を超える結果が得られた場合には、測定時期や、その中に含まれる物質の種類や由来を確認した上で、個々の良否の評価を行うべきである。例えば、天然材を用いた住宅のような場合は、特定の天然成分が高濃度で測定される可能性が高いことから、特別な配慮が必要であろう。
この点は、本検討会中間報告書(2000年6月26日)において、背景因子の異なる個々の測定値と指針値との関係について更なる検討を進めることの重要性に言及している通りである。
(2)採取方法及び測定方法について
詳細なTVOC測定手順を作成・公表するまでの間、現時点のスキームは、欧州委員会共同研究センター研究所「室内空気質とヒトへの影響報告書No.19:室内空気質の検討における総揮発性有機化合物(TVOC)(1997)にて勧告されたTVOC決定手順を参考にし、以下の通りとする。
3.室内空気質指針値の適用範囲の在り方について(別添4)
本検討会で策定される指針値は、生産的な生活に必須な特殊な発生源がない限り、あらゆる室内空間(下記)に適用されるべきである。特に弱者(小児、高齢者、妊婦、病人など)が暴露される可能性の高い空間においては、積極的な空気質管理が求められ、当事者による継続的なモニタリングによってその効果を高めていくべきである。
住居(戸建、集合住宅)、オフィスビル(事務所、販売店など)、病院・医療機関、学校・教育機関、幼稚園・保育園、養護施設、高齢者ケア施設、宿泊・保養施設、体育施設、図書館、飲食店、劇場・映画館、公衆浴場、役所、地下街、車両、その他
4.室内空気中化学物質に関する機器等目録について
室内空気の測定機器や方法につき、目的に応じた選択をする際の参考となるものとして、原理その他特徴を含めて現時点で利用可能な測定機器についての目録を作成した。
当該目録は、(財)ビル管理教育センターを通じて行った製品調査による企業からの回答を基に作成したものである。従って本検討会として検証を行ったものではないので、技術的な参考資料として、測定依頼者等関係者に利用していただきたい。
なお本目録については、測定機器の新開発や改良等に伴い、順次更新していくものとする。公表の仕方については、厚生省や(財)ビル管理教育センターのホームページ等において、また、別途作成中の測定・相談マニュアルに添付する等して行うものとする。
5.測定・相談マニュアルの基本方針について
6. 次回以降予定する本検討会の課題
(1) 室内濃度指針値策定の新たな対象物質
本検討会中間報告書-第1回~第3回のまとめ(平成12年6月26日)の「3.指針値策定の今後の方針について」に従い、個別の指針値策定の次の対象は、以下の通りとする。
(2) 測定分析方法に係る今後の課題
(3) シックハウス用語・略語集の整備
現在作成中の測定・相談マニュアル及び測定法目録と併せて、正しい知識の普及と相談専門家の養成のためのテキストとして、さらには行政当局や一般消費者にも便利に利用できるような、シックハウス問題関連用語・略語集の作成を行う。
(4) 空気質に関する情報開示と継続的なモニタリングのための体制
建材や家庭用品等の発生源を生産・供給する業者による情報開示、また継続的なモニタリング体制として、建物の生産者又は管理者が、自ら自主的に又は居住者等その室内空間で生活活動を営む者からの要求によって、定期的に空気質汚染のチェックを行いその情報を開示し、双方でモニタリングをしていくシステムが必要である。
そこで、例えば測定機関や室内空間の管理者又は居住者の協力を得て、シックハウス(室内空気汚染)問題に関する室内空気質モニター制度を設置して、定期的にデータを集計・公表し、室内環境評価に利用していくことを検討する。
1. エチルベンゼンについては、マウス及びラットにおける吸入暴露に関する知見から、肝臓及び腎臓に影響を及ぼさないと考えられる無作用量を基に、室内濃度指針値を3800μg/m3(0.88ppm)と設定した。
2. スチレンについては、ラットにおける吸入暴露に関する知見から、脳や肝臓に影響を及ぼすと考えられる最小毒性量を基に、室内濃度指針値を220μg/m3(0.05ppm)と設定した。
3. クロルピリホスについては、母動物が経口暴露された仔ラットの発育に関する知見から、神経発達に影響を及ぼすと考えられる最小毒性量を基に、吸入暴露に置き換えて、室内濃度指針値を1μg/m3(0.07ppb)と設定した。また特に新生児脳の形態学的変化に係る知見を考慮し、小児を対象とした指針値を0.1μg/m3(0.007ppb)と設定した。
4. フタル酸ジ-n-ブチルについては、母動物が経口暴露された仔ラットの発育に関する知見から、生殖器の構造異常等の影響を及ぼすと考えられる最小毒性量を基に、吸入暴露に置き換えて、室内濃度指針値を220μg/m3(0.02ppm)と設定した。
1.エチルベンゼンの室内濃度指針値案の策定
(1) 発がん性に関して、マウスとラットへの各吸入暴露実験において、雄マウスの肺腺腫の発生増加、雌マウスの肝腺腫の発生増加、また雄ラットの尿細管腺腫・癌腫の発生増加が報告されている。
(2) 工場でエチルベンゼンに暴露されている可能性のある作業者を対象にした2つの調査では、発がん率や発がんによる死亡率が特に増加したという知見は得られていない。
(3) 変異原性に関して、細菌、酵母、昆虫細胞では陰性であった。チャイニーズハムスター胚細胞では染色体異常を誘発せず、培養ヒトリンパ球でも非常に弱い陽性を示す程度であった。シリアンハムスター胚細胞では陽性であったものの、in vivoでは微小核を誘発しなかった。
(4) 以上のことから、エチルベンゼンの発がん性については、実験動物においては十分な証拠が認められるものの、遺伝毒性は多くの実験系において陰性であり、またヒトにおいては発がん性を示唆する証拠は得られていないことから、エチルベンゼンの指針値の策定には、その他の毒性指標を基に、耐容1日摂取量を算出して求める方法が適当と判断した。
(5) エチルベンゼンは、動物及びヒトに対し、中枢神経系に対する毒性並びに鼻粘膜や眼に対する刺激性を示す。これらは、ヒトへの単回暴露の場合、430~860mg/m3の濃度より現れる。
(6) Wistar系雌ラットにエチルベンゼン0、13.6、136、408及び680mg/kg/日を、週5日6ヶ月間、胃に強制経口投与した結果、408及び680mg/kg投与群にて、肝・腎重量の僅かな増加や一部の肝細胞の僅かな肥大等の変化が認められた。
(7) ラット(F-344/N)及びマウス(B6C3F1)に、エチルベンゼン0、430、1075、2150、3225及び4300mg/m3を、1日6時間、週5日、13週間、吸入暴露した結果、3225及び4300mg/m3投与群にて、マウスの雄雌において、用量相関性のある肝臓絶対重量の増加が見られた他、4300mg/m3では、雌マウスの腎臓相対重量の増加が観察された。雄ラットにおいては、3225及び4300mg/m3投与群にて、肝臓・腎臓の絶対及び相対重量の増加が見られた。雌ラットでは、2150、3225及び4300mg/m3投与群にて、肝臓・腎臓の絶対重量の増加が見られたが、相対重量の増加は観察されなかった。いづれの場合もエチルベンゼンに関係した組織学的変化は認められなかった。他の臨床化学検査にも異常は認められず、精子や膣粘膜上皮細胞にも変化は見られなかった。
(8) ラット(Wistar系)の妊娠1~19日まで、及びウサギ(ニュージーランド白)の妊娠1~24日まで、0、430及び4300mg/m3のエチルベンゼンを、1日6~7時間吸入暴露させた場合、ウサギでは、2用量群において対照群に比し有意に(p<0.05)生存胎児数が減少したが、胎児着床数、死亡及び吸収胚数には対照群との間に有意差はみられなかった。ラットでは、4300mg/m3投与群にて母動物の肝臓、腎臓及び膵臓重量の増加が見られ、また胎児において、2用量群とも有意な(p<0.05)肋骨数の増加が観察された。
(9) ラット(CFY)の妊娠7~15日まで600、1200及び2400mg/m3のエチルベンゼンを1日24時間連続暴露させた結果、2400mg/m3で骨格形成遅延、肋骨数の増加、胎児発育率の減少が見られた。ウサギ(ニュージーランド白)の妊娠7~20日まで500及び1000mg/m3のエチルベンゼンを連続暴露させた場合は、1000mg/m3で流産による胎児数の減少が観察された。ラット胚をエチルベンゼン含有キシレン下で培養した実験では、用量依存的な胚の成長阻害が認められたものの、催奇形成は認められなかった。
(10) 職業暴露に関する多くの疫学的調査が実施されているが、これらは、エチルベンゼンを含む溶媒混合物への暴露を調査しているため、観察された異常がエチルベンゼンに由来するものなのかどうかの特定は困難である。なお、エチルベンゼン生産工場の200人の作業者を対象にした20年間の健康医学調査が実施されているが、血液学的な異常は観察されていない。この際の、マンデル酸濃度から推定したエチルベンゼンの最大暴露濃度は86mg/m3、平均暴露濃度は8.6mg/m3であった。
(11) ヒト暴露データからは、(10)よりNOELが8.6~86mg/m3の間にあると推定されるが、このデータからは用量相関性が導けないため、指針値の推定に用いることは適切ではない。生物学的に意義のある毒性知見としては、(7)の動物試験において用量相関性のある毒性発現が認められており、リスク評価には、このデータから無作用量(NOEL)を決定して指針値を求めることが適当と判断した。肝臓重量の増加は、病理組織学的変化を伴っていないので、無毒性量(NOAEL)は4300mg/m3よりも高濃度に位置すると思われるが、無作用量(NOEL)となる2150mg/m3を指針値の計算に用いることとした。1日24時間及び週7日に平均化し、不確実係数100(種差10、個体間差10)を考慮すると、エチルベンゼンの室内濃度指針値=2150mg/m3×6/24×5/7×1/100 = 3.8mg/m3(=3800μg/m3;0.88ppm)と推定された。
(参考文献)
1. IPCS Environmental Health Criteria 186, ETHYLBENZENE, World Health Organisation, Geneva 1996
2. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, Vol 77, ETHYLBENZENE, World Health Organisation International Agency for Research on Cancer, Lyon 2000
3. NTP (1992) Toxicity studies of ethylbenzene in F344/N rats and B6C3F1 mice (inhalation studies), US Department of Health and Human Services, National Toxicology Programme, NIH Publication No.92 - 3129
2.スチレンの室内濃度指針値案の策定
(1) スチレンは代謝活性化されてエポキシド体となって変異原性を示す可能性が疑われるものの、細菌、酵母及びほ乳類細胞を用いた各種in vitro試験並びにほ乳動物を用いた各種in vivo試験の結果からは、むしろ変異原性を否定する結果が多く得られている。7,8-エポキシド体を直接作用させた場合においても、in vitro試験では多くの実験系で陽性であったものの、in vivo試験では変異原性を否定する結果が得られている。
(2) 発がん性に関して、スチレン1350mg/kg/日をO20系マウスに経口投与した場合、肺腫瘍の増加を誘発したことが報告されているが、Fischer344ラットでは、500、1000及び2000mg/kg/日の投与群で、腫瘍発生率に差が見られなかった。また7,8-エポキシド体をラットに経口投与した場合は、50及び250mg/kg/日を週4又は5日、52週の投与により、前胃の乳頭腫及び扁平上皮癌が観察され、また別の実験で、100~150mg/kg/日を120週、ラットに投与した場合、前胃癌及び肺腫瘍が誘発されたことが報告されている。
(3) 非常に高濃度のスチレンに暴露された強化プラスチック生産作業者において、末梢血リンパ球の染色体異常の増加が認められている以外は、暴露量の低いそれ以外のプラスチック生産作業者の事例も含め、ヒト遺伝子への明確な影響は認められていない。各調査とも交雑因子が多く、結果のバラツキが非常に大きく、用量相関性は見いだされていない。
(4) 発がん性に係る幾つかの疫学的調査では、スチレン含有ゴムを扱う作業者に白血病やリンパ腫が発生した等の報告が少数あるものの、因果関係は明かにされておらず、ヒトでのスチレン暴露と癌発生との関連性は否定されている。
(5) このように、スチレンの発がん性を示唆する証拠は、一部の動物実験に限定されており、ヒトでの発がん性や遺伝子障害性を示唆する証拠は得られていないことから、スチレンの指針値の策定には、その他の毒性指標を基に、耐容1日摂取量を算出して求めることが適当と判断した。
(6) 急性毒性に関して、ラットの経口LD50は5~8g/kg体重であった。またラットにスチレンを5460mg/m3の濃度より1~4時間単回吸入させた場合、鼻粘膜及び眼の刺激や中枢神経系の抑制が見られている。
(7) 亜急性及び慢性毒性に関して、ラットに1260mg/m3のスチレンを1日6時間、週5日、11週吸入させた場合、脳内軸策タンパク質の変化、腎臓及び肝臓の薬物代謝酵素誘導、肝臓の組織学的変化、肝臓等のグルタチオン量減少が認められている。420mg/m3のスチレンを投与した場合は、グルタチオン量の大きな減少は認められていない。
(8) 雌ラットに週5日6ヶ月間経口投与した試験では、肝・腎重量の増加のみが観察され、NOAELは133mg/kgであった。またビーグル犬に0、200、400及び600mg/kg/日のスチレンを19ヶ月間経口投与した試験では、400mg/kg投与群より、用量依存的に、赤血球内ハインツ小体の増加が認められ、NOAELは200mg/kgであった。
(9) 生殖発生毒性に関して、ラットの妊娠6~15日にスチレン180及び300mg/kg/日を投与しても胎児死亡率や妊娠率に変化は見られなかった。ラットの3世代試験は、2年間スチレン混入飲料水(7.7~21mg/kg/日)を投与して実施されたが、スチレン暴露と関係のある生殖発生の異常は認められなかった。一方、スチレン400mg/kg/日を60日間経口投与した雄ラットでは、精子数の減少や精細管の萎縮が認められ、雌よりも雄の生殖系がスチレン暴露の影響を受けやすいことが示唆された。マウスに1130及び1260mg/m3のスチレンを1日6時間、5日間吸入させても、精子頭の異常の頻度に差はみられなかった。
(10) スチレンのヒト短期暴露に関して、健常ボランティアによる複数の暴露実験が報告されている。これらを要約すると、0.2~0.34mg/m3から臭いによる不快感、420~840mg/m3を超えると鼻腔粘膜や眼の刺激性、及びめまい・頭痛などの中枢神経系の症状が起きる傾向がある。630~840mg/m3から反応時間や行動、平衡感覚への影響、さらに1470mg/m3を超えると、明かな中枢神経系の障害が起こりうる。
(11) また職域でのヒト長期暴露に関する各種疫学的調査成績を総合した結果、210mg/m3の暴露で末梢神経伝達速度の遅れ、105mg/m3以上の暴露で数字符号テストや反応時間の遅れ、126mg/m3以上の暴露で色覚障害が起こりうるとされ、神経機能障害を引き起こす可能性のないと推定される職域の濃度として85mg/m3が提案されている。しかし、生殖への影響等については、交絡要因が非常に多く、現在までのデータからは明かになっていない。
(12) 従ってスチレンの室内濃度指針値の算出には、入手した毒性知見から最も安全サイドにたった数値が得られるデータを採用することとし、(7)のラット11週の吸入毒性データを用いることとした。LOAEL=1260mg/m3として、耐容1日摂取濃度を計算すると、1日24時間及び週7日に平均化し、不確実係数を1000(LOAEL10、種差10、個体間差10)で計算すると、スチレンの室内濃度指針値は、1260mg/m3×6/24×5/7×1/1000 = 0.225mg/m3(=220μg/m3;0.05ppm)と推定された。
(参考文献)
1. IPCS Environmental Health Criteria 26, STYRENE, World Health Organisation, Geneva 1983
2. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, Vol 60, STYRENE, World Health Organisation International Agency for Research on Cancer, Lyon 1994
3. Savolainen, H. et al., Effects of chronic styrene inhalation on rat brain protein metabolism, Acta Neuropath, 1977, 40, 237-241
4. Savolainen, H. et al., Behavioural and glial cell effects of inhalation exposure to styrene vapour with special reference to interactions of simultaneous ethanol intake, Acta Pharmacol. Toxicol., 1980, 46, 51-56
5. Vainio, H. et al., Adaptive changes caused by intermittent styrene inhalation on xenobiotic biotransformation, Toxicol. Appl. Pharmacol., 1979, 49, 7-14
6. Elovaara, E. et al., Effects of intermittent styrene inhalation, ethanol intake and their combination on drug biotransformation in rat liver and kidneys, Med. Biol., 1979, 57, 321-327
7. Toxicological profile for STYRENE (TP-91/25), US Department of Health and Human Services, Agency for Toxic Substances and Disease Registry, 1992
8. 産業衛生学雑誌第41巻4号p130(1999年7月)、(社)日本産業衛生学会
3.クロルピリホスの室内濃度指針値の策定
(1) 遺伝子毒性に関して、雄ショウジョウバエ D.melanogasterにおいて、0.717mg/m3(吸入)、0.05mg/kg(経口)のクロルピリホスの投与によって、全染色体欠損の増加が誘発されることが認められている。またマウス経口14日間投与では、4.18mg/kg/日にて小核の増加が報告されている。
(2) 発がん性を示唆する動物試験データはこれまでのところ報告されていない。ラット及びビーグル犬にクロルピリホス3mg/kg/日を1~2年食餌投与した試験では腫瘍の発生の増加は認められていない。
(3) ヒト血液細胞に対する影響については、最近の報告で、有機リン系殺虫剤を家庭内使用した8事例について調査した結果、通常使用する用量への暴露で、染色体異常を引き起こしたことが示され、将来的な発がんリスク増大への懸念が指摘されている。しかしながら現時点においては、用量相関性を明かにした報告はなく、発がん性の有無についてのデータも報告されていない。
(4) これらより、クロルピリホスについては、ヒト遺伝子障害の可能性を示唆する知見があるものの、用量相関性は明かにされておらず、発がん性との関係も明かにされていないことから、現時点では、クロルピリホスの指針値の策定には、耐容1日摂取量を算出して求めることが適当と判断した。
(5) 急性毒性に関して、マウス吸入LD50が94mg/kg、雌ラット吸入LD50が78mg/kg、ラット経口LD50が82~163mg/kgと報告されている。
(6) 亜急性及び慢性毒性に関して、Fischer344ラットに0、0.075、0.148及び0.295mg/m3のクロルピリホスを1日6時間、週5日、13週間、吸入暴露した試験結果が報告されているが、最大用量でも、呼吸器や肝臓、腎臓、体重、中枢神経系、生殖器、血液学的検査及び生化学的検査等、いづれも影響は認められていない。
(7) 経口投与では、中枢神経系以外の特記すべき影響は認められていない。中枢神経系への毒性に関しては、いくつかの報告がされている。Fischer344妊娠ラットの妊娠6~15日に投与した場合、3及び15mg/kg/日の用量で、赤芽球アセチルコリンエステラーゼ活性の著しい減少が認められ、15mg/kg/日では、有機リン系化合物による中毒症状(過剰唾液、震え等)が観察された。しかし0.1mg/kg/日では、異常は認められなかった。
(8) 雌CF-1マウスに1、10及び25mg/kg/日の用量で妊娠6~15日投与した場合、1mg/kg/日より、血漿及び赤芽球コリンエステラーゼ濃度の著しい低下が認められた。同様な実験を0.1、1及び10mg/kg/日で実施したところ、無影響量は、0.1mg/kg/日であることが確認された。
(9) 赤芽球及び血漿コリンエステラーゼ濃度の著しい低下は、1mg/kg/日を食餌投与したSprague-Dawley雌雄ラットのF1及びF2にも認められたが、0.1mg/kg日では変化は認められなかった。
(10) 鶏を用いた反復投与試験では、1日10mg/kgを20日間投与、4週間の回復期間をおいて観察した結果、体重、脳重量、血中アセチルコリンエステラーゼの著しい減少が認められ、また脳内アセチルコリンエステラーゼ活性が大きく抑制された。
(11) ラットに2年間食餌投与した場合、3mg/kg/日の用量では、いずれの測定時点でも脳内アセチルコリンエステラーゼ活性の抑制が見られ、1及び3mg/kg/日の用量では、血漿及び赤血球アセチルコリンエステラーゼ活性の抑制が認められたが、0.1mg/kg/日以下の用量では影響はみられていない。ビーグル犬に2年間食餌投与した結果でも、1~3mg/kg/日の用量で、同様の所見が認められている。
(12) 生殖発生毒性に関して、(7)においては、15mg/kg/日の用量で、膣出血が観察され、また(8)においては、25mg/kg/日の用量にて、母胎の毒性影響考えられる、胎児の骨格変化が認められているが、それ以外に特記すべき影響は報告されていない。
(13) ヒトでは、クロルピリホスの誤吸入によるアセチルコリンエステラーゼ抑制に由来する中枢神経系の各種症例が報告されている。一方、慢性暴露に関して、クロルピリホスの生産に携わる作業者群175人と有機リン系化合物の暴露経験のないコントロール群335人との間で、疾病の発生の比較調査が実施されているが、特記すべき差は認められていない。
(14) ボランティア成人男性を対象に0.1mg/kg/日を9日、0.03mg/kg/日を20日経口投与した試験が報告されている。前者では血漿コリンエステラーゼ活性が66%抑制されたが、0.03mg/kg/日では影響はみられなかった。
(15) 眼毒性について、ヒト疫学的調査研究や、ビーグル犬に有機リン剤を2年間5-15mg/kg/日経口投与した実験、およびラットにクロルピリフォスを経口投与した実験によれば、近視誘発や眼軸延長の変化による眼屈折の異常の発生が報告されている。なお経口投与をビーグル犬に行なった場合は、半年、及び1年の投与では近視発生は対照との間に有意差なく、最低15ヶ月以上の投与が必要であるとされている。
(16) 本年6月に、米国環境保護庁(US-EPA)から、直近のデータを加味したクロルピリホスのリスク再評価の結果が明かにされているが、その中では、次の2つの新たな知見が報告されている。
(17) まず、慢性毒性に関して、イヌ経口90日及び2年間投与試験、ラット90日及び2年間投与試験、ラット神経発達毒性試験の5試験の結果をweight-of-evidenseの考え方に従って評価した結果、0.22~0.3mg/kg/日の用量で血漿及び赤血球コリンエステラーゼ活性の顕著な抑制が認められ、無毒性量(NOAEL)は、0.03mg/kg/日と決定された。
(18) 次に、ラット神経発達毒性試験に関して、妊娠ラットに2週間クロルピリホスを投与した結果、1mg/kg/日群では、出生後66日の雌仔ラットにおいて、脳外皮質の減少が、顕著な用量依存性をもって認められ、また5mg/kg/日群では、雌雄仔ラットにおいて体重及び体重増加率の減少、食餌摂取量の減少の他、成長抑制、発達遅延、脳重量の減少、脳の形態学的変化が認められた。一方母胎では、0.3mg/kg/日群にて血漿及び赤血球コリンエステラーゼ活性抑制が、1mg/kg/日群にて顕著な脳内コリンエステラーゼ活性抑制が、また5mg/kg/日群では、筋線維束、過呼吸、過行動、体重増加抑制の所見が認められた。最小毒性量(LOAEL)が0.3mg/kg/日と決定されている。
(19) これらの試験結果から、クロルピリホスは低用量でも新生児に影響を及ぼす可能性があること、成熟動物と幼若動物でクロルピリホスへの反応性の明確な違いがあること、クロルピリホスはコリンエステラーゼ抑制作用とは関係なく脳発達に影響を及ぼす可能性のあること、また仔動物の無毒性量(NOAEL)が決定できないこと、が指摘された。
(20) そこでUS-EPAのFQPA(Food Quality Protection Act)安全係数委員会は、クロルピリホス暴露による新生児及び小児への影響を未然防止するためには、安全係数10を維持しなければならないと勧告し、さらにその係数は、急性・慢性暴露や居住暴露の全てにおいて、新生児、小児及び妊娠可能な女性に適用されうると決定している。
(21) 以上のことから、クロルピリホスの指針値の推定においては、より直近のデータによって低濃度での影響が用量相関性をもって明かにされている(18)神経発達毒性試験の結果を用いて計算することが適当と判断した。すなわち、LOAEL=0.3mg/kg/日として耐容1日摂取量を求めた場合、不確実係数1000(LOAEL10、種差10、個体間差10)、ヒト体重50kg、ヒト呼吸量15m3/日として、クロルピリホスの室内濃度指針値=0.3mg/kg/日×1/1000×50kg×1/15m3/日 = 0.001mg/m3(=1μg/m3;0.07ppb)と推定される。なお本物質については、特に、新生児の脳に形態学的変化を起こす知見から、小児等弱者を対象とした指針値として、更に不確実係数10を考慮し、クロルピリホスの室内濃度指針値(小児等弱者に対して)を0.0001mg/m3(=0.1μg/m3;0.007ppb)と推定した。
(22) また、直近のデータも加味した5種類の長期投与試験データからNOAELが決定されている(17)の結果を考慮した場合、NOAEL=0.03mg/kg/日として耐容1日摂取量を求めると、不確実係数100(種差10、個体間差10)、ヒト体重50kg、ヒト呼吸量15m3/日として、クロルピリホスの室内濃度指針値=0.03mg/kg/日×1/100×50kg×1/15m3/日 = 0.001mg/m3(=1μg/m3;0.07ppb)と推定され、(21)と同値となった。
(参考文献)
1. Toxicological profile for CHLORPYRIFOS, US Department of Health and Human Services, Agency for Toxic Substances and Disease Registry, 1997
2. Human Health Risk Assessment CHLORPYRIFOS (revised), US Environmental Protection Agency, Office of Pesticide Programmes, 8 June 2000.
3. Genotoxicity from Domestic Use of Organophosphate Pesticides, A.D.Lieberman et al., JOEM, Volume 40, No.11, November 1998, p954
4. The Organophosphate Pesticide Chlorpyrifos Affects Form Deprivation Myopia, A.M. Geller et al., IOVS, June 1998, Vol.39, No.7, p1290
5. Development of Myopia following chronic organophosphate pesticide intoxication: an epidemiological and experimental study, S.Ishikawa et al., Neurotoxicity of the Visual System, edited by W.H.Merigan and B. Weiss. Raven Press, New York, 1980, p233
6. Increase of Myopia-possible interaction of environmental chemicals, S.Ishikawa et al., Springer-Verlag Tokyo 2000, printed in Hong-Kong.
4.フタル酸ジ-n-ブチルの室内濃度に関する指針値
ごく最近までのフタル酸ジ-n-ブチルに関する毒性研究報告について調査したところ、以下のような結論を得た。
(1) 遺伝子傷害性については、細菌における変異原性試験が行われているが、陰性の結果が得られている1)。
L5178Yマウスを用いたlymphoma cell assayでは、非代謝活性化条件における最高用量で変異体の発現頻度の増加が認められたものの、当該試験については偽陽性の結果が得られやすいという特徴がある2)。
チャイニーズハムスターCHO細胞においては娘染色体交換及び染色体異常が引き起こされなかったものの3)、チャイニーズハムスター線維芽細胞においては、非代謝活性化条件下で、疑陽性の結果が報告されている4)。
マウスを用いたin vivoの小核試験では陰性を示しており2)、その他の遺伝毒性試験においても、概ね陰性の結果が得られている1)。
遺伝子傷害性に関しては、最近の研究報告においても、特に注目すべき知見は得られていない。
(2) 発がん性試験は実施されていないが、2種類の1年間反復投与試験では、いずれも過剰腫瘍の発生は認められていない5) ,6)。 発がん性に関しては、最近の研究報告においても、特に注目すべき知見は得られていない。
(3) これらのことから、ヒトに対してフタル酸ジ-n-ブチルが発がん性であるかどうかは明白でないが、遺伝子傷害性を示さないことから、フタル酸ジ-n-ブチルの室内濃度に関する指針値については非発がん性影響を指標とし、TDIを求める方法で算出するのが適当と考えられる。
(4) 一般毒性では、マウス及びラットに対する急性毒性は弱いが、高用量では通常行動の抑制、呼吸困難、運動調和の欠如等が認められている1)。ヒトに対する感作性が数例報告されているものの、動物に対する皮膚又は眼への刺激性はほとんど認められておらず1)、感作性についてもほとんど認められていない1)。ヒトに対する偶発的な大量暴露では、悪心、嘔吐感や目眩に引き続き、頭痛、眼の痛みと刺激、流涙、羞明感と結膜炎が引き起こされ、尿検査においても色調の異常や、潜血などの所見が認められている7)。
(5) 短期間の反復投与毒性に関しては、ラットに420mg/kg/day以上の用量で経口投与を行ったところ、ペルオキシゾームの増加及び肝腫大等、被験物質の投与影響が認められている1)。
(6) いくつかの長期反復投与毒性試験が行われているが、多くは経口投与によるものである。吸入暴露による毒性関連情報は限られており、毒性評価を行うに際し必ずしも十分なものとは言い難いことから、経口投与による毒性情報が評価の対象とされる1)。例えば、ラットに3ヶ月間、強制経口投与を行ったところ、120mg/kg/day以上の用量で肝相対重量の増加が認められている6)。また、ラットを用いた混餌投与による13週間の反復投与毒性試験において、体重増加抑制、肝腫脹、精巣及び精巣上体の重量減少、肝細胞変性、ペルオキシゾームの増加、精巣の胚細胞変性など、肝臓及び精巣が標的と考えられる投与影響が認められる。LOELはペルオキシゾームの増加で356mg/kg/day、それ以外の肝臓と精巣の変化で720mg/kg/dayとされている2)。さらに妊娠ラットを用いた混餌投与試験においても類似の変化が認められており、この場合のNOELは雄で138mg/kg/day、雌で294mg/kg/dayとされている2)。特に精巣への影響については種差が大きく、マウス及びハムスターでは発現の程度が弱いことが示唆されている1)。なお、マウスを用いた亜慢性毒性試験では、体重及び臓器重量への影響や肝臓の病理組織学的変化が報告されており、NOELは353mg/kg/dayとされている1)。
(7) 作業環境条件下における疫学的な調査がいくつか行われているが、全般的な傾向として、勤続年数が長くなるに伴い、疼痛や知覚異常などが次第に持続していく労働者の割合が増えていくことが示唆されている1)。
(8) 一般毒性に関しては、最近の研究報告においても、特に注目すべき知見は得られていない。
(9) 生殖発生毒性に関する知見がいくつか存在する。全体として、精巣等の顕著な重量減少、精母細胞数の減少、精細管の変性、精巣中における亜鉛及び鉄の含有レベルの低下、テストステロンの血清中濃度の減少及び精巣中濃度の増加、コハク酸脱水素酵素の活性の低下、亜鉛の尿中排泄量の減少等の投与影響が、250 mg/kg/day以上の用量で認められている1)。
(10) 実施された生殖発生毒性試験の中では、ラットを用いた世代試験の結果が注目される。フタル酸ジ-n-ブチルの混餌投与が、対照群と3投与群(それぞれ雌雄の平均値で66, 320及び651mg/kg/dayに相当8))に対して行われており、320mg/kg/day群では、母動物の体重変動は認められないが第1世代の児動物で体重減少が認められており、これは被験物質の投与影響と考えられる。また、すべての投与群において、生存児動物数の減少が統計学的に有意に認められている。
一方、第2世代の児動物における影響はより大きく、すべての投与群において児動物の体重減少が認められている。また、320mg/kg/day群以上で陰核又は陰茎の奇形、精細管の変性、精巣上体の欠如又は発育不全などの異常所見が認められたことに加え、親動物には見られない、651mg/kg/day群での精子形成能への軽微でない影響が認められている。
(11) これらの結果より、フタル酸ジ-n-ブチルの毒性影響は、親動物が暴露されるよりも、発達及び成熟期の児動物に暴露された場合に、より顕著なものとなることが示唆される。当該試験結果におけるNOELは明確ではないが、LOAELは66mg/kg/dayと考えられる1), 2), 9)。
(12) 発生毒性に関しては、ラットにおいて高用量で、統計学的に有意な母動物の体重増加及び児動物の体重減少、奇形の発現頻度の増加等が認められ、NOELは500mg/kg/dayと考えられる10)。
(13) フタル酸ジ-n-ブチルの生殖影響に関する疫学的な調査が行われており、定量的なデータには欠けるものの、フタル酸化合物に暴露された女性については、対照群と比較して妊娠頻度及び出産頻度が減少していることが報告されている。また、月経周期の変動などの生理的変化も観察されており、フタル酸化合物の暴露による影響であることが示唆されているが、定量的なデータに欠ける等により、因果関係等についての明確な結論を導き出すのは困難と考えられている1)。
(14) 生殖発生毒性に関しては、最近の研究報告においても、特に注目すべき知見は得られていない。
(15) 以上の知見から、ヒトに対するフタル酸ジ-n-ブチルの毒性影響を考慮するに当たっては、ヒトの暴露に関する研究報告が重要と考えられるものの、得られているデータが科学的な評価を行うに足るものではなく、他にヒトでの研究報告は見いだされていない。したがって、科学的な評価を行うに足るものとして得られている動物実験データから、ヒトへの毒性影響を外挿することとする。
(16) 動物実験データとしては、上記(10)で注目された、生殖発生毒性が認められた66mg/kg/dayがラットにおけるLOAELと考えられる1)。NOAELについては特定されていない。
(17) UFについては、種差として10、個体差として10、及びNOAELの代わりにLOAELを用いたことから10となり、これらを乗じると1000になる1)。
(18) LOAELをUFで除すことによって、TDIを求めると、
TDI=66(mg/kg/day)/1000=0.066mg/kg/day となる。
(19) 日本人の平均体重を50kg、一日当たりの呼吸量を15m3とすると11)、
0.066(mg/kg/day)×50(kg)/15(m3/day)=0.22mg/m3
=220μg/m3
となる。
これをppmに換算すると、0.02ppmとなる。
(20) よって、ラットにおける生殖発生への影響に基づき、フタル酸ジ-n-ブチルの室内濃度に関する指針値は220μg/m3 (0.02ppm)と設定することが適当と考えられる。
参照文献
1) IPCS (International Programme on Chemical Safety). Di-n-butyl Phthalate. Environmental Health Criteria 1997; 189
2) NTP (National Toxicology Program). NTP technical report on toxicity studies of dibutyl phthalate (CAS No. 84-74-2) administered in feed to F344/N rats and B6C3F1 mice 1995; Toxicity Series No. 30
3) Abe, S.and Sasaki, M. Chromosome aberrations and sister chromatid exchanges in Chinese hamster cells exposed to various chemicals. Journal of the National Cancer Institute 1977; 58 (6): 1635-1641
4) Ishidate, M.and Odashima, S. Chromosome tests with 134 compounds on Chinese hamster cells in vitro - a screening for chemical carcinogens. Mutation Research 1977; 48 (3/4): 337-354
5) Smith, CC. Toxicity of butyl stearate, dibutyl sebacate, dibutyl phthalate and methoxyethyl oleate. Archives of Industrial Hygiene and Occupational Medicine 1953; 7: 310-318
6) Nikonorow, M., Mazur, H. and Piekacz, H. Effect of orally administered plasticizers and polyvinyl chloride stabilizers in the rat. Toxicology and Applied Pharmacology 1973; 26: 253-259
7) Sandmeyer, EE. and Kirwin, CJ. Esters. In: Clayton GD and Clayton FE ed. Patty's industrial hygiene and toxicology 1981; Volume 2A: Toxicology, 3rd rev ed. New York, John Wiley and Sons Inc., 2345-2346
8) NTP. Final report on the reproductive toxicity of di-n-butyl phthalate (CAS No. 84-74-2) in Sprague-Dawley rats 1991; Report No. T-0035C; NTIS Publication No. PB92-111996
9) Wine, R. N., Li, L. H. Barnes, L. H. Gulati, O. K. and Chapin, R. E. Reproductive toxicity of di-n-butylphthalate in a continuous breeding protocol in SD rats. Environmental Health Perspectives 1997; 105(1): 102-107
10) Ema, M., Amano, H., Itami, T. and Kawasaki, H. Teratogenic evaluation of di-n-butyl phthalate in rats. Toxicology Letters 1993; 69(2): 197-203
11) 厚生省生活衛生局企画課生活化学安全対策室.「パラジクロロベンゼンに関する家庭用品専門家会議(毒性部門)報告書」.平成9年8月28日
・3.1.2(3)、3.2.2(3)、3.3.2(4)にある標準物質として、エチルベンゼンの純度が98%以上 の高純度試薬を用いる。
・3.1.3(7)、3.2.3(8)、3.3.3(8)の表1にある測定対象物質と測定用質量数は以下の表による。
| 測定対象物質 | 測定質量数 |
| エチルベンゼン | 91, 106 |
・3.1注7、3.2注10、3.3注8にある標準源ガスにはエチルベンゼンも同時に混合してよ い。
・3.1.2(3)、3.2.2(3)、3.3.2(4)にある標準物質として、スチレンの純度が98%以上の高純度試薬を用いる。
・3.1.3(7)、3.2.3(8)、3.3.3(8)の表1にある測定対象物質と測定用質量数は以下の表による。
| 測定対象物質 | 測定質量数 |
| スチレン | 104, 77 |
・3.1注7、3.2注10、3.3注8にある標準源ガスにはスチレンも同時に混合してよい。
注:捕集剤の種別やロットにより捕集効率が異なることがあるので、回収率を確認しておく必要がある。
1.1.1.測定方法の概要
捕集装置に室内空気及び外気を一定流速で吸引して、測定対象物質を捕集する。捕集装置から測定対象物質を溶媒で溶出させ、これをキャピラリーカラムに導入してGC/MSにより分離、定量することを基本とする。
1.1.2.試薬
(1) アセトン:1μl程度をGC/MSに注入したとき、測定対象物質及び内標準物質のクロマトグラムに妨害を生じないもの。
(2) 標準物質:クロルピリホスは残留農薬分析用標準物質、またはこれと同等以上のもの。
(3) 標準原液(1000μg/ml):各メスフラスコ10mlに標準物質10mgを精秤し、アセトンを加えて10mlとする。この溶液1mlは各々の標準物質1000μgを含む。(注2)(注3)
(4) 標準溶液(100μg/ml):標準原液の一定量をアセトンを用いて10倍に希釈する。この溶液1mlは各々の標準物質100μgを含む。(注2)(注3)
(5) 高純度窒素ガス:測定対象物質及び内標準物質のクロマトグラムに妨害を生じないもの。(注4)
1.1.3.器具および装置
(1) 抽出瓶:ガスクロマトグラフ用バイアル(容量0.1~2ml)
(2) マイクロシリンジ:容量1~10μlまたは10~100μlが計りとれるもの。
(3) 共栓付き試験管:10ml程度が計りとれるもの。(注5)
(4) 試料採取装置:試料採取装置は、捕集装置、マスフローコントローラ、ポンプ、ガスメータとを連結したものから成り、その例を図1に示す。
試料採取装置に使用する器具類は十分に洗浄して汚染に注意する。試料採取に当たって装置を組み立てた後、漏れのないことを確認する。

図1 試料採取装置
1) 捕集装置:スチレンジビニルベンゼン共重合体またはオクタデシルシリル化シリカゲルを捕集剤として利用したもの。またはこれらを組み合わせたもので測定対象物質に対して十分な捕集能力を有するもの。(注6)
2) マスフローコントローラー:流量を1L/min程度(24時間)、1~10L/min程度(約2時間)(注7)の設定流量に対して±10%以内の制御精度を有するもの。または、これと同等以上の性能を有するもの。
3) ポンプ:ダイヤフラム型等の密閉式のポンプで捕集装置をつけた状態で1~10L/minの捕集流量が確保できるもの。または、これと同等以上の性能を有するもの。
4) ガスメータ:湿式型のもの、またはこれと同等の能力のあるもので、積算測定が可能であり、マスフローコントローラの流量制御範囲で精度よく作動する性能を有するもの。
(7) ガスクロマトグラフー質量分析計(GC/MS)
1)GC/MS装置
a) 試料注入口:スプリット/スプリットレス注入が可能なもの。(注8)
b) カラム恒温槽:恒温槽の温度制御範囲が35~300℃であり、測定対象物質の最適分離条件に温度制御できるような昇温プログラムが可能なもの。
c) 分離管:内径0.25~0.32mm、長さ25~60mの溶融シリカ製のものであって、内面にメチルシリコンまたは5%フェニルメチルシリコンを0.5~1.5μmの膜厚で被覆したキャピラリーカラム、またはこれと同等の分離性能を有するもの。
d) インターフェース部:温度を200~300℃程度に保つことができるもの。
e) イオン源:温度を160~300℃に保つことができ、イオン化電圧は70eV程度のもの。
f) 検出器(MS):EI法が可能で、SIMもしくはScan検出法が可能なもの。
g) キャリヤーガス:ヘリウム(純度99.999vol%以上)。1ml/min程度。
h) 測定質量数:各測定対象物質の測定用質量数は表1による。
表1 各測定対象物質の測定用質量数
| 測定対象物質 | 測定質量数 |
| クロルピリホス | 197, 199 |
2) GC/MSの分析条件の設定と機器の調整
GC/MSの分析条件の例を以下に示す。これを参考にして適宜設定する。分離及び定量が十分であればこの限りではない。測定対象物質を検証試験で確認する。
| (20℃/min) | (30℃/min) | カラム温度 | :80℃(1min保持) | ----→ | 230℃(1min保持) | ----→ | 300℃ |
| 注入口温度 | :280℃ | ||||
| 試料注入法 | :スプリットレス | ||||
| インターフェース温度 | :300℃ | ||||
| イオン源温度 | :200℃ |
1.1.4.試料採取および試験液の調製
(1) 試料採取
空気試料の採取は、室内では居間及び寝室2カ所、ならびに室外1カ所についてそれぞれ2回ずつ採取する。試料採取に際しては、トラベルブランクとして捕集装置を密栓したまま状態で試料採取と同様に持ち運ぶ。
1) 室内空気の採取
(a)新築住宅における試料の採取(概ね2時間採取):試料採取装置を用いて10L/min程度の流量で概ね2時間採取する。捕集装置はアルミ箔等で遮光し、試料採取後、捕集装置は密封し、活性炭入り保存缶に入れて分析時まで保存する。(注7)(注8)
(b)居住住宅における試料の採取(24時間採取):試料採取装置を用いて捕集装置に1L/min程度の流量で24時間採取する。捕集装置はアルミ箔等で遮光し、試料採取後、補修装置は密封し、活性炭入り保存缶に入れて分析時まで保存する。(注8)
2) トラベルブランク:トラベルブランク試験用として未使用の密封した捕集装置を用い、試料採取操作を除いて、室内空気の試料採取用の捕集装置と同様に持ち運び、取り扱う。溶封した捕集装置では試料の採取時に開封後、密封して分析時まで同様に保存する。この操作は、一住宅の室内試料採取において一試料もしくは一連の試料採取において試料数の10%程度の頻度で実施する。(注9)
3) 2重測定用捕集装置:試料は、室内の2カ所及び室外1カ所にでそれぞれ2回ずつ 採取し、2重測定(n=2)の意味を持たせる。2重測定のための試料採取は、一住宅の室内試料採取において一試料もしくは一連の試料採取において試料数の10%程度の頻度で行う。(注10)
(2) 試験液の調製
1) 試料空気試験液の調製:
捕集剤からアセトンを用いて抽出する。必要に応じて超音波抽出装置等の装置を利用する。抽出液はメンブレンフィルターもしくは遠心分離器にかけ、浮遊粒子などの夾雑物を取り除く。これを目盛り付き試験管等に受ける。
得られた抽出液に窒素ガスを穏やかに吹き付けて0.5ml以下になる程度まで濃縮し、内標準溶液(100μg/ml)を1μl加えてアセトンで0.5mlに定容したものを試験液とする。
2) 操作ブランク試験液の調製:試料空気用の捕集装置と同一捕集装置について1)と同様の操作を一連の操作の中で一回以上行い、操作ブランク試験液を調製する。(注12)
3) トラベルブランク試験液の調製:トラベルブランク試験用の捕集装置について1)と同様の操作を行い、トラベルブランク試験液を調製する。(注13)
4) 2重測定用試験液の調製:2重測定用の捕集装置について1)の操作を行い、2重測定用試験液を調製する。
1.1.5.試験操作
(1)測定
1) 試料空気の試験
(a) 測定:1.1.4の(2)の1)で調製した試験液の4μl程度をGC/MSに注入する。
(b) 対象化学物質の確認:1.1.3の(7)の1)のh)で設定した各測定対象物質の定量用質量数および確認用質量数によるクロマトグラムを記録し、両者の強度比を求める。(注14)
(c) 定量:検出された各測定対象物質の定量用質量数および内標準物質のピーク面積またはピーク高さを求め、そのピーク面積またはピーク高さの比から、あらかじめ(2)により作成した検量線を用いて、注入した試料液中の各測定対象物質の重量(As:ng)を求める。(注15)
2) 操作ブランク試験:1.1.4の(2)の2)で調製した操作ブランク試験液について1)の操作を行い、各測定対象物質の操作ブランク値を求める。(注16)
3) トラベルブランク試験:1.1.4の(2)の3)で調整したトラベルブランク試験液について1)の操作を行い、注入した試験液中の各測定対象物質の重量を測定する。本試験は3試料以上を測定し、平均値をトラベルブランク値(At:ng)とする。(注17)
4) GC/MS装置の感度試験:混合標準濃度系列の中から中間程度の濃度のものを選び、1)の操作を行って感度の変動を確認する。この確認は1日に1回以上行う。(注18)
5) 2重測定:1.1.4の(2)の4)で調製した2重測定用試験液について1)の操作を行って、各測定対象物質の重量を測定する。(注19)
(2) 検量線の作成
1) 混合標準濃度系列の調製
混合標準溶液を用いて、GC/MSの感度に合わせて混合標準濃度系列を調製する。直接、抽出瓶にアセトン0.5mlを加えて栓をし、標準溶液(100μg/ml)を0.2~10μl、内標準溶液1μlを添加して5段階程度の混合標準濃度系列を調製する。
2)測定:
(a) 測定:1)で調製した混合標準濃度系列の1μl程度をGC/MSに注入し、1.1.3(7)1)のh)で設定した各測定対象物質のクロマトグラムを記録する。
(b) 測定対象物質の確認:1)で調製した検量線用混合標準濃度系列の中から各測定対象物質のGC/MSへの注入量が検量線の中間程度のものを選び、各測定対象物質毎に定量用質量数および確認用質量数のピーク面積またはピーク高さを用いて強度比を算出する。 (注20)
(c) 測定対象物質の検量線作成用質量数の決定:混合標準濃度系列毎に各測定対象物質の強度比を求め、(b)で求めた各測定対象物質毎の強度比と一致することを確認する。(注21)
(d) 検量線の作成:各測定対象物質のピーク面積またはピーク高さを求め、そのピーク面積またはピーク高さの比と各測定対象物質の重量とにより検量線を作成する。
1.1.6.検出下限値、定量下限値の測定
検量線作成時の最低濃度(定量下限値付近)の混合標準濃度系列について、1.1.5の(1)の1)操作を行って測定値(A:ng)を求め、(As-At)にAを代入して、1.1.7の濃度の算出式より空気濃度を算出する。(但し、V=144l、t=20℃、P=101.3kPaとする)5試料以上を測定して求めた標準偏差(s)から次式により、各測定対象物質の検出下限値及び定量下限値を算出する。ただし、操作ブランク値のある物質では操作ブランク値を測定し、混合標準濃度系列と操作ブランク値のうち、大きい方の標準偏差を用いて計算する。(注22)
この測定は機器の分析条件を設定した場合など必要に応じて必ず1回以上行う。
目標定量下限値はガイドライン値の1/10とする。
1.1.7.濃度の算出
1.1.5の(1)で得られた結果から次式を用いて空気中の各測定対象物質の濃度を算出する。
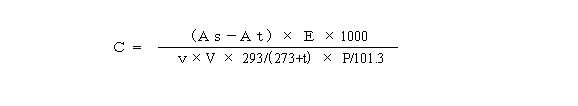
| C | : | 20℃における空気中の各測定対象物質の濃度 (mg/m3) |
| As | : | GC/MSに注入した試料中の各測定対象物質の重量(ng) |
| At | : | 各測定対象物質のトラベルブランク値(ng) 操作ブランク値と同等と見なせる場合は操作ブランク値を用いる。 |
| E | : | 試験液量(ml) |
| v | : | GC/MSへの注入液量(μl) |
| V | : | ガスメータで測定した捕集量(l) |
| t | : | 試料採取時の平均の気温(℃)。湿式型積算流量計を使用しているときには、積算流量計の平均水温(℃) |
| P | : | 試料採取時の平均大気圧(kPa)。湿式型積算流量計の場合には(P-Pw)を用いる。 ここで、Pwは試料採取時の平均気温tでの飽和水蒸気圧(kPa) |
結果には個々の測定値と各場所における平均値の両方を記載する。
注 1:精度が保証されているならば検出器として炎光光度検出器(FPD)を用いることも可 能である。物質の同定はリテンションタイムによることになるが、検出感度はこちらのほうが高い。この場合内標準物質はリンを含んだ物質を利用する。
注 2:試料採取量、濃縮操作及びGC/MSの条件等によって測定感度は異なるので、ここ に示した濃度を目安に適宜変えてもよい。
注 3:FPDを用いて測定する場合は、保持時間等を標準溶液を用いて確認する。
注 4:精製空気を使用してもよい。有機化合物を含有しないことが重要であり、測定対象以外の物質については全炭化水素で0.01ppm以下、一酸化炭素0.05ppm以下、二酸化炭素0.3ppm以下、水分濃度2ppm以下(露点-70℃以下)で純度99.999%以上のものが望ましい。
注 5:3000rpm程度の遠心ができ、目盛りが付いているものが望ましい。
注 6:十分な性能を有する市販品を利用してよい。この場合の捕集物の抽出法に関しては説明書を参照すること。捕集装置がフィルター状の場合、フィルターを通気漏れのないよう吸引部に固定できるフィルターホルダーを使用する。
注7:測定対象下限値を考慮して採取時間をある程度前後させてもよい。
注 8:感度を得る目的で大容量注入法を用いてもよい。
注 9:室内より室外での化学物質濃度が高いと考えられる事情があるときは、トラベルブランクは室外で行う。
注10:採取は2回ずつ行うが、分析について2重に行うのは10%の頻度でもよい。指針 値近傍の測定値が得られた場合などは採取した2本とも分析する必要がある。
注11:フィルター上の粉塵の損失に留意すること。
注12:分析環境から試験操作過程で汚染されることがあるので、操作ブランクを一連の測定操作の中で少なくとも一回以上実施する。
注13:空気試料の測定に際して、その準備-機器の運搬-試料採取-持ち帰り-前処理-測定の過程で化学物質で汚染された空気で捕集管が暴露する可能性があるので試料採取時の記録を参考にして試験の頻度を考慮する。
注14:定量用質量数のピークに対する他イオンからの影響を判断するために行う操作であり、強度比が検量線作成時と大きくかけはなれている場合は、まず、装置の性能を確認するために再度標準試料を測定して強度比を算出する。その強度比が90~110%の範囲内であれば、測定済み試料のクロマトグラムのベースライン等を再検討したり、かけ離れた原因をチェックして再分析を行い、その強度比が検量線作成時と大きくかけはなれないことを確認する。
注15:試料空気の測定値が作成した検量線の直線範囲からはずれている場合は、分析の諸条件を検討したうえで検量線を作成し直し、再度測定する。
注16:操作ブランク試験は試料測定に先立って行い、操作ブランク値を大気濃度に換算した値が目標定量下限値を超える場合には、再洗浄や機器の調製を行った後、再度測定し、操作ブランク値を十分低減してから試験液を測定する。
注17:測定対象物質のトラベルブランク値が操作ブランク値と同等(等しいか小さい)とみなせる場合には移送中の汚染は無視できるものとして試料の測定値から操作ブランク値を差し引いて濃度を計算する。移送中の汚染がある場合には、3試料以上のトラベルブランク値を測定した時の標準偏差(s)から求めた定量下限値(10s:大気濃度への換算値)が目標定量下限値以下の場合、およびトラベルブランク値による定量下限値が目標定量下限値より大きくても試料の測定値が、トラベルブランク値による定量下限値以上の場合には、試料の測定値からトラベルブランク値を差し引いて濃度を計算する。 しかし、移送中に汚染があり、またトラベルブランク値による定量下限値が目標定量下限値より大きく、しかも試料の測定値がトラベルブランク値による定量下限値より小さい場合は原則として欠測扱いとする。この場合には、汚染の原因を取り除いた後、再度試料採取から行う。
注18:内標準物質の感度が検量線作成時の感度と大きく異ならないことを確認する。また、内標準物質との相対感度が検量線作成時の相対感度に対して±20%以内の変動であることを確認し、これを越えて感度が変動する場合には、その原因を取り除き、それ以前の試料を再測定する。さらに、保持時間については、比較的短い間に変動(通常、1日に保持時間が±5%以上、内標準物質との相対保持比が±2%以上)する場合には、その原因を取り除き、それ以前の試料の再測定を行う。
注19:定量下限値以上の濃度の測定対象物質に対して、測定値平均とそれぞれの測定値の間に±15%以上の開きがある場合は、原則として欠測扱いとして、その原因をチェックし、再度試料採取を行う。
注20:FPDを用いる場合はリテンションタイムで測定対象物質を確認する。
注21:測定対象物質のいずれかの強度比が(b)で算出した90~110%の範囲を超える場合 は、その濃度の混合標準濃度系列を再度測定する。
注22:測定対象物質のいずれかの定量下限値が目標下限値より大きい場合には、試薬、器具、機器等をチェックして、目標定量下限値以下になるよう調整する。
ここに掲げる測定方法は、室内空気中のフタル酸ジ-n-ブチルを対象とする。室内空気の採取は、新築住宅における場合と居住住宅における場合は二つの異なる方法による。室内空気採取は、居間(リビング)および寝室で採取し、いずれかの高い値を記載し、評価する。また外気の影響を考慮するため、同時に外気も採取する。試料は、固相吸着-溶媒抽出法、固相吸着-加熱脱着法の2種の方法のいずれかを用いて採取し、ガスクロマトグラフ/質量分析計と連動した装置によって測定する。
1.1 第1法 固相吸着-溶媒抽出-ガスクロマトグラフ/質量分析法
1.1.1.測定方法の概要
吸着剤を充てんした捕集装置に室内空気及び外気を一定流速で吸引して、測定対象物質を捕集する。捕集管から測定対象物質を溶媒で溶出させ、これをキャピラリーカラムに導入してGC/MSにより分離、定量することを基本とする。(注1)
1.1.2.試薬
(1) アセトン:1μl程度をGC/MSに注入したとき、測定対象物質及び内標準物質のクロマトグラムに妨害を生じないもの。
(3) 標準物質:フタル酸エステル分析用として市販されているもの。
(4) 標準原液(1000μg/ml):各メスフラスコ100mlに標準物質100mgを精秤し、アセトンを加えて100mlとする。この溶液1mlは各々の標準物質1000μgを含む。(注2)(注3)
(5) 標準溶液(100μg/ml):標準原液の一定量をアセトンを用いて10倍に希釈する。この溶液1mlは各々の標準物質100μgを含む。(注2)(注3)
(7) 高純度窒素ガス:測定対象物質のクロマトグラムに妨害を生じないもの。(注4)
(10) 内標準原液(1000μg/ml):内標準物質(フタル酸ジ-n-ブチル-d4)の100mgを精秤し、アセトン100mlに溶解する。(注2)(注3)
(11) 内標準溶液(100μg/ml):内標準原液をアセトンで10倍に希釈する。この溶液1mlは内標準物質100μgを含む。(注2)(注3)
1.1.3.器具および装置
(1) 抽出瓶:スクリューキャップバイアル(容量2ml程度)
(3) マイクロシリンジ:容量1~10μlまたは10~100μlが計りとれるもの。
(4) ガスタイトシリンジ:容量1~10mlまたは10~100mlが計りとれるもの。
(6) 試料採取装置:試料採取装置は、捕集装置、マスフローコントローラ、ポン
プ、ガスメータとを連結したものから成り、その例を図1に示す。
試料採取装置に使用する器具類は十分に洗浄して汚染に注意する。試料採取に当たって装置を組み立てた後、漏れのないことを確認する。(注5)

図1 試料採取装置
1)捕集装置
捕集剤として、カーボン系吸着剤、オクタデシルシリル化シリカゲル、またはスチレンジビニルベンゼン共重合体を用いる。その他、測定対象物質に対して十分な捕集能力を有するもの。(注6)
2) マスフローコントローラー:流量を1~10L/minの範囲で制御でき、設定流量に対して±10%以内の制御精度を有するもの。または、これと同等以上の性能を有するもの。
3) ポンプ:ダイヤフラム型等の密閉式のポンプで捕集管をつけた状態で1~10L/minの捕集流量が確保できるもの。または、これと同等以上の性能を有するもの。
4) ガスメータ:湿式型のもの、またはこれと同等の能力のあるもので、積算測定が可能であり、マスフローコントローラの流量制御範囲で精度よく作動する性能を有するもの。
(7) ガスクロマトグラフー質量分析計(GC/MS)
1)GC/MS装置
a) 試料注入口:スプリット/スプリットレス注入が可能なもの。
b) カラム恒温槽:恒温槽の温度制御範囲が35~300℃であり、測定対象物質の最適分離条件に温度制御できるような昇温プログラムが可能なもの。
c) 分離管:内径0.25~0.32mm、長さ25~60mの溶融シリカ製のものであって、内面にメチルシリコンまたは5%フェニルメチルシリコンを0.5~1.5μmの膜厚で被覆したキャピラリーカラム、またはこれと同等の分離性能を有するもの。
d) インターフェース部:温度を200~300℃程度に保つことができるもの。
e) イオン源:温度を160~300℃に保つことができ、イオン化電圧は70eV程度のもの。
f) 検出器(MS):EI法が可能で、SIMもしくはScan検出法が可能なもの。
g) キャリヤーガス:ヘリウム(純度99.999vol%以上)。1ml/min程度。
h) 測定質量数:各測定対象物質の測定用質量数は表1による。
表1 各測定対象物質の測定用質量数
| 測定対象物質 | 測定質量数 |
| フタル酸ジ-n-ブチル フタル酸ジ-n-ブチルd4 | 149,150 153,154 |
2) GC/MSの分析条件の設定と機器の調整
GC/MSの分析条件の例を以下に示す。これを参考にして適宜設定する。分離及び定量が十分であればこの限りではない。測定対象物質を検証試験で確認する。
| (10℃/min) | (10℃/min) | カラム温度 | :60℃(1分間保持) | ----→ | 200℃ | ----→ | 300℃ |
| 注入口温度 | :280℃ | ||||
| 試料注入法 | :スプリットレス | ||||
| インターフェース温度 | :300℃ | ||||
| イオン源温度 | :200℃ |
*MSに質量校正用標準物質(PFTBA またはPFK)を導入し、質量校正用プログラムにより、マスパターン、分解能{質量数(m/z)=18~300程度の範囲で1質量単位(amu)以上}等を測定目的に応じて所定の値に校正する。質量校正結果は測定結果と共に保存する。
1.1.4.試料採取および試験液の調製
(1) 試料採取
空気試料の採取は、室内では居間及び寝室2カ所、ならびに室外1カ所についてそれぞれ2回ずつ採取する。試料採取に際しては、トラベルブランクとして捕集装置を密封したまま状態で試料採取と同様に持ち運ぶ。
1) 室内空気の採取
(a)新築住宅における試料の採取(概ね30分間採取):試料採取装置を用いて1~10L/min程度の流量で概ね30分間採取する。捕集装置はアルミ箔等で遮光し、試料採取後、捕集装置は密封し、活性炭入り保存缶に入れて分析時まで保存する。(注7)(注8)
(b)居住住宅における試料の採取(24時間採取):試料採取装置を用いて捕集装置に1~10L/min程度の流量で24時間採取する。捕集装置はアルミ箔等で遮光し、試料採取後、捕集装置は密封し、活性炭入り保存缶に入れて分析時まで保存する。(注8)
2) トラベルブランク:トラベルブランク試験用として未使用の密封した捕集装置を用い、試料採取操作を除いて、室内空気の試料採取用の捕集装置と同様に持ち運び、取り扱う。溶封した捕集装置では試料の採取時に開封後、密栓して分析時まで同様に保存する。この操作は、一住宅の室内試料採取において一試料もしくは一連の試料採取において試料数の10%程度の頻度で実施する。
3) 2重測定用捕集装置:試料は、室内の2カ所及び室外1カ所にでそれぞれ2回ずつ 採取し、2重測定(n=2)の意味を持たせる。2重測定のための試料採取は、一住宅の室内試料採取において一試料もしくは一連の試料採取において試料数の10%程度の頻度で行う。
(2) 試験液の調製
1) 試料空気試験液の調製:
捕集剤からアセトン10ml程度を用いて抽出する。必要に応じて、超音波抽出装置等を用いる。抽出液はメンブレンフィルターもしくは遠心分離器にかけ、浮遊粒子などの夾雑物を取り除く。これを目盛り付き試験管等に受ける。(注9)
得られた抽出液をとり窒素ガスを穏やかに吹き付けて1ml程度まで濃縮し、内標準溶液(100μg/ml)を1μl加えてアセトンで1mlに定容したものを試験液とする。
2) 操作ブランク試験液の調製:試料空気用の捕集装置と同一の洗浄済み捕集装置について1)と同様の操作を一連の操作の中で一回以上行い、操作ブランク試験液を調製する。(注10)
3) トラベルブランク試験液の調製:トラベルブランク試験用の捕集装置について1)と同様の操作を行い、トラベルブランク試験液を調製する。(注11)
4) 2重測定用試験液の調製:2重測定用の捕集装置について1)の操作を行い、2重測定用試験液を調製する。(注12)
1.1.5.試験操作
(1)測定
1) 試料空気の試験
(a) 測定:1.1.4の(2)の1)で調製した試験液の1 μl程度をGC/MSに注入する。
(b) 対象化学物質の確認:1.1.3の(7)の1)のh)で設定した各測定対象物質の定量用質量数および確認用質量数によるクロマトグラムを記録し、両者の強度比を求める。(注13)
(c) 定量:検出された各測定対象物質の定量用質量数および内標準物質のピーク面積またはピーク高さを求め、そのピーク面積またはピーク高さの比から、あらかじめ(2)により作成した検量線を用いて、注入した試料液中の各測定対象物質の重量(As:ng)を求める。(注14)
2) 操作ブランク試験:1.1.4の(2)の2)で調製した操作ブランク試験液について1)の操作を行い、各測定対象物質の操作ブランク値を求める。(注15)
3) トラベルブランク試験:1.1.4の(2)の3)で調整したトラベルブランク試験液について1)の操作を行い、注入した試験液中の各測定対象物質の重量を測定する。本試験は3試料以上を測定し、平均値をトラベルブランク値(At:ng)とする。(注16)
4) GC/MS装置の感度試験:混合標準濃度系列の中から中間程度の濃度のものを選び、1)の操作を行って感度の変動を確認する。この確認は1日に1回以上行う。(注17)
5) 2重測定:3.1.4の(2)の4)で調製した2重測定用試験液について1)の操作を行って、各測定対象物質の重量を測定する。(注18)
(2) 検量線の作成
1) 混合標準濃度系列の調製
(a) 溶液混合標準列の調製:混合標準溶液を用いて、GC/MSの感度に合わせて混合標準濃度系列を調製する。抽出瓶に混合標準溶液(100μg/ml)を0.5~10μl、内標準溶液1μlを添加して5段階程度の混合標準濃度系列を調製する。
2)測定:
(a) 測定:1)で調製した混合標準濃度系列の1μl程度をGC/MSに注入し、1.1.3(7)1)のh)で設定した各測定対象物質のクロマトグラムを記録する。
(b) 測定対象物質の確認:1)で調製した検量線用混合標準濃度系列の中から各測定対象物質のGC/MSへの注入量が検量線の中間程度のものを選び、各測定対象物質毎に定量用質量数および確認用質量数のピーク面積またはピーク高さを用いて強度比を算出する。
(c) 測定対象物質の検量線作成用質量数の決定:混合標準濃度系列毎に各測定対象物質の強度比を求め、(b)で求めた各測定対象物質毎の強度比と一致することを確認する。(注19)
(d) 検量線の作成:各測定対象物質のピーク面積またはピーク高さを求め、そのピーク面積またはピーク高さの比と各測定対象物質の重量とにより検量線を作成する。
1.1.6.検出下限値、定量下限値の測定
検量線作成時の最低濃度(定量下限値付近)の混合標準濃度系列について、1.1.5の(1)の1)操作を行って測定値(A:ng)を求め、(As-At)にAを代入して、1.1.7の濃度の算出式より空気濃度を算出する。(但し、V=144l、t=20℃、P=101.3kPaとする)5試料以上を測定して求めた標準偏差(s)から次式により、各測定対象物質の検出下限値及び定量下限値を算出する。ただし、操作ブランク値のある物質では操作ブランク値を測定し、混合標準濃度系列と操作ブランク値のうち、大きい方の標準偏差を用いて計算する。(注20)
この測定は機器の分析条件を設定した場合など必要に応じて必ず1回以上行う。
目標定量下限値はガイドライン値の1/10とする。
1.1.7.濃度の算出
1.1.5の(1)で得られた結果から次式を用いて空気中の各測定対象物質の濃度を算出する。
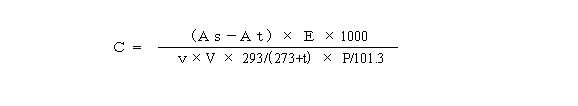
| C | : | 20℃における空気中の各測定対象物質の濃度 (mg/m3) |
| As | : | GC/MSに注入した試料中の各測定対象物質の重量(ng) |
| At | : | 各測定対象物質のトラベルブランク値(ng) 操作ブランク値と同等と見なせる場合は操作ブランク値を用いる。 |
| E | : | 試験液量(ml) |
| v | : | GC/MSへの注入液量(μl) |
| V | : | ガスメータで測定した捕集量(l) |
| t | : | 試料採取時の平均の気温(℃)。湿式型積算流量計を使用しているときには、積算流量計の平均水温(℃) |
| P | : | 試料採取時の平均大気圧(kPa)。湿式型積算流量計の場合には(P-Pw)を用いる。 ここで、Pwは試料採取時の平均気温tでの飽和水蒸気圧(kPa) |
結果には個々の測定値と各場所における平均値の両方を記載する。
注 1:フタル酸エステル類の測定精度は、試料の採取、前処理、測定操作におけるフタル酸エステル類のブランクをいかに低くするかにかかっており、器具の洗浄等には十分に配慮する必要がある。
注 2:試料採取量、濃縮操作及びGC/MSの条件等によって測定感度は異なるので、ここ に示した濃度を目安に適宜変えてもよい。
注 3:標準及び内標の原液、溶液は市販のものを用いても良い。精度保証されているものが望ましい。
注 4:精製空気を使用してもよい。有機化合物を含有しないことが重要であり、測定対象以外の物質については全炭化水素で0.01ppm以下、一酸化炭素0.05ppm以下、二酸化炭素0.3ppm以下、水分濃度2ppm以下(露点-70℃以下)で純度99.999%以上のものが望ましい。
注 5:各装置の接続にはなるべくシールテープは使用せず、テフロンコネクタなどを使用する。
注 6:吸着剤や器具は使用前にアセトンで洗浄し、十分乾かしてから用いる。乾燥が不十分であると室内を二次汚染する可能性がある。空気の取り入れ口側には捕集剤の前に石英ウールを重層しておく。捕集剤がフィルター状の場合フィルターを通気漏れのないよう吸引部に固定できるフィルターホルダーを用いる。
注7:測定に十分な量が得られないと考えられる場合は、採取時間をある程度長くしても よい。ブランクの影響を少なくするためにはある程度大量に採取したほうがよい。
注 8:吸引側及び空気取り入れ側を明確にしておく。
注 9:吸着剤にカーボン系のものを用いた場合には、溶出はジクロロメタンを用いたほうが回収率が上がる。
注10:分析環境から試験操作過程で汚染されることがあるので、操作ブランクを一連の測定操作の中で少なくとも一回以上実施する。
注11:空気試料の測定に際して、その準備-機器の運搬-試料採取-持ち帰り-前処理-測定の過程で化学物質で汚染された空気で捕集管が暴露する可能性があるので試料採取時の記録を参考にして試験の頻度を考慮する。
注12:採取は2回ずつ行うが、分析について2重に行うのは10%の頻度でもよい。指針 値近傍の測定値が得られた場合などは採取した2本とも分析する必要がある。
注13:定量用質量数のピークに対する他イオンからの影響を判断するために行う操作であり、強度比が検量線作成時と大きくかけはなれている場合は、まず、装置の性能を確認するために再度標準試料を測定して強度比を算出する。その強度比が90~110%の範囲内であれば、測定済み試料のクロマトグラムのベースライン等を再検討したり、かけ離れた原因をチェックして再分析を行い、その強度比が検量線作成時と大きくかけはなれないことを確認する。
注14:室内空気中の各対象化合物の濃度は範囲が広いことが予想されるため、定量上限を明確に把握しておくことが必要である。試料空気の測定値が作成した検量線の直線範囲からはずれている場合は、分析の諸条件を検討したうえで検量線を作成し直し、再度測定する。
注15:操作ブランク試験は試料測定に先立って行い、操作ブランク値を大気濃度に換算した値が目標定量下限値を超える場合には、再洗浄や機器の調製を行った後、再度測定し、操作ブランク値を十分低減してから試験液を測定する。
注16:測定対象物質のトラベルブランク値が操作ブランク値と同等(等しいか小さい)とみなせる場合には移送中の汚染は無視できるものとして試料の測定値から操作ブランク値を差し引いて濃度を計算する。移送中の汚染がある場合には、3試料以上のトラベルブランク値を測定した時の標準偏差(s)から求めた定量下限値(10s:大気濃度への換算値)が目標定量下限値以下の場合、およびトラベルブランク値による定量下限値が目標定量下限値より大きくても試料の測定値が、トラベルブランク値による定量下限値以上の場合には、試料の測定値からトラベルブランク値を差し引いて濃度を計算する。 しかし、移送中に汚染があり、またトラベルブランク値による定量下限値が目標定量下限値より大きく、しかも試料の測定値がトラベルブランク値による定量下限値より小さい場合は原則として欠測扱いとする。この場合には、汚染の原因を取り除いた後、再度試料採取から行う。
注17:内標準物質の感度が検量線作成時の感度と大きく異ならないことを確認する。また、内標準物質との相対感度が検量線作成時の相対感度に対して±20%以内の変動であることを確認し、これを越えて感度が変動する場合には、その原因を取り除き、それ以前の試料を再測定する。さらに、保持時間については、比較的短い間に変動(通常、1日に保持時間が±5%以上、内標準物質との相対保持比が±2%以上)する場合には、その原因を取り除き、それ以前の試料の再測定を行う。
注18:定量下限値以上の濃度の測定対象物質に対して、測定値平均とそれぞれの測定値の間に±15%以上の開きがある場合は、原則として欠測扱いとして、その原因をチェックし、再度試料採取を行う。
注19:測定対象物質のいずれかの強度比が(b)で算出した90~110%の範囲を超える場合 は、その濃度の混合標準濃度系列を再度測定する。
注20:測定対象物質のいずれかの定量下限値が目標下限値より大きい場合には、試薬、器具、機器等をチェックして、目標定量下限値以下になるよう調整する。
1.2 第2法 固相吸着-加熱脱着-ガスクロマトグラフ質量分析法
1.2.1.測定方法の概要
吸着剤を充填した捕集管に室内空気及び外気を一定流量で吸引し測定対象物質を捕集する。捕集管を加熱脱着装置に装着し、加熱脱着する測定対象物質をキャピラリーカラムに導入してGC/MSにより分離、定量することを基本とする。(注1)
1.2.2.試薬
(1) アセトン:残留農薬測定用などの高純度のもの。GC/MSに注入しても、測定対象物質及び内標準物質のクロマトグラムに妨害を生じないもの。
(3) 標準物質:フタル酸エステル分析用として市販されているもの。
(4) 標準原液(1000μg/ml):各メスフラスコ100mlに標準物質100mgを精秤し、アセトンを加えて100mlとする。この溶液1mlは各々の標準物質1000μgを含む。(注2)(注3)
(5) 標準溶液(100μg/ml):標準原液の一定量をアセトンを用いて10倍に希釈する。この溶液1mlは各々の標準物質100μgを含む。(注2)(注3)
(7)高純度窒素ガス:測定対象物質及び内標準物質のクロマトグラムに妨害を生じないもの。(注4)
(10) 内標準原液(1000μg/ml):内標準物質(フタル酸ジ-n-ブチル-d4)の100mgを精秤し、アセトン100mlに溶解する。(注2)
(11) 内標準溶液(100μg/ml):内標準原液をアセトンで10倍に希釈する。この溶液1mlは内標準物質100μgを含む。(注2)
1.2.3器具および装置
(3) マイクロシリンジ:容量1~10μlまたは10~100μlが計りとれるもの。
(4) ガスタイトシリンジ:容量1~10mlまたは10~100mlが計りとれるもの。
(5) 検量線作成用T字管:図1に示すように、注入口のセプタム、捕集管及び高純度窒素ガスが接続できるもので、高純度窒素ガスを30~50ml/minの流速で3~5分間通気させることができるもの。
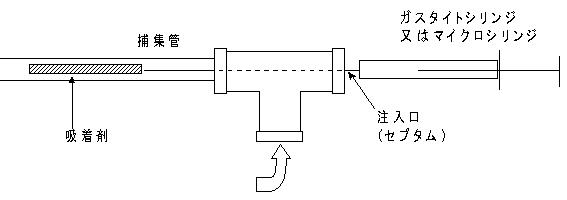
図1 検量線作成用T字管
(6) 試料採取装置:試料採取装置は、捕集管、マスフローコントローラ、ポンプ、ガスメータとを連結したものから成り、その例を図2に示す。 試料採取装置に使用する器具類は十分に洗浄して汚染に注意する。試料採取に当たって装置を組み立てた後、漏れのないことを確認する。(注5)

図2 試料採取装置
1)捕集管
a) 捕集管:内径3~4mm程度のガラス管に測定対象物質を吸着・保持し、且つ加熱による脱着が十分に行うことができる吸着剤を充てんし、両端を石英ウールで押さえたもの、または測定対象物質に対して十分な捕集能力を有するもの。(注6)
b) 調製:加熱炉に捕集管を装着し、高純度窒素等を毎分50ml程度に流して捕集管内の空気を十分置換した後、高純度窒素等を流したまま300℃程度で2時間以上空焼き洗浄し冷却後、両端を密栓する。調製した捕集管は活性炭入り密閉できるガラスまたは金属管に保存する。なるべく使用直前に調製する。
3) マスフローコントローラー:流量を5~20ml/minまたは30~200ml/minの範囲で制御でき、設定流量に対して±10%以内の制御精度を有するもの。または、これと同等以上の性能を有するもの。
4) ポンプ:ダイヤフラム型等の密閉式のポンプで捕集管をつけた状態で5~200ml/minの捕集流量が確保できるもの。または、これと同等以上の性能を有するもの。
5) ガスメータ:湿式型のもの、またはこれと同等の能力のあるもので、積算測定が可能であり、マスフローコントローラの流量制御範囲で精度よく作動する性能を有するもの。
(7)試料導入装置
捕集管の加熱部と、トラップ管及びクライオフォーカスの再捕集部の冷却・加熱部、またはそのどちらかが組み込まれたもので、その例は図3のようである。(注7)
捕集管が試料導入装置に装着されると流路と接続され、捕集管を加熱して、脱着する測定対象物質を再捕集部に濃縮した後、再捕集部を加熱して濃縮した対象物質をGC/MSに直結して導入できる装置であり、キャピラリーカラムの前段に内径0.5mm程度の中空細管、または内径2mm以下の細管に適当な吸着剤等を充填したものを取り付け、この部分を液体窒素等で-100℃以下に温度制御でき、かつ80℃以上に急速加熱できるもの、または、これと同等以上の性能を有するもの。(注8)さらに、捕集管及び、または再捕集部の後にスプリットができる装置を備えたもの。
1)トラップ部:トラップ管とその加熱部からなるもの。
(a)トラップ管:捕集管と連結され、捕集管から脱着してきた測定対象物質をトラップするもので、常温又は-20~-100℃程度に冷却できるもの。(注9)
(b)加熱部:80℃/min程度で加熱でき、かつ脱着流速が30~50ml/min確保できるもの。
2)クライオフォーカス部:クライオフォーカスとその加熱部からなるもの。
(a)クライオフォーカス装置:キャピラリーカラムの直前で冷却して測定対象物質をクライオフォーカスできるもの。
(b)加熱部:250℃/min程度で加熱でき、スプリットが可能な流速が確保されること。
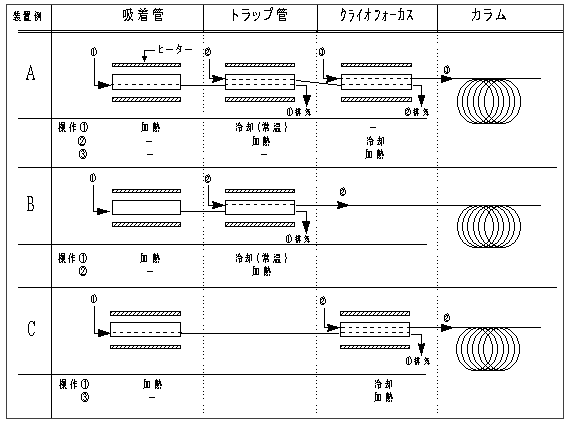
図3 試料導入装置の例
(8) ガスクロマトグラフー質量分析計(GC/MS)
1)GC/MS装置
a) 試料注入口:試料導入装置又はスプリット/スプリットレス注入が可能なもの。
b) カラム恒温槽:恒温槽の温度制御範囲が35~300℃であり、測定対象物質の最適分離条件に温度制御できるような昇温プログラムが可能なもの。
c) 分離管:内径0.25~0.32mm、長さ25~60mの溶融シリカ製のものであって、内面にメチルシリコンまたは5%フェニルメチルシリコンを0.5~1.5μmの膜厚で被覆したキャピラリーカラム、またはこれと同等の分離性能を有するもの。
d) インターフェース部:温度を200~300℃程度に保つことができるもの。
e) イオン源:温度を160~300℃に保つことができ、イオン化電圧は70eV程度のもの。
f) 検出器(MS):EI法が可能で、SIM又はScan検出法が可能なもの。
g) キャリヤーガス:ヘリウム(純度99.999vol%以上)。1ml/min程度。
h) 測定質量数:各測定対象物質の測定用質量数は表1による。
| 測定対象物質 | 測定質量数 |
| フタル酸ジ-n-ブチル フタル酸ジ-n-ブチルd4 | 149,150 153,154 |
2) GC/MSの分析条件の設定と機器の調整
加熱脱着装置、GC/MSの分析条件の例を以下に示す。これを参考にして適宜設定する。分離及び定量が十分であればこの限りではない。測定対象物質を検証試験で確認する。
a)加熱脱着装置 (60℃/min) 加熱脱着温度:20℃(2min)---→280℃(5min) 脱着流量 :50ml/min
b)GC/MS
(10℃/min) カラム温度 :40℃(2分間保持)---→280℃ 注入口温度 :280℃ 試料注入法 :スプリット(スプリット比1:20~1:100) インターフェース温度:300℃ イオン源温度 :200℃
*MSに質量校正用標準物質(PFTBA またはPFK)を導入し、質量校正用プログラムにより、マスパターン、分解能{質量数(m/z)=18~300程度の範囲で1質量単位(amu)以上}等を測定目的に応じて所定の値に校正する。質量校正結果は測定結果と共に保存する。
1.2.4.試料採取および試験液の調製
(1) 試料採取
試料採取に際しては、室内2カ所、外気1カ所を各2試料づつ、計6試料を採取する。また、トラベルブランクとして捕集管を密栓したまま状態で試料採取とを試料採取時の操作と同様に持ち運ぶ。
1) 室内空気の採取
(a)新築住宅における試料の採取(概ね30分間採取):試料採取装置を用いて、概ね30分間、100~200mL/min程度の流量で採取する。捕集管はアルミ箔等で遮光し、試料採取後、捕集管の両端を密栓し、活性炭入り保存缶に入れて分析時まで保存する。(注10)
(b)居住住宅における試料の採取(24時間採取):試料採取装置を用い24時間、10~100mL/min程度の流量で採取する。捕集管はアルミ箔等で遮光し、試料採取後、捕集管の両端を密栓し、活性炭入り保存缶に入れて分析時まで保存する。(注10)
2) 2重測定用の捕集管:試料は室内の2カ所及び室外1カ所でそれぞれ2回ずつ採取する。同時に2重測定(n=2)の意味を持たせる。2重測定のための試料採取は、一住宅の室内試料採取において一試料もしくは一連の試料採取において試料数の10%程度の頻度で行う。
3) トラベルブランク:トラベルブランク試験用として未使用の密栓した捕集管を用い、試料採取操作を除いて、室内空気の試料採取用の捕集管と同様に持ち運び、取り扱う。溶封した捕集管では試料の採取時に開封後、密栓して分析時まで同様に保存する。この操作は、一住宅の室内試料採取において一試料もしくは一連の試料採取において試料数の10%程度の頻度で実施する。(注11)
(2) 試験捕集管の調製
1) 試料空気捕集管の調製:図1の例に示すように、試料を採取した捕集管に検量線作成用T字管及び高純度窒素ガスを連結し、毎分10~30ml程度の高純度窒素等を流しながら、内標準溶液1μlをマイクロシリンジで注入して捕集管に吸着させる。
2) 操作ブランク試験捕集管の調製:試料空気用の捕集管と同一ロットの捕集管について1)と同様の操作を一連の操作の中で一回以上行い、操作ブランク試験捕集管を調製する。(注12)
3) トラベルブランク試験捕集管の調製:トラベルブランク試験用の捕集管については、内標準ガスまたは内標準液の添加の操作を省いて、そのままトラベルブランク試験捕集管とする。(注13)
4) 2重測定用試験液の調製:2重測定用の捕集管について1)の操作を行い、2重測定用試験液を調製する。
1.2.5.試験操作
(1)測定
1) 試料空気の試験
(a) 測定:1.2.4の(2)の1)で調製した捕集管を試料導入装置に装着し、GC/MSを操作させる。
(b) 対象化学物質の確認:1.2.3の(8)の1)のh)で設定した各測定対象物質の定量用質量数および確認用質量数によるクロマトグラムを記録し、両者の強度比を求める。(注14)
(c) 定量:検出された各測定対象物質の定量用質量数および内標準物質のピーク面積またはピーク高さを求め、そのピーク面積またはピーク高さの比から、あらかじめ(2)により作成した検量線を用いて、注入した試料液中の各測定対象物質の重量(As:ng)を求める。(注15)
2) 操作ブランク試験:1.2.4の(2)の2)で調製した操作ブランク試験捕集管を試料導入装置に装着し、1)の操作を行って各測定対象物質の操作ブランク値を求める(注16)。
3) トラベルブランク試験:1.2.4の(2)の3)で調整したトラベルブランク試験捕集管について(1)の操作を行い、注入した試験液中の各測定対象物質の重量を測定する。本試験は3試料以上を測定し、平均値をトラベルブランク値(At:ng)とする。(注17)
4) GC/MS装置の感度試験:混合標準濃度系列の中から中間程度の濃度のものを選び、(1)の操作を行って感度の変動を確認する。この確認は1日に1回以上行う。(注18)
5) 2重測定:1.2.4の(2)の4)で調製した2重測定用試験液について(1)の操作を行って、各測定対象物質の重量を測定する。(注19)
(2) 検量線の作成
1) 混合標準捕集管系列の調製:1.2.2の(5)または(6)の標準溶液を用い、図1に示すように、検量線作成用T字管に高純度窒素ガス及び捕集管を連結し、高純度窒素ガスを20~50ml/minの流速で流しながら標準溶液の1~10μlを段階的に採り、捕集管の間近にマイクロシリンジを用いて注入し、さらに数分間通気して標準物質捕集管を調製する。同様の操作を数本について行い、混合標準捕集管系列を調製する。(注2)(注3)
2)測定:
(a) 測定:1)で調製した混合標準捕集管系列を試料導入装置に装着し、GC/MSを操作させる。1.2.3の(8)の1)のh)で設定した各測定対象物質の定量用質量数および確認用質量数各のクロマトグラムを記録する。
(b) 測定対象物質の確認:1)で調製した検量線用混合標準捕集管系列の中から各測定対象物質のGC/MSへの注入量が検量線の中間程度のものを選び、各測定対象物質毎に定量用質量数および確認用質量数のピーク面積またはピーク高さを用いて強度比を算出する。
(c) 測定対象物質の検量線作成用質量数の決定:混合標準捕集管系列毎に各測定対象物質の定量用質量数および確認用質量数の強度比を求め、(b)で求めた各測定対象物質毎の強度比と一致することを確認する。(注20)
(d) 検量線の作成:各測定対象物質の定量用質量数と内標準物質のピーク面積またはピーク高さの比を求め、そのピーク面積またはピーク高さの比と各測定対象物質の重量とにより検量線を作成する。
1.2.6.検出下限値、定量下限値の測定
検量線作成時の最低濃度(定量下限値付近)の混合標準濃度系列について、1.2.5の(1)の1)操作を行って測定値(A:ng)を求め、(As-At)にAを代入して、1.2.7の濃度の算出式より空気濃度を算出する。(但し、V=144l、t=20℃、P=101.3kPaとする)5試料以上を測定して求めた標準偏差(s)から次式により、各測定対象物質の検出下限値及び定量下限値を算出する。ただし、操作ブランク値のある物質では操作ブランク値を測定し、混合標準濃度系列と操作ブランク値のうち、大きい方の標準偏差を用いて計算する。(注31)
この測定は機器の分析条件を設定した場合など必要に応じて必ず1回以上行う。
1.2.7.濃度の算出
1.2.5の(1)で得られた結果から次式を用いて空気中の各測定対象物質の濃度を算出する。
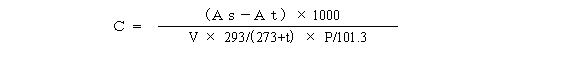
| C | : | 20℃における空気中の各測定対象物質の濃度 (mg/m3) |
| As | : | GC/MSに注入した試料中の各測定対象物質の重量(ng) |
| At | : | 各測定対象物質のトラベルブランク値(ng) 操作ブランク値と同等と見なせる場合は操作ブランク値を用いる。 |
| E | : | 試験液量(ml) |
| v | : | GC/MSへの注入液量(μl) |
| V | : | ガスメータで測定した捕集量(l) |
| t | : | 試料採取時の平均の気温(℃)。湿式型積算流量計を使用しているときには、積算流量計の平均水温(℃) |
| P | : | 試料採取時の平均大気圧(kPa)。湿式型積算流量計の場合には(P-Pw)を用いる。 ここで、Pwは試料採取時の平均気温tでの飽和水蒸気圧(kPa) |
測定結果については個々の値と各採取場所における平均値をそれぞれ記載する。
注 1:当方法は採取試料の前処理に溶媒を用いないため、前処理操作による溶媒、雰囲気等からの汚染を受けにくいという利点がある。一方、測定対象のフタル酸エステル類は高沸点で吸着を起こしやすい性質を持つため、加熱脱着装置内への吸着やクロスコンタミネーションに留意する必要がある。
注 2:試料採取量、濃縮操作及びGC/MSの条件等によって測定感度は異なるので、ここ に示した濃度を目安に適宜変えてもよい。
注 3:標準、内標の原液、溶液は市販品を用いてもよい。これらは精度保証されているものが望ましい。
注 4:精製空気を使用してもよい。有機化合物を含有しないことが重要であり、測定対象以外の物質については全炭化水素で0.01ppm以下、一酸化炭素0.05ppm以下、二酸化炭素0.3ppm以下、水分濃度2ppm以下(露点-70℃以下)で純度99.999%以上のものが望ましい。
注 5:バラツキが大きいのでマニホールドを使用すると良い。接続部分等についてはシールテープの使用は出来るだけ避け、テフロンコネクタ等を利用することが望ましい。
注 6:吸着剤としてはTenax TAやTenax GR等が利用できる。
注 7:試料導入装置には複数のタイプがあり、それぞれに最適条件を設定する。第1は、捕集管が試料導入装置に装着されると流路が確保され、加熱して脱着してトラップ管にいったん再捕集後、さらにトラップ管を加熱してクライオフォーカスに捕集し、さらに加熱してキャピラリーカラムに導入する方式である。第2には、捕集管が試料導入装置に装着されると流路が確保され、加熱して脱着してトラップ管またはクライオフォーカスに再捕集した後、いずれかを加熱してキャピラリーカラムに導入する方式である。
注 8:ガラス製または溶融シリカ製の中空管または吸着剤を充填したトラップ管では冷却を要しない装置もある。また、トラップ管の冷却、加熱条件等は導入装置毎に決定する必要がある。市販の装置ではこれらの条件は提示されている場合が多い。
注 9:トラップ管には石英等の不活性物質を詰めることもあるが、吸着剤を充てんする場合もある。その充てん剤は温度(-20℃程度の低温)でも破過を起こすことがあるので注意する必要がある。
注10:吸引側及び空気取り入れ側を明確にしておく。
注11:室外で塗装工事等が行われて室内より室外での化学物質濃度が高いと考えられる場合は、トラベルブランクは室外で行う。
注12:分析環境から試験操作過程で汚染されることがあるので、操作ブランクを一連の測定操作の中で少なくとも一回以上実施する。
注13:空気試料の測定に際して、その準備-機器の運搬-試料採取-持ち帰り-前処理-測定の過程で化学物質で汚染された空気で捕集管が暴露する可能性があるので試料採取時の記録を参考にして試験の頻度を考慮する。
注14:定量用質量数のピークに対する他イオンからの影響を判断するために行う操作であり、強度比が検量線作成時と大きくかけはなれている場合は、まず、装置の性能を確認するために再度標準試料を測定して強度比を算出する。その強度比が90~110%の範囲内であれば、測定済み試料のクロマトグラムのベースライン等を再検討し たり、かけ離れた原因をチェックして再分析を行い、その強度比が検量線作成時と大きくかけはなれないことを確認する。
注15:室内空気中の各対象化合物の濃度は範囲が広いことが予想されるため、定量上限を明確に把握しておくことが必要である。試料空気の測定値が作成した検量線の直線範囲からはずれている場合は、分析の諸条件を検討したうえで検量線を作成し直し、再度測定する。
注16:この操作は試料測定に先立って行い、操作ブランク値を大気濃度に換算した値が、目標定量下限値を超える場合には、再洗浄や機器の調製を行った後、再度測定し、操作ブランク値を十分低減してから試験液を測定する。
注17:測定対象物質のトラベルブランク値が操作ブランク値と同等(等しいか小さい)とみなせる場合には移送中の汚染は無視できるものとして試料の測定値から操作ブランク値を差し引いて濃度を計算する。移送中の汚染がある場合には、3試料以上のトラベルブランク値を測定した時の標準偏差(s)から求めた定量下限値(10s:大気濃度への換算値)が目標定量下限値以下の場合、およびトラベルブランク値による定量下限値が目標定量下限値より大きくても試料の測定値が、トラベルブランク値による定量下限値以上の場合には、試料の測定値からトラベルブランク値を差し引いて濃度を計算する。
しかし、移送中に汚染があり、またトラベルブランク値による定量下限値が目標定量下限値より大きく、しかも測定値がトラベルブランク値による定量下限値より小さい場合は原則として欠測扱いとする。この場合には、汚染の原因を取り除いた後、再度試料採取から行う。
注18:内標準物質の感度が検量線作成時の感度と大きく異ならないことを確認する。また、内標準物質との相対感度が検量線作成時の相対感度に対して±20%以内の変動であることを確認し、これを越えて感度が変動する場合には、その原因を取り除き、それ以前の試料を再測定する。さらに、保持時間については、比較的短い間に変動(通常、1日に保持時間が±5%以上、内標準物質との相対保持比が±2%以上)する場合には、その原因を取り除き、それ以前の試料の再測定を行う。
注19:定量下限値以上の濃度の測定対象物質に対して、測定値平均とそれぞれの測定値の間に±15%以上の開きがある場合は、原則として欠測扱いとして、その原因をチェックし、再度試料採取を行う。
注20:測定対象物質のいずれかの強度比が(b)で算出した90~110%の範囲を超える場合 は、その濃度の混合標準濃度系列を再度測定する。
注21:測定対象物質のいずれかの定量下限値が目標下限値より大きい場合には、試薬、器具、機器等をチェックして、目標定量下限値以下になるよう調整する。
*フタル酸エステル類の測定に係る注意事項
フタル酸エステル類は容易に環境からの汚染を受けるため、測定精度は、試料の採取、前処理、測定操作におけるフタル酸エステル類のブランクをいかに低くするかにかかっているといって過言ではない。試料採取、試験液調製、分析には細心の注意が必要である
。
精度の管理については各試験機関にて留意する必要があるが、汚染を防ぐ方策としてそれぞれの機関において現在までに何点かの試みが行われているので、以下に例示する。これらについては試行錯誤が継続している状態であり、今後さらに検討が必要な点が残されている。
[はじめに]
シックハウス(室内空気汚染)問題に関する検討会では、個別のVOCについて、国内外の知見に基づき、順次室内濃度指針値の策定を進めているところ。一方TVOCとは、複数のVOC混合物の濃度レベルのことであり、第3回検討会(2000年6月26日)においては、個別のVOCによる汚染を全体として低減させ、より快適な室内環境を実現するための補完的指標としての導入に向けて、TVOCの指針値の策定方法を検討することが必要とされた。
事務局では、これを受けて、OECD加盟29ヶ国及び欧州委員会に対し、TVOCの取扱状況等を調査したところ、20ヶ国から回答を得た。その多くは、TVOCの導入については未定か若しくは予定がないということであったが、いづれも日本における取り組みへの大きな期待を寄せていた。
一方、EC合同研究センターのような国際機関においては、以前からTVOC策定方法の例について発表してきており、今回の調査においても、その報告書が参考文献として提示されているケースが見られた。
今回の調査は各国行政庁への調査であり、必ずしも各国の民意と一致していることにはならない点に留意すべきである。実際我が国では、パブリックコメントで、TVOCの導入を強く求める意見が散見されている。一方、科学的知見が限られている中、TVOCの早期導入にはその影響を考えると問題があるとの意見も見られる。
これらを踏まえ、毒性学的知見に基づいたTVOC指針値設定は現時点では困難ではあるが、現時点で得られる室内VOC実態等の調査結果を最大限活用し、合理的に達成可能な範囲で、空気質の状態の目安としての暫定目標値と暫定策定方法を提示することは、室内空気質の状態を向上し、居住者の健康を確保する上で、有効であると考えられるのではないか、と判断した。
なお、TVOCについては、個別のVOCのリスク評価や混合毒性の評価、あるいは測定法での改良を待たないと、指針値としては明確には定められないことは明らかであり、今後の調査研究や海外での状況を把握しながら、必要な見直しをしていくことが必要である。
[要旨]
室内空気質のTVOC暫定目標値を 400μg/m3 とする。この数値は、国内家屋の室内VOC実態調査の結果から、ある仮定(2.参照)に基づいて、合理的に達成可能な限り低い範囲で決定した値であり、室内空気質の状態の目安として利用されることが期待される。TVOC暫定目標値は、毒性学的知見から決定したものではなく、含まれる物質の全てに健康影響が懸念されるわけではない。また、個別のVOC指針値とは独立に扱われなければならない。今後TVOCについては、実施される必要な調査研究によって、暫定目標値の妥当性の追跡とリスク評価に基づいた指針の策定が必要である。また発生源や換気に注意し、住宅の構造や日常の住まい方の改善によって、室内空気質の状態を向上させる取組みが不可欠である。
個別VOC指針値とTVOC暫定目標値について
個別VOC指針値はリスク評価に基づいた健康指針値であり、その濃度以下であれば通常の場合そのVOCは健康への悪影響は起さないと推定された値である。しかしその濃度以下であればその空気質が快適で安全ということでは決してなく、実際には複数のVOCsが存在することから、他のVOCについても順次健康指針値を決めていかなければならない。しかしそれには多大な時間を有すること、またその間に指針値を決めていない有害物質による汚染の進行を未然に防ぐ目的から、VOC全体としての空気中濃度の目安を示して、個別VOC指針値を補足することが重要であると判断した。その際、TVOCとしてのリスク評価を行うにはデータが不足していることから、国内における室内VOC濃度の実態調査の結果を用いて、合理的に達成可能な限り低い範囲において暫定目標値を決定した次第である。従って個別VOC指針値とTVOC暫定目標値は、現時点ではそれぞれ独立して扱われるべきものである。
将来リスク評価に基づくTVOC指針値が設定された場合には、個別VOC濃度とTVOC濃度の双方がそれぞれの指針値を満たしていないと、その空気質は安全であるとは言えない。従って、関係者においては、暫定目標値が将来指針値として設定し直されたときのことを今から念頭におくと同時に、その間、暫定目標値を室内空気質の状態をモニタリングする際の目安として、是非とも快適で安全な室内空間の確保を目指していっそうの努力をしていただきたい。
測定結果の評価方法について
この暫定目標値は、竣工後居住を開始してある程度時間が経過した状態における目安であって、竣工後入居してしばらくの間は、暫定目標値を超える場合も予測される。
またTVOCに含まれる物質の全てに健康影響が懸念される訳ではないこと、またその中には日常の居住環境で用いられる発生源に由来する物質が含まれることに留意すべきである。
従って、測定されたTVOC値が暫定目標値を超える結果が得られた場合には、測定時期や、その中に含まれる物質の種類や由来を確認した上で、個々の良否の評価を行うべきである。例えば、天然材を用いた住宅のような場合は、特定の天然成分が高濃度で測定される可能性が高いことから、特別な配慮が必要であろう。
この点は、本検討会中間報告書(2000年6月26日)において、背景因子の異なる個々の測定値と指針値との関係について更なる検討を進めることの重要性に言及している通りである。
1.OECD加盟国に対する調査結果の概要
1-1 TVOC又は個別のVOCについて指針値又はこれに類するものが設定若しくは検討されているか
オーストラリアでは、1992年に、健康状態に基づく基準により、TVOCを、単一の化合物が全体の50%を超えない範囲において、500μg/m3と勧告している。ただし個別のVOCの指針値を勧告するにはデータが不十分であり、TVOCが250~400μg/m3のレベルで呼吸器過敏症が報告されていることを指摘し、最新のデータを用いて新たな基準を設定すべきとしていた。現在、VOCに係る暴露モニタリング研究が実施されている他、2000年10月には、室内空気質に関する報告書の最終案をとりまとめる予定との回答であった。
ノルウェーでは、旧指針(1990年)でTVOCを400μg/m3としていたが、科学的データに基づくものではないので説得性に欠けており有効ではないとして、新指針(1999年)では削除され、個別のVOCの評価がなされている。
オーストリア及びドイツでは、TVOC及び個別のVOCに関する指針値設定に関して共同研究を進めており、そのガイドラインの草案が来年1月に出来上がる予定とのことであるが、現時点で具体的な設定方法の説明は困難との回答であった。
カナダでは、室内空気質ガイドラインにおいて、アルデヒド類等幾つかの個別のVOCについて指針値を定めている。TVOCに関する指針値策定の優先度は高くないが、将来考慮の対象になることはあり得るとしている。
ハンガリーでは、室内空気質の指標設定の努力がされているところではあるが、まだ承認に至っていないとの回答であった。
ポーランドでは、室内空気質の指標として、35の個別の化合物について基準が設けられているが、TVOCに関する指針値は設定されていない。
米国からは、室内空気質ガイドラインの検討はされていないが、将来の指標設定に不可欠な健康及び暴露に関する基礎調査を行っているところであるとの回答があった。
英国からの回答は、VOCsの健康影響について検討を行ったが、室内空気質の指針を示すには疫学的なデータが不十分であること、しかし平均的なTVOC濃度(0~1mg/m3)下で何らかの健康影響が認められた場合は家庭内のVOC発生源に注意し暴露の削減を図るべきと指摘している。具体的なスケジュールは未定であるが、今後指針の設定の検討を行うとの回答であった。
オランダからは、2000年5月の保健議会において、室内のVOCs濃度が0.2mg/m3を超えないことが望ましいこと、発がん性や生殖発生毒性並びに感作性を有する物質の建材への使用を避けることなどが勧告されている、との回答であった。
ECからは、環境総局としての検討は行っていないものの、EC共同研究センターにて室内空気質の研究が進められているとの回答であった。
TVOC及び個別のVOCに関する室内空気質の指針の設定若しくは検討がされていない、という回答の場合、その主たる背景は、人体への毒性影響が明確に立証されなければ指標の設定はできない(米、チェコ、ポルトガル)、室外大気中の濃度基準が存在する(EC、ニュージランド)、事業活動や職域あるいは建材等からの排出基準のほうが重要な課題である(EC、ニュージーランド、韓国、アイルランド、ポルトガル)、などであった。
1-2 TVOCに関する指針を考える上で、参考にできるような研究報告や文献等があるか
欧州委員会共同研究センター環境研究所による「室内空気質とヒトへの影響-報告書No.19:室内空気質の検討における総揮発性有機化合物(TVOC)(1997年)」("Indoor Air Quality & Its Impact on Man-Report No.19: Total Volatile Organic Compounds (TVOC) in Indoor Air Quality Investigations, European Commission Joint Research Center Environment Institute 1997")以外には、特に新たな知見は見い出せず、現時点では、この報告書が、TVOCの指針値策定の可能性を提供する唯一の文献と考えられる。
すなわち、この報告書では、TVOCの決定方法について、今までに報告されているTVOC値は、分析方法や個別のVOCの合計方法が異なるため、比較ができないとした上で、以下の実際的な手順を提案している。
TVOC決定手順の考え方
TVOCの決定には、次の3つを考慮すること。すなわち、
1.TVOC値を構成する個別の化合物が明確に定義されなければならない。
2.TVOC値は、採取空気中の全VOC濃度に出来る限り近いものとなるべきである。
3.TVOC値は、室内空気質の評価に出来る限り有益となる方法で構築されるべきである。
そのためには、次の要件を満たすこと。すなわち、
・採取空気中の出来る限り多くの化合物を同定すること、及び少なくとも検出上位10物質を同定すること
・TVOCの計算に含めるVOCsリスト。すなわち、
勧告手順
上記の考え方に従って、TVOC値の決定には、次の手順を勧告する。
1.空気の採取には、Tenax TA吸着体を使用する。同水準の吸着と脱着が確保できる場合は、他の吸着体を用いてもよい。
2.加熱脱着により、採取したVOCsを吸着体からGCカラムに移す。
3.分析には不活化された非極性のGCカラムを使用する。その分析システムは、トルエン及び2-ブトキシエタノールの検出限界をそれぞれ少なくとも0.5μg/m3、2.5μg/m3まで許容しなければならない。
4.クロマトグラムでは、n-ヘキサンからn-ヘキサデカンまでの部分に見つけられる化合物を考慮すること。
5.個別の検出ピークに基づいて、できるだけ多くのVOCを定量すること。その際には、少なくとも、別途示す必須VOCsリストに含まれる化合物及び検出上位10ピークにそれぞれ該当する化合物を定量すること。同定された各化合物の合計濃度Sidを計算する。
6.未同定の各VOCのピークについては、トルエンの検出量に換算して、合計濃度Sunを決定する。
7.手順5及び6の結果、SidがSid+Sunの合計の2/3量に達していれば、VOCsの特定は許容できる水準にあると言える。 Sid+Sunの合計が1mg/m3未満のときは、SidがSid+Sunの合計の1/2量に達していれば十分である。
8.Sid+Sunの合計がTVOC値と定義される。
9.たくさんの化合物ピークが手順4で示したVOC範囲の外に観察される場合は、その旨注釈を付けること。
なお、上記の手順で決定されたTVOC値は、室内空気中の全VOCを含む訳ではないことに留意すべきである。TVOC値には反映されない、室内空気質に深く係る汚染物質が存在する。特に低分子のアルデヒド類はその代表例で、通常、TVOCとは別途、望ましくはDNPH法を用いて測定される。
必須VOCsリスト
○芳香族炭化水素
ベンゼン、トルエン、エチルベンゼン、キシレン、n-プロピルベンゼン、
1,2,4-トリメチルベンゼン、1,3,5-トリメチルベンゼン、2-エチルトルエン、
スチレン、ナフタレン、4-フェニルシクロヘキセン
○脂肪族炭化水素(n-C6~C16)
n-ヘキサン、n-ヘプタン、n-オクタン、n-ノナン、n-デカン、n-ウンデカン、
n-ドデカン、n-トリデカン、n-テトラデカン、n-ペンタデカン、
n-ヘキサデカン、2-メチルペンタン、3-メチルペンタン、1-オクテン、
1-デセン
○環状アルカン
メチルシクロペンタン、シクロヘキサン、メチルシクロヘキサン
○テルペン
3-カレン、α-ピネン、β-ピネン、リモネン
○アルコール
2-プロパノール、1-ブタノール、2-エチル-1-ヘキサノール
○グリコール/グリコールエーテル
2-メトキシエタノール、2-エトキシエタノール、2-ブトキシエタノール、
1-メトキシ-2-プロパノール、2-ブトキシエトキシエタノール
○アルデヒド
ブタナール、ペンタナール、ヘキサナール、ノナナール、ベンズアルデヒド
○ケトン
メチルエチルケトン、メチルイソブチルケトン、シクロヘキサノン、アセトフェノン
○ハロゲン化炭化水素
トリクロロエチレン、テトラクロロエチレン、1,1,1-トリクロロエタン、1,4-ジクロロベンゼン
○酸
ヘキサン酸
○エステル
酢酸エチル、酢酸ブチル、酢酸イソプロピル、酢酸2-エトキシエチル、テキサノールイソブチレート
○その他
2-ペンチルフラン、テトラヒドロフラン
上記の報告書によれば、VOC混合物のリスク評価について、VOC混合物による暴露実験や疫学的な調査による幾つかの試みがなされているものの、TVOCと健康影響の首尾一貫した関係は未だ明かにされておらず、TVOCに係る明確な指針は存在しないとして、ALARA(as low as reasonably achievable: 合理的に達成可能な限り低く)の原則を勧告している。
そして、VOC混合物の暴露-効果関係に係るより多くの情報と注意深くデザインされた疫学研究の必要性を指摘し、その結果として、例えば個別のVOCの生物反応性に基づく加重補正値を合計するような、より優れたモデルが確立される可能性を示唆している。
また、本報告書の中では、TVOC決定の新しい勧告手順に先立って、従来利用されている、個別検出ピークの同定は行わない、水素炎イオン化法(FID)などの直接読取法によるTVOC測定法を紹介している。この方法は、ある1物質(通常はトルエンかn-ヘキサン)についてのみ補正を行って、全ピークをその物質換算値に置き換えてTVOCを算出する方法である。この方法は、上記の勧告手順の中で、未同定ピークの定量にも利用することができる方法である。
両方法によって得られるTVOCはそれぞれ意味が異なるので、いくつかのサンプルを用いて両者の関係を検証しなければ、単純な数値の比較はできない。これを踏まえ、報告書では、例えば、この直接読取法をスクリーニング目的で使用して、ある一定以上の数値が得られた場合には、新しい勧告手順に従って詳細な分析を行うやり方を勧めている。
なお、本報告書の中では、これまで室内空気中のTVOCに係る指針の設定について、TVOCの定義と方法の異なる以下の2通りのアプローチが提案されたことを紹介している。
Molhave (1990) の方法
空気質毒性の健康影響に関する文献値から、影響が増す順に4段階の暴露レベル(測定はGC/FID)を示唆した。すなわち、快適レベル(<0.2mg/m3)、多因子性暴露レベル(0.2~3mg/m3)、不快レベル(3~25mg/m3)、毒性レベル(>25mg/m3)。
Seifert (1990) の方法
ドイツの家屋を対象にした実地試験の経験から、TVOCの上限値を推測した。すなわち、実地試験の平均値である300μg/m3が容易に達成可能なレベルであるので、これを超えないものとした。またこのTVOCを異なる化学分類に割り振る場合は、次の通りとした。脂肪族炭化水素100μg/m3、芳香族炭化水素50μg/m3、テルペン30μg/m3、ハロゲン化炭化水素30μg/m3、エステル20μg/m3、アルデヒド/ケトン(ホルムアルデヒドを除く)20μg/m3、その他50μg/m3。さらに個別のVOC濃度に関して、該当する化学分類の平均値の50%を超えているVOCが存在しないこと、及び測定されたTVOC値の10%を超えるVOCが存在しないこと、とした。これらの数値は、全て、毒性学的データから求めたものではなく、合理的に達成可能なレベルとして判断されたものである。
2.TVOC指針値策定の可能性とその方法
現時点で得られている情報から、TVOCの指針値(暫定値)設定のアプローチをするとした場合、少なくとも下記の手順を踏むことが必要となる。
・実態調査における測定値(例えば中央値)に基づき、合理的に達成可能なレベルを設定すること
・測定の際には、日本版の必須VOCsリストを準備すること
・リスト化された物質については、標準的な測定法が存在すること
そこで、1-2で示された手順に沿って、厚生省の「居住環境内における揮発性有機化合物の全国実態調査」の結果をもとにシミュレーションをしてみると、以下の通りとなる。
2-1 調査時の測定対象物質とSidの計算
調査時の測定対象物質リスト
(芳香族炭化水素)
ベンゼン、トルエン、エチルベンゼン、キシレン、スチレン、
1,2,4-トリメチルベンゼン、1,3,5-トリメチルベンゼン、
1,2,3-トリメチルベンゼン、1,2,4,5-テトラメチルベンゼン
(脂肪族炭化水素)
n-ヘキサン、n-ヘプタン、n-オクタン、n-ノナン、n-デカン、n-ウンデカン、
n-ドデカン、n-トリデカン、n-テトラデカン、n-ペンタデカン、
n-ヘキサデカン、2,4,-ジメチルペンタン、2,2,4-トリメチルペンタン
α-ピネン、リモネン
(オキシ化炭化水素)
1-ブタノール、ノナナール、デカナール、メチルエチルケトン、メチルイソブチルケトン
(ハロゲン化炭化水素)
トリクロロエチレン、テトラクロロエチレン、1,1,1-トリクロロエタン、
1,4-ジクロロベンゼン、クロロホルム、1,2-ジクロロエタン、
1,2-ジクロロプロパン、四塩化炭素、クロロジブロモメタン
(その他)
酢酸エチル、酢酸ブチル
Sidの計算
本調査では、全家屋数205戸に対し、新築住宅を竣工後1又は3ヶ月以内の建物、それ以外を中古住宅と定義して、いづれの場合も、居住・平常時の24時間連続空気採取にて行われたものであり、室内空気200試料を採取、41VOCsについて濃度測定(n=177~201)を行っている。その結果は、対象家屋全体の物質毎の実測値データとしてとりまとめられており、各物質濃度の中央値が求められている。またいくつかの背景因子別(新築/中古、夏/冬、症状あり/なし)に層別解析した場合の物質毎の実測値データもまとめられており、同様に各物質濃度の中央値が求められている。
TVOCの計算では、個別の調査家屋のチャートを再解析する必要があるが、ここでは、便宜上、既にとりまとめられた物質ごとの測定データを用いて算出する。
実態調査における各VOC濃度の実測値分布は、全般的に低濃度領域に大きな母集団があり、高濃度領域にいくつかの特別に高濃度の汚染事例が散見する分布を示したことから、合理的に達成可能な限り低い範囲でTVOC値を決定するには、分布上、より真の平均に近いと考えられる中央値を用いることによって、算出することとした。
下記の表は、これら中央値の総和を示したものである。
| 特定VOC濃度の中央値の総和(Sid) | 153μg/m3 |
| 新築1ヶ月 新築3ヶ月 中古1ヶ月 中古3ヶ月 夏の場合 冬の場合 症状なし 症状あり |
436 468 178 165 134 175 154 157 |
2-2 Sun及びTVOC(=Sid+Sun)の計算
未同定VOC量Sunについては、元のチャートを再解析しないと推測できないが、ここでは便宜上、Sid+Sunが1mg/m3未満であると想定すると、SidはSid+Sunの1/2量でよいことになる。TVOC(=Sid+Sun)を計算すると、下記の表の通りとなった。
| TVOC(=Sid+Sun) | 306μg/m3 |
| 新築1ヶ月 新築3ヶ月 中古1ヶ月 中古3ヶ月 夏の場合 冬の場合 症状なし 症状あり |
872 936 356 330 268 350 308 314 |
算出された数値は、200~400μg/m3の間(特に中古1ヶ月の場合で356μg/m3、冬の場合で350μg/m3)にあることから、TVOC暫定目標値を、以下の通りとした。
| TVOC暫定目標値 | 400 μg/m3 |
3.今後の進め方
上記のTVOC暫定目標値は、限られたデータからの仮定に基づいて算定された数値であり、そのTVOCの構成は、採取空気の構成に近いものとは言えない。しかし、一定の目安を与えることは、快適な室内空間の確保に一役を買うものと期待する。今後以下の検討を進めて、より採取空気の構成に近い必須VOCsリストの作成、健康影響が起こりうるTVOC濃度域の調査とTVOCリスク評価に基づく指針の策定をしなければならない。
・本格的TVOC実態調査の実施(健康影響調査も同時)。必須VOCsリストの完成(特に、グリコール、環状アルカン、フラン体、低分子アルデヒド類、有機リン系化合物、フタル酸エステル類の追加等。VVOCs(Very Volatile Organic Compounds)、SVOCs(Semi-volatile Organic Compounds)の区別を含む)。健康影響が起こるTVOC濃度域の特定とTVOCのリスク評価。TVOC指針値の策定。
・詳細な測定手順の作成。既存標準測定法の測定範囲の特定。その方法ではカバーできない物質の測定法の確立。
・TVOCを化学分類に割り振った場合の生物反応性に基づく加重の方法の調査研究。各化学分類の目標値及び指針値の策定。
・継続的なモニタリングによる、TVOC目標値/指針値の見直し。
なお、詳細なTVOC測定手順を作成・公表するまでの間、現時点のスキームは、1-2で紹介した欧州委員会共同研究センターの報告書による勧告手順を参考にし、以下の通りとしたい。
採取と分離
・本検討会中間報告書-第1回~第3回のまとめ(平成12年6月26日)にて策定した、室内空気中化学物質の採取方法に基本的に従う。少なくとも2本の捕集管に空気を採取する。
検出と定量
・まず、TVOC値のスクリーニングのために直接読取法にて、指定範囲内のピーク面積をトルエン換算値として求める。スクリーニングにて暫定目標値を超過するような場合は、GC/MS法により出来る限り個別物質の同定及び定量を行う。
・定量した物質に相当するチャート上のピークのトルエン換算値を差し引き、代わりに厳密に定量した値を加える。この定量値の合計をTVOCとする。
・同定すべき個別物質については暫定的にリストに掲載されているが、実態調査を含め、現在精査・検討中である。
同定が必要なVOCの代表例
・芳香族炭化水素:トルエン、エチルベンゼン、キシレン、スチレンなど
・脂肪族炭化水素: ノナン、デカン、トリデカン、テトラデカンなど
・オキシ化炭化水素:1-ブタノール、ノナナール、メチルエチルケトンなど
・ハロゲン化炭化水素:トリクロロエチレン、1,1,1-トリクロロエタンなど
・その他:酢酸エチル、酢酸ブチルなど
| 報道発表資料 | HOME |