III.本 論
1.意義及び目的について
厚生省が先に示した「第六次改定日本人の栄養所要量-食事摂取基準-」は、栄養素欠乏症から遠ざかり、栄養素過剰症からも遠ざかって、よりよい栄養状態を維持し、健康を増進する上での基準となるものである。しかし、適切な栄養摂取は、その人の身体状況、生活状況等により異なる。このため、いわゆる栄養補助食品については、適切な栄養摂取を補助することにより、国民の健康の維持増進を図る上で有意義であるとして、積極的に評価すべき一面がある。また、さらには、一部の栄養成分には、通常の食生活からは期待することが困難な、健康を維持増進させる働きも期待されている。
一方、健康を維持増進するためには、バランスが取れた食事が基本であり、可能な限り必要なすべての栄養成分を普通の食事から摂取すべきであって、いわゆる栄養補助食品の普及によって、これがないがしろにされてはならないことも考慮すべきである。このため、栄養補助食品の意義あるいは目的を明らかにすることにより、このような適切かつ安全な摂取を促す必要がある。
他方、規制緩和の流れの中で、これまで医薬品として使用されていたビタミン等の錠剤等を、適切な表示を認めながら、食品としても流通できるようにすべきとの方向性は固まっており、また、既に栄養補助食品等と称して、機能の表示が許されないままに、ビタミン、ミネラル、ハーブ類等の錠剤等の形状の食品が流通していることから、これらについて、適切な類型区分を行い、表示についての適切なルールを設けることも、その適切かつ安全な摂取の上で必要となっている。
以上のことを念頭におきつつ、当該食品の意義、目的については、
- (1) 高齢化、食生活の乱れ等により通常の食生活を行うことが困難な場合等に、不足しがちな栄養成分を補給する食品として、国民生活上の意義、目的があること
すなわち、栄養の補給・補完としての意義、目的と、
- (2) 通常の食生活における栄養摂取量からは期待することが困難な、一部栄養成分について明らかにされつつある身体の機能や構造に影響を与え健康を維持増進させる働きを評価し、その栄養成分の働きに着眼した栄養補助食品として、生活の質(QOL)の向上を図るとともに、国民の健康の維持増進を図るという意義、目的があること
すなわち、QOLの向上、健康の維持増進としての意義、目的
について、積極的に評価すべきである。
なお、QOLの向上、健康の維持増進に関連して、生活習慣病等の罹患リスクの軽減(リスク・リダクション)という観点も、合わせて考慮すべきであるとの意見もあった。
-
(注)「栄養成分」とは、食品に本来含有される成分で、人体で利用されるものをいい、本報告書では、栄養素のほかハーブ等に含まれる成分等を含めた広い意味に用いる。
2.定義について
一般的な意味での栄養補助食品の定義としては、
「栄養成分を補給し、又は特別の保健の用途に資するものとして販売の用に供する食品のうち、錠剤、カプセル等通常の食品の形態でないもの」
などと表現することが適切であると考えられる。
3.範囲について
栄養補助食品の範囲としては、ビタミン、ミネラル、ハーブその他の栄養成分に及ぶが、安全性の確立していない成分を食品として用いることができないことは当然であり、また、栄養成分の機能等の表示も、人において科学的に証明できている場合に限定されることも当然である。
4.名称について
名称については、日常生活では不足しがちな、又は健康の維持増進のために意義のある栄養成分を補給するものであり、さらに、通常の形態の食品に対して補助的であるという位置付けにふさわしい名称として、既に一般的な使用例が多くなっている「栄養補助食品」の名称を総称として用いる。
5.表示について
(1)表示の意義
栄養補助食品の適切な選択や摂取を行う上では、消費者に対し適切な情報を提供する必要があり、表示の基準を適切に設定する必要がある。
表示の内容は、該当するすべての食品に対し表示が義務付けられる「義務表示」と、表示を行うか否かは表示者の任意である「任意表示」があり、次のとおりとすることが適当である。
- (1)義務表示
- ・栄養補助食品の類型を示す表示
・栄養成分の表示
・過剰摂取等に対する注意喚起表示
・品質保持期限に関する表示
- (2)任意表示
- ・栄養成分機能表示、特定保健用途の表示
(2)類型名の表示
栄養補助食品は、医薬品等との誤認を与えないよう、食品である旨の表示が必要である。
さらに、栄養補助食品としては、
- (1)科学的な審査を経て特定の保健用途の表示を行うもの
- (2)科学的に証明された栄養成分の機能の表示を行うもの
といった類型になる。こうした栄養補助食品について、国民に正しい情報が提供されるよう、これらについては、類型の名称の表示を義務付けることが適当である。
(3)栄養成分に関わる表示
- (1)栄養成分含有表示
- 当該食品が当該栄養成分を含むことの表示。この場合、食品中の栄養成分含有量の多い少ないを表示する場合もある。
- 例:「この食品はカルシウムを多く含みます。」
- (2)栄養成分機能表示
- 当該栄養成分の機能についての表示。身体の成長、発達、正常な機能における栄養成分の生理的な役割を表示するもの。
なお、その機能は、人において科学的な根拠で証明されたものでなければならない。また、その表現に当たっては、消費者に当該食品への正しい理解を促進するために、疾病に言及し疾病の診断・治療又は予防を目的とする旨を表示しない範囲において、できるだけ分かりやすい表示を行うべきである。
- 例:「カルシウムは、歯や骨を丈夫にします。」
- (3)保健用途の表示
- 当該食品が健康の維持増進に役立ち、特定の保健の用途に適することの表示。食品に着目した表示。
なお、その機能は、人において科学的な根拠で証明されたものでなければならない。また、その表現に当たっては、消費者に当該食品への正しい理解を促進するために、疾病に言及し疾病の診断・治療又は予防を目的とする旨を表示しない範囲において、できるだけ分かりやすい表示を行うべきである。
- 例:「この食品は、吸収の良いカルシウムを多く含み、歯や骨を丈夫にし、健康の維持増進に役立ちます。」
- (4)疾病リスク低減表示(リスクリダクション表示)
- 特定の疾病罹患リスクの低減ができる旨の表示。
- 例:「この食品は、カルシウムを多く含み、将来の骨粗鬆症の危険度を減らします。」
- 厚生省の「第六次改定日本人の栄養所要量-食事摂取基準-」にあるとおり、健康の維持増進や生活習慣病の予防に果たす適切な食事の役割は大きい。しかし、食品における疾病リスク低減表示については、その概念や表示の在り方は未だ検討途上であり、また、医薬品的効能効果である疾病の予防効果の表示と区別が付きにくいとの意見もあることから、本検討会で結論を得るには時期尚早と考えられる。
なお、食事を通じた健康の維持増進や生活習慣病の予防の重要性にかんがみ、また、現在、コーデックス食品表示部会において検討されている「健康強調表示の使用に関する勧告案」でも、疾病リスク低減表示を含めて検討がされていることから、その動向をも踏まえつつ、この問題については引き続き検討を進める必要がある。
(4)注意喚起表示
- (1)過剰摂取に対する注意喚起表示
- 当該食品は、過剰摂取により健康危害をもたらすおそれのある栄養成分を高単位で含むものもあることから、過剰摂取に対する注意喚起表示として、
- 過剰摂取による危害発生が明らかな成分に関しては、具体的な過剰摂取による症状の表示
- を義務付けることとする。
- ただし、成分によっては、過剰摂取による症状が一つに特定できない場合や、摂取量、年齢・性別等により症状が異なる場合などがあることから、個別成分毎に表示方法を検討することが適切である。
- (2)一日当たりの摂取量の目安
- 当該食品は、医薬品ではないことから、医薬品的な用法用量の表示は適切でないが、過剰摂取を防止し、また、含有栄養成分が効果的に吸収されることを図るため、
- 一日当たりの摂取量の目安、及び、適切な摂取方法の表示
- を義務付けることが必要である。
- また、あわせて、一日当たりの栄養所要量が示されている栄養成分を含有する場合は、
- 一日当たりの栄養所要量に対する摂取割合の表示
- を義務付けることが必要である。
なお、その場合、栄養所要量が年齢、性別で異なることにも対応できる表示を行えるような方法を考慮することが望ましい。
- (3)その他注意喚起表示
- 当該食品が含有する成分によっては、特定の人(妊婦や子供、特定の医薬品を服用している人など)にとって摂取が危険である場合もあることから、このような危険事項に関する表示も義務付ける必要がある。
また、他の栄養補助食品や通常の食品とのいわゆる「食べ合わせ」などの摂取上の注意事項もあわせて表示する必要がある。
なお、これとあわせて、「健康を維持増進するためには、バランスのとれた食事をすることが基本である」旨も表示すべきとの意見もあった。
(5)品質保持期限に関する表示
栄養補助食品に含まれる成分には、長期の保存に伴い品質が変化するものもあることから、品質保持期限についても義務表示とする必要がある。
(6)表示制度の法的枠組み ※本項では適宜記述順序を変更した
- (1)食品衛生法の表示制度と栄養改善法の表示制度
- 栄養補助食品は、摂取の方法等によっては、健康に危害を生じたり、あるいは、健康に良い影響を期待しながらそれを得られないなどの問題が生じることから、「飲食に起因する衛生上の危害の発生を防止し、公衆衛生の向上及び増進に寄与する」ことを目的とする食品衛生法の表示制度を根拠とすることが適切である。
とりわけ、栄養補助食品に用いられる成分の個別審査や、各種の注意喚起表示や、摂取量の目安等は、健康被害の防止のために重要なものであるから、食品衛生法に根拠を置くことが適当である。
- ○食品衛生法第11条(食品の表示の基準)
- 「厚生大臣は、公衆衛生の見地から、販売の用に供する食品若しくは添加物に関する表示につき、必要な基準を定めることができる。」
- また、栄養補助食品には、栄養の補給・補完ないしは健康の維持増進の意義があることを考えると、「国民の栄養を改善する方途を講じて国民の健康及び体力の維持向上を図ること」を目的とする栄養改善法の表示制度の適用を受けることも必要である。
- ○栄養改善法第12条(特別用途表示の許可)
- 「販売の用に供する食品につき、乳児用、幼児用、妊産婦用、病者用等の特別の用途に適する旨の表示(以下「特別用途表示」という。)をしようとする者は、厚生大臣の許可を受けなければならない。」
- *同法施行規則第8条第1項第5号において、「食生活において特定の保健の目的で摂取をする者に対し、 その摂取により当該保健の目的が期待できる旨の表示をするもの(以下「特定保健用食品」という。)」
- とされており、特定保健用途の表示を行う場合には、厚生大臣の許可が必要とされている。
- ○栄養改善法第17条(栄養表示基準)
- 「販売に供する食品につき、栄養成分(厚生省令で定めるものに限る。)又は熱量に関する表示(以下「栄養表示」という。)をしようとする者は、厚生大臣の定める栄養表示基準に従い、必要な表示をしなければならない。」
- 従って、栄養補助食品の表示については、食品衛生法と栄養改善法の両法の表示制度に基づくものとして検討することが適当と考えられる。
- (2)個別許可型(特定保健用食品)と規格基準型(栄養機能食品)
- ア.個別許可型
- 栄養補助食品に保健の用途の表示を行うためには、食品衛生法において、個別に審査して安全性及び保健の用途を確認して、保健用途の表示を認める仕組みが適当である。また、栄養改善法においても、特定用途表示の許可が必要であり、これまで、錠剤やカプセル形状の特定保健用食品の許可は行ってこなかったが、この規定は、食品である以上、錠剤やカプセル形状の栄養補助食品にも当然に適用されるものであり、保健用途の表示を行うためには、厚生大臣の許可が必要となる。この個別許可型の場合、保健用途の表示及び栄養成分の機能表示が許される。
なお、「特定保健用食品」については、当初から名称が分かりにくいとの指摘もあり、これを契機に、「保健機能食品」あるいは「健康機能食品」などの消費者にとって分かりやすい名称に改めてはどうかという考え方がある。一方、制度化以来、定着に努力してきた名称であるので、変更は適当でないとの考え方もあり、詳細を具体化するまでに十分検討すべきである。
- イ.規格基準型
- 一方、個別許可でなくとも、(3)(2)の栄養成分機能表示については、規格基準の設定により、認めうる。
この場合、表示する栄養成分の機能は、人において科学的な根拠で証明されたものでなければならないことから、食品衛生法の表示基準において、ポジティブリストにより表示可能な個別事項を列挙し、栄養成分機能表示を行うことができる栄養成分の種類と、表示できる機能の内容を規制することが適当である。
この類型の名称としては、栄養成分の機能を表示する食品であることから、「栄養機能食品」とするなど、国民に分かりやすい適切な名称を検討することが望ましい。なお、個別許可型と名称は分けなくてもよいのではないかという考え方もあり、検討が必要である。
- 規格基準型に該当する栄養成分としては、当初は、日本人の栄養所要量における一日当たりの適正摂取量が示されているビタミン、ミネラル等が中心となることが予想される。多様なハーブ類については、その機能の科学的根拠による証明が未だ不十分である場合が多く、その場合は、当面、栄養成分機能表示は認められず、(3)(1)の栄養成分含有表示のみが許されることとなる。
ただし、当該成分の機能の科学的証明ができていない場合でも、当該成分を含む個別の食品について、その機能の科学的根拠が示されれば、上記の個別許可型の制度を活用して、栄養成分の機能の表示ができる。
(7)食品への具体的な表示方法
商品によっては、上記の表示をすべて行うには物理的スペースに限りがある場合がある。
この場合には、商品選択の上で必要な表示(例:危険に関する表示、栄養成分機能表示等)については、外包に表示するとともに、摂取の上で留意すべき表示(例:過剰摂取に関する注意喚起表示)については、添付書に表示するなどの工夫が必要である。
(8)虚偽又は誇大な表示又は広告の規制
栄養補助食品の信頼を確保するためには、虚偽又は誇大な表示又は広告の規制が重要である。
このため、食品衛生法第12条(虚偽表示等の禁止)において、
- 「食品、添加物、器具又は容器包装に関しては、公衆衛生に危害を及ぼす虞がある虚偽の又は誇大な表示又は広告はこれを行ってはならない。」
とされており、この規定等を適切に運用し、適切な措置を講じることが必要である。
6.安全性の確保について
栄養補助食品も食品である以上、安全性の確保は、何よりも重要であり、食品衛生法の以下の制度について、適切な運用が必要である。
(1)食品成分の規格基準及び食品添加物規制
ビタミン、ミネラルは、過剰摂取により健康被害を生じるおそれがあり、また、ハーブ等についても、安全な食経験に乏しい植物等が使用されるおそれもある。
このため、食品衛生法の規格基準において、錠剤、カプセル等の形状の食品として用いられる成分の規制を行い、安全性を確保することが必要である。
一方、錠剤、カプセル等を形作る材料等、食品添加物の規制が適用される物質については、必要に応じて新規の添加物指定や、使用基準の設定など、制度の適切な運用を行いながら、安全性を確保していくことが必要である。
なお、食品衛生調査会毒性・添加物合同部会では、栄養補助食品に係る食品添加物規制の在り方の概要を、次のようにまとめている。
- (1)栄養補助食品に栄養成分として用いられるものについては、これまでの食品添加物規制とは異なった位置付けとなることは差し支えない。食品成分として取り扱うとしても、品質や安全性を確保するため、栄養成分のうち少なくとも化学的合成品(精製等により通常の食品と成分比率が異なっているものを含む。)については、厳格な審査の必要性が高いものと考えられ、食品添加物と同等の規格を適用することが適切である。また、使用基準についても所要の措置を講じるべきである。
- (2) 個別許可型又は規格基準型の栄養補助食品に用いられるビタミン類、ミネラル類等を新たに指定する場合には、審査の際の一部の資料を省略することができるが、これは別枠リストとして指定すべきである。
- (3) 通常の食品にビタミン類、ミネラル類等の栄養成分を用いる場合には、従来通り取り扱うことが適切である。
- (4) 栄養補助食品に用いられる賦形剤、乳化剤など非有効成分については、食品添加物として取り扱うことが適切である。当該物質の中で、新たに指定する必要があり、我が国で医薬品に対して用いられてきたものについては、評価の際に医薬品としての使用実績や毒性試験結果等を考慮し、審査の際に一部の資料を省略することができるが、これは、別枠リストとして指定するとともに、個別の使用基準を定めるべきである。
- (5) 栄養補助食品に用いられる有効成分及び非有効成分についての具体的な検討は、個別の物質で行う必要があり、今後専門的な分科会を本合同部会に設置し、検討する必要がある。
(2)食品衛生法に基づく製造基準(食品GMP)の設定について
- (1) 栄養補助食品のように、栄養成分を人為的に調整して製造される食品については、安全性の確保のためには、適切な製造管理・品質管理が重要である。
また、ビタミン、ミネラル、ハーブ等の栄養成分の中には、過剰摂取により健康被害のおそれがあるものがあり、また、栄養成分の機能の観点からも、栄養補助食品等には、摂取量の目安の表示を義務付けることとされているが、これを目安に一定の摂取量をとることができるようにするためにも、製品の品質の一定性が重要であり、適切な製造管理・品質管理が重要である。
このような公衆衛生上の観点から、これらの類型の食品には、食品衛生法第7条に基づく製造基準において、食品GMP制度による製造基準を義務付けることが適切と考えられる。
- (2) なお、この場合、個別許可型又は規格基準型以外のいわゆるその他の健康食品については、機能についての科学的根拠が明確でなく、機能成分に着目した製造管理を義務付ける根拠が必ずしも明確でないことから、当面、食品GMP制度は、個別許可型及び規格基準型のものに限って義務付けることが適当と考えられる。
(3)施設基準及び営業許可について
上記の製造基準(食品GMP)を適用する場合、製造に際して栄養成分の量を制御することが必須であるため、一般的な食品の衛生管理を担保するための構造設備のほかに、栄養成分制御の目的で一定の構造設備を備えることを要する。
従って、これらの類型の健康食品の製造施設にあっては、食品衛生法第20条に基づく施設基準を設定することが適切である。
なお、施設基準を設定した業種については、法第21条の規定による都道府県知事の営業許可が必要となるが、当該営業許可制度は、この製造基準(食品GMP)を都道府県が効果的に監視指導していく上で有効な制度であると考えられる。
7.監視、情報提供及び相談指導について
(1)監視制度
栄養補助食品については、その安全性の確保や、表示のルールの遵守徹底のため、監視制度の適切な運用が必要である。
食品衛生法では、規格基準、表示基準、営業規制の監視については、報告徴収、立入検査、収去など、行政機関の食品衛生監視員等による監視制度が設けられている。
また、栄養改善法においても、特別用途表示許可制度や栄養表示基準の実施のため、監視制度が設けられている。
(2)消費者への情報提供、相談指導
消費者が適切かつ安全に栄養補助食品を摂取するためには、この制度の意義が正しく消費者に理解されることが重要である。また、この食品は、消費者が各人の食生活を十分理解した上で適切に摂取することにより、初めてその効果が得られるものである。
したがって、消費者がこれらの食品を選択する際の適切な情報提供やアドバイス方法について、具体策を検討していく必要がある。
8.いわゆる健康食品全体の類型について
(1)いわゆる健康食品全体の類型化
本検討会では、「栄養成分を補給し、又は特別の保健の用途に資するものとして販売の用に供する食品のうち、錠剤、カプセル等の通常の食品の形態でないもの」を、一般的な用語として「栄養補助食品」ということが適当(8ページ「2.定義について」参照)としたが、この定義の前段の「栄養成分を補給し、又は特別の保健の用途に資するものとして販売の用に供する食品」は、通常の食品の形態である食品も含めたものであり、「健康食品」と呼ばれるものである。(この概念は、これまで、「健康食品の摂取量及び摂取方法の表示に関する指針」(昭和63年11月30日付厚生省生活衛生局長通知)等において使われてきている。)
本検討会は、錠剤等の形状の栄養補助食品について検討してきたが、個別許可型(特定保健用食品)と規格基準型(栄養機能食品)等についての取扱いは、添加物規制等の考え方の一部を除き、大部分が、通常形態の食品と、錠剤等の形態の食品とで区別をせずに、共通の制度が適用可能と考えられる。
そこで、その健康食品全体の類型としては、次の図のとおりに整理することができる。
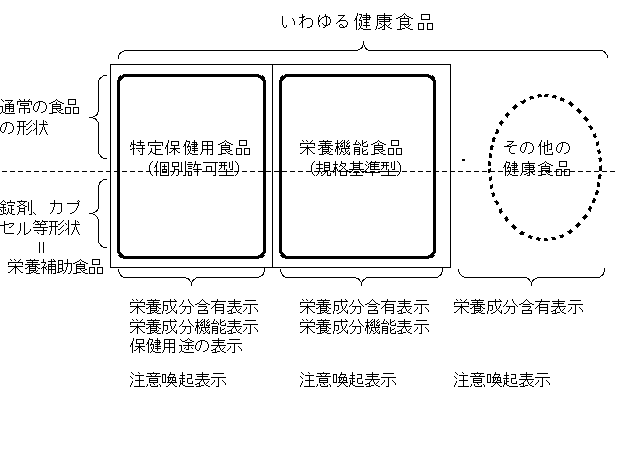
(注)特定保健用食品、栄養機能食品の名称については、引き続き検討。
(2)通常の食品形態である栄養機能食品について
近年、栄養調整食品などの名称で、シリアルやビスケット状等通常の形状をした食品であって、ビタミン、ミネラル等の栄養成分を強化した食品が広く販売されている。
このような食品については、その摂取の目的からみて、「栄養補助食品」の範疇に含めることは適当ではないが、錠剤等の形態の食品について栄養成分の機能の表示を認めるのであれば、これらの食品についても、栄養成分の機能の表示を認めることが適当である。
また、特定栄養成分の過剰摂取等の注意喚起表示も必要であり、適切な栄養摂取バランスを考慮できるよう、個々の栄養成分に関する表示の基準を定めることにより、消費者の商品選択に資するものであること等から、規格基準型の「栄養機能食品」の制度を適用し、通常の食品の形態の栄養機能食品にふさわしい基準を設定すべきである。
(3)その他の健康食品について
現在、健康の維持増進等に有効であると期待され、あるいは称される様々な食品が、いわゆる健康食品として販売されており、これらについては、身体の機能等に及ぼす働き等の表示は認められていないが、「健康食品の摂取量及び摂取方法の表示に関する指針」(昭和63年厚生省生活衛生局長通知)、「健康食品の表示等に関する指針」(平成元年厚生省生活衛生局長通知)により、適正な摂取についての注意喚起表示を行うことや、誇大な表示、医薬品と紛らわしい表示を行わないよう定められている。
また、現在、国の認可を受けた公益法人の中には、消費者の適切な選択に資するため、これらの健康食品の種類ごとに、安全性と品質の面から、独自の基準を定めて、認証マークを交付している法人がある。
今後、本報告書による制度が実施された場合、これまでのいわゆる健康食品で錠剤等の形状のものは、栄養成分の人の健康に対する機能が科学的に証明されれば、逐次、規格基準型の「栄養機能食品」に指定され、当該食品について特定の保健的効果が科学的に証明されれば、個別許可型の「特定保健用食品」として許可されていくこととなる。
しかし、栄養成分の機能についての科学的な証明はされていないが、古くから、一般に健康に役立ち、何らかの効果があると期待されて、人々の間で利用されてきているものが多数あることは事実である。その中には、効果が疑われるものや、消費者にとって誤った情報を提供して販売されているものもある。このため、消費者が適切に選択し、安全な摂取ができるよう、配慮されなければならない。こうした食品について、消費者の適切な選択に資するためにどのような方策が考えられるのか、実態を踏まえつつ、引き続き検討することが必要である。
IV.おわりに
本検討会の報告書は、栄養補助食品等についての制度的枠組み案をとりまとめたものであり、実際の制度化に当たっては、今後別途、次のような個別具体的な検討が必要である。
なお、その際、関連する薬事行政との連携を図る必要がある。
- (1)規格基準型「栄養機能食品」の栄養成分のリストアップ
(2)各成分毎の表示方法を含む規格基準、表示基準の検討
(3)個別評価型の「特定保健用食品」の評価方法の検討
(4)個別の食品添加物の取扱いについての検討
(5)その他健康食品を含めた基準の検討
(6)消費者への情報提供、相談指導の検討
(7)その他
本検討会は、栄養補助食品について、適切な制度化がなされ、国民の健康増進に資することを願って、この報告書をまとめるものである。
