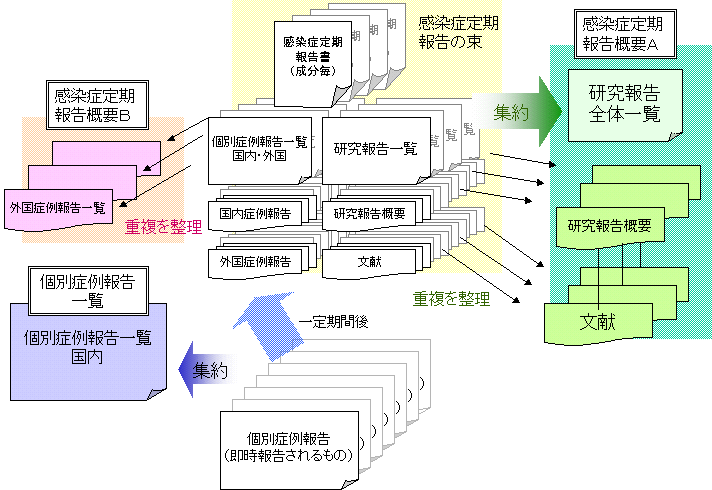
| 2 | 具体的な方法
| (1) | 感染症定期報告の内容は、原則、すべて運営委員会委員に送付することとするが、次の資料概要を作成し、委員の資料の確認を効率的かつ効果的に行うことができるようにする。
| (1) | 研究報告は、同一文献による重複を排した別紙のような形式の一覧表を作成し、当該一覧表に代表的なものの報告様式(別紙様式第2)及び該当文献を添付した「資料概要A」を事務局が作成し、送付する。 |
| (2) | 感染症発生症例報告のうち、発現国が「外国」の血漿分画製剤の使用による症例は、同一製品毎に報告期間を代表する感染症発生症例一覧(別紙様式第4)をまとめた「資料概要B」を事務局が作成し、送付する。 |
| (3) | 感染症発生症例報告のうち、発現国が「国内」の輸血による症例及び血漿分画製剤の使用による感染症症例については、「感染症報告事例のまとめ」を提出することから、当該症例に係る「資料概要」は作成しないこととする。ただし、運営委員会委員から特段の議論が必要との指摘がなされたものについては、別途事務局が資料を作成する。 |
|
| (2) | 発現国が「外国」の感染症発生症例報告については、国内で使用しているロットと関係がないもの、使用時期が相当程度古いもの、因果関係についての詳細情報の入手が困難であるものが多く、必ずしも緊急性が高くないと考えられるものも少なくない。また、国内症例に比べて個別症例を分析・評価することが難しいものが多いため、緊急性があると考えられるものを除き、その安全対策への利用については、引き続き、検討を行う。 |
| (3) | 資料概要A及びBについては、平成16年9月の運営委員会から試験的に作成し、以後「感染症定期報告について(目次)」資料は廃止することとする。 |
(別添)感染症定期報告・感染症個別症例報告の取扱い(案) |