

| ���j | ��L�\�� |
| �P | �@������ݒu�̎�| |
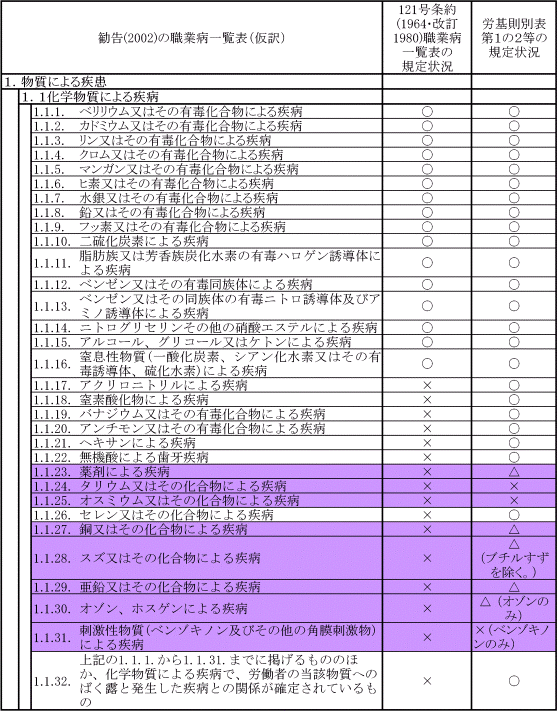
| �@�Ɩ��㎾�a�͈̔͂��߂Ă���J����@�{�s�K���i�ȉ��u�J��v�Ƃ����B�j��35���̋K��́A�ی����t�̐����̗e�Չ��y�ыƖ��㎾�a�ɑ���v���������ȕ⏞��}��ړI�ŁA���a53�N�ɔ��{�I�ȉ������Ȃ��ꂽ�B �@���a53�N�̉����ɓ�����A�����J����R�c��y�јJ���ҍЊQ�⏞�ی��R�c��ɑ����₵���Ƃ���A���R�c�������K���̉^�p�ɂ��Ĕz�����ׂ������̈�Ƃ��āA�V�������a�̔������ɑΏ�������悤�Ȉ�w���Ƃɂ�����I�Ȍ������s���ׂ��ł���|�����\�ɕt�L���ꂽ�B �@�����J���Ȃ́A���̓��\�܂��A��w���Ƃɂ��\������錟��������I�ɊJ�Â���ƂƂ��ɁA���̌������ʂɊ�Â��A�J���35���̋K��ɂ��ď��v�̐������s���Ă��Ă���B ���̌��ʁA���݂̘J����@�Ɋ�Â��Ɩ��㎾�a�͈̔͂́A�J��ʕ\��1��2�y�ѓ��\�Ɋ�Â������i�ȉ��u�J��ʕ\��1��2���v�Ƃ����B�j�ɂ�莦����Ă���Ƃ���ł���B |
| �Q | �@�������� | |||
|
| �R | �@�����ɓ������Ă̊�{�I�l���� | |||||||||
|
| �S | �@��������1�ɌW�錟���̍l�����y�ь������� | |||||||||||||||||||||||||||||||||||||||||||||||
|
| �T | �@��������2�̌������� |
| �@���a53�N�ȍ~�A��K��ɂ��Ɩ��㎾�a�Ƃ��ĔF�肳�ꂽ���Ăɂ��āA����I�ɘJ��ʕ\��1��2���ɒlj����ׂ����ۂ���w���Ƃɂ�錟�����s���A���̌��_�܂��ď��v�̑[�u���u�����Ă����Ƃ���ł���B����܂ŁA��K��ɂ��Ɩ��㎾�a�Ƃ��ĔF�肳�ꂽ���Ă̒��ł́u���������͉���������H���ɂ�����Ɩ��ɂ��x����v�y�сu�W�A�j�V�W���ɂ��炳���Ɩ��ɂ��A�H�n��ᇁv�ɂ��āA�lj����ׂ��Ƃ̌��_�Ɏ���A���v�̑[�u���u�����Ă����B �@���ʁA��K��ɂ��Ɩ��㎾�a�Ƃ��ĔF�肳�ꂽ���̂̂����A�V���ɒlj����ׂ����̂����邩�ۂ���������ɓ������āA�����e�̋Ɩ��ɂ�����V�����v�[�t�̎g�p���ɂ��ڐG���畆���A�������f�_�i�g���E���ɂ���Q�y�уt�����K�X�ɂ��̏�Q�ɂ��āA�ߔN�A�p���I�ɔF�莖�Ⴊ���������߁A���ڂ��Ă����Ƃ���ł���B�������Ȃ���A�����e�̋Ɩ��ɂ�����V�����v�[�t�̎g�p���ɂ��ڐG���畆���ɂ��ẮA�J��ʕ\��P�̂Q��4��1�̋K��Ɋ�Â������i����8�N�J���ȍ�����33���j�ł́u�P�̂��鉻�w�����y�щ������v�����ė��Ă��邽�߁A���Y���a�̌����ł��鉻�w�������������ł��邽�߁A���݂̋K��ɓ���܂Ȃ����ƕ��тɎ������f�_�i�g���E���ɂ���Q�y�уt�����K�X�ɂ��̏�Q�ɂ��ẮA����12�N�x�y�ѕ���13�N�x�ɂ�����F�茏��������܂ł̌����ɔ䂵�Č������Ă���V���Ɏ��グ��K�v���Ȃ����Ɠ��ɂ��A�����_�ɂ����āA�V���ɒlj�����K�v�͂Ȃ��ƍl������B |
| �U | �@�܂Ƃ� |
| �@�{������ł́A��194�������Ɏ�����Ă��鎾�a���тɕ���12�N�x�y�ѕ���13�N�x�ɕ�K��ɂ��Ɩ��㎾�a�Ƃ��ĔF�肳�ꂽ���a�܂��āA�V���ɒlj����ׂ����a�̗L���ɂ��Č������s�����B����̌����ł́A�����_�ɂ����ĐV���ɒlj�����K�v�͂Ȃ��Ƃ̌��_�ɒB�����B �@�Ȃ��A�؍ޕ�����ɂ�邪��i���@�o���j�ɂ��ẮA�����ɂ�����؍ޕ�����̎�ޕʂɌ������I�̒��x�A�l�����̎��Ԓ����A�u�w�������̎��{���]�܂��B |
| �����P |
| �@ | ���� |
��E�� |
| �@ | �R�@�p�N | �@���R��w���_���� |
| �@ | ��v�ۗ��W | �@�Y�ƈ�ȑ�w�w�� |
| �@ | ���c�@���O | �@�Q�n�p�[�X�Ō�Z����w�w�� |
| �@ | �����@��F | �@�k����w���_���� |
| �@ | �����@�B�� | �@�������M�a�@������ȑO���� |
| �@ | �H���@�ē� | �@���{��ȑ�w���� |
| (����) | �N��@���F | �@�����J���ЊQ�h�~����J���q���������̓Z���^�[���� |
| �@ | �Ėځ@�� | �@��㏾�����q��w���� |
| �@ | �쌩�R�ꐶ | �@������ȑ�w���_���� |
| �@ | �n���@���F | �@���l�J�Еa�@���@�� |
| �@ | ���с@�� | �@�c�F���`�O�ȕa�@���@�� |
| �@ | ���V�@�M�v | �@�֓��J�Еa�@�@�� |
| �@ | �a�c�@�U | �@��ʈ�ȑ�w���� |
| ����14�N | 9�� | 6�� | �@��1���� |
| ����14�N | 12�� | 17�� | �@��2���� |
| ����15�N | 3�� | 24�� | �@��3���� |
| �����Q |
R194 List of Occupational Diseases Recommendation, 2002
Recommendation concerning the List of Occupational Diseases and the Recording and Notification of Occupational Accidents and Diseases
Recommendation:R194
The General Conference of the International Labour Organization,
Having been convened at Geneva by the Governing Body of the International Labour Office, and having met in its 90th Session on 3 June 2002, and
Noting the provisions of the Occupational Safety and Health Convention and Recommendation, 1981, and the Occupational Health Services Convention and Recommendation, 1985, and
Noting also the list of occupational diseases as amended in 1980 appended to the Employment Injury Benefits Convention, 1964, and
Having regard to the need to strengthen identification, recording and notification procedures for occupational accidents and diseases, with the aim of identifying their causes, establishing preventive measures, promoting the harmonization of recording and notification systems, and improving the compensation process in the case of occupational accidents and occupational diseases, and
Having regard to the need for a simplified procedure for updating a list of occupational diseases, and
Having decided upon the adoption of certain proposals with regard to the recording and notification of occupational accidents and diseases, and to the regular review and updating of a list of occupational diseases, which is the fifth item on the agenda of the session, and
Having determined that these proposals shall take the form of a Recommendation;
adopts this twentieth day of June of the year two thousand and two the following Recommendation, which may be cited as the List of Occupational Diseases Recommendation, 2002.
1. In the establishment, review and application of systems for the recording and notification of occupational accidents and diseases, the competent authority should take account of the 1996 Code of practice on the recording and notification of occupational accidents and diseases, and other codes of practice or guides relating to this subject that are approved in the future by the International Labour Organization.
2. A national list of occupational diseases for the purposes of prevention, recording, notification and, if applicable, compensation should be established by the competent authority, in consultation with the most representative organizations of employers and workers, by methods appropriate to national conditions and practice, and by stages as necessary. This list should:
(a) for the purposes of prevention, recording, notification and compensation comprise, at the least, the diseases enumerated in Schedule I of the Employment Injury Benefits Convention, 1964, as amended in 1980;
(b) comprise, to the extent possible, other diseases contained in the list of occupational diseases as annexed to this Recommendation; and
(c) comprise, to the extent possible, a section entitled "Suspected occupational diseases".
3. The list as annexed to this Recommendation should be regularly reviewed and updated through tripartite meetings of experts convened by the Governing Body of the International Labour Office. Any new list so established shall be submitted to the Governing Body for its approval, and upon approval shall replace the preceding list and shall be communicated to the Members of the International Labour Organization.
4. The national list of occupational diseases should be reviewed and updated with due regard to the most up-to-date list established in accordance with Paragraph 3 above.
5. Each Member should communicate its national list of occupational diseases to the International Labour Office as soon as it is established or revised, with a view to facilitating the regular review and updating of the list of occupational diseases annexed to this Recommendation.
6. Each Member should furnish annually to the International Labour Office comprehensive statistics on occupational accidents and diseases and, as appropriate, dangerous occurrences and commuting accidents with a view to facilitating the international exchange and comparison of these statistics.
ANNEX
LIST OF OCCUPATIONAL DISEASES| �����R |
 |
||
 |
||
 |
||
|
| �����S |
�P�@��܂ɂ�鎾�a
�@���舵���������ƍl������E�Ɗ֘A�������ł́A�b���܂����畆�Ǐ唼���߂Ă���B��܂����̂ɋy�ڂ��e���Ƃ��ẮA1) ���̕����������ٓI�ȓŐ��E��p�ɂ����́A2)����ٓI�Ȏh���Ǐ�A3)�A�����Q���Ƃ��Ă̍�p�A�̂R���l������B
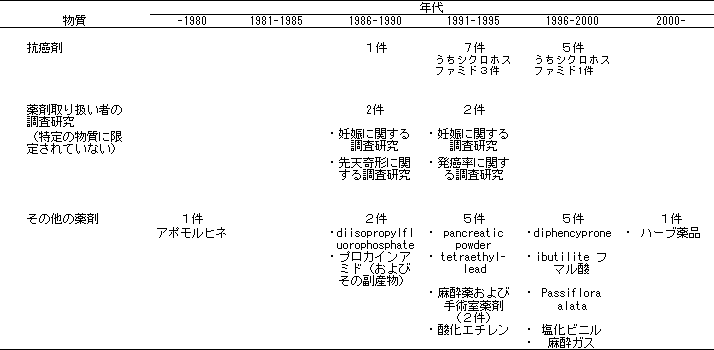
�@��܂Ƃ��Ďg�p�����Ώۉ��w�����̎�ނ͋ɂ߂đ����A�{�����őS�Ă��m���߂邱�Ƃ͕s�\�ł������B�����ŁA�܂��A�A�����J National Library of Medicine�̐E�Ƌy�ъ��Ɋւ���_���̃f�[�^�x�[�X�ɂ����āA1970�N�Ȍ�̕�������A�u��܁A��ܐ��́v�Ɓu�E�Ɛ��v�̌������ƂɁA�����������s�����i94�������o�j�B���̌����ł́A��܂��̂��̖̂���⊳�҂ւ̉e���Ȃǂ����S�ɕ������邱�Ƃ�����A���Ƃōi�荞�݂�������Ȃ��������A����ł����e���s���̂��̂����Ȃ��Ȃ������B���̂����A����^�[���A���ː��Ȃǂ��I����܂łȂ����́A�܂���܋N�����ɂ��ċL�q���Ă��Ȃ����̂�������31�����c�����iP.23�ʓY�Q�Ɓj�B���̌��ʂ�N�x�ʂɌ���ƁA�V�N���t�H�X�t�@�~�h�̔����Ɋւ���4���̕������A�啔����1�����ɂP�`2���̕ɂƂǂ܂�A���ɐE�ƕa�Ƃ��ďW�ϓI�ɖ��ɂȂ��Ă�����i�͖������Ƃ����������B
�@�܂��A���ɂ킪���ŕ��ꂽ��܂��������Ȃ��悤�ɂ��邽�߁A��w�����G���f�[�^�x�[�X�ŁA�ߋ��P�O�N�ɂ����āu�E�Ɛ��v�Ɓu��v�܂��́u���i�v�̃L�[���[�h�̑g�ݍ��킹�Ō������ꂽ�W�S�����̂�������A��܋N�����b�����̂����A�E�ƂƂ̊֘A�Ɋւ��ăp�b�`�e�X�g��Ɖu�w�I�Ȍ����ɂ���ď\���ȍl�@���s���Ă���U���̓��e�i�v16�����j�ɂ��đI�ʂ����e�����������B
�@���̌��ʁA�����ɂ����Ă�����̈��i�ő����̌��N�e�������ꂽ���̂͂Ȃ������B�������A����������Q�������͕̂X�R�̈�p�ƍl�����A���̐E�ƋN�����̖֘A�����͑��ɂ���������\�������邱�Ƃ���A��戵���J���҂̌��N��Q�h�~���߂̋���A���̒�����ɏ[��������Ȃǂ̑[�u�͕K�v�ł��낤�B
| 1) | Chan-Yen M, Malo J-L (1994): Aetiological agents in occupational asthma. Eur Respir J, 7: 346-371 |
| 2) | Sestini P, et al.(1996): Inhaled PGE2 prevents aspirin-induced bronchoconstriction and urinary LTE4 excretion in aspirin-sensitive asthma. Am J Respir Crit Care Med, 153: 572-575 |
| 3) | Szczeklik A, Mastalerzl L, et al.(1996): Protective and bronchodilator effects of prostaglandin E and salbutamol in aspirin induced asthma. Am J Respir Crit Care Med, 153: 567-571 |
| 4) | Cowburn AS, et al.(1998): Over expression of leukotriene C4 synthase in the bronchial biopsies of aspirin-intolerant asthmatics. J Clin Invest, 101: 834-846 |
| 5) | ����L��(2001): �n���Q�������掆�Ɏg�p����s���]�����U���̂ɂ��E�Ɛ��b���̈��,ASTHMA, 14: 15-19 |
| 6) | ��_���(1990): �Ζ�戵�҂Ɍ���ꂽ�E�Ɛ��b��,�A�����M�[�̗Տ�,10(5): 62-63 |
| 7) | ���c�މ���(1993): ���i�ɂ��E�Ɛ��A�����M�[�̗Տ��w�I����.��ʌ���w��G��,28(2): 371 |
| 8) | �H�c�_�F��(2001): ���`���o���g���l��]��悵��bisphenol A�ɂ��E�Ɛ��ڐG�畆���̂P��.�A�����M�[�̗Տ�,21(13): 1048-1051 |
| 9) | Whitfelt MJ, et al.(1991): Erythema multiforme after contact dermatitis is response to an sealant. J Am Acad Dermatol, 25: 386-388 |
| 10) | Estlander T, et al.(1999): Occupational contact allergy to bisphenol A. Contact Dermatitis, 40: 52-53 |
| 11) | Matsunaga K, et al.(1995): Occupational allergic dermatitis-Experience from 26 cases in the past three years. Environ Dermatol, 2: 185-190 |
| 12) | Kanerva L, et al.(2000): Occupatinal allergic airbone contact dermatitis and delayed bronchial asthma from epoxy resin revealed by bronchial provocation test. Eur J Dermatol, 10: 474-477 |
| 13) | Miyamoto T, et al.(1998): Occupational contact urticaria due to epoxy resin. Environ Dermatol, 5: 53-57 |
| 14) | Hayakawa R, Tuyoshi T(1984): Occupational dermatitis due to bisphenol F. Skin Research, 26: 620-634 |
| 15) | Torinuki W, et al.(1995): Contact dermatitis to biperiden and phtocontact dermatitis to phenothiazines in a pharmacist. Tohoku J Exp Med, 176: 249-252 |
| 16) | �l����(1991): �畆,33(10): 142-147 |
| 17) | ���ʂ�(1990): �畆,32(8): 242-247 |
| 18) | �������q��(1992): �畆,33(10): 83-87 |
| 19) | Harman RRM, Sarkany I(1960): Copy paper dermatits. Trans St John's Hosp Derm Soc, 44: 37-42 |
| 20) | Foussereau J, et al.(1982): Occupational contact dermatitis. Munksgaard, Copenhagen,306-309 |
| 21) | Ueda K, et al.(2000): A case of occupational contact uriticaria due to 2-ethyl-6-methyl aniline and 2,4,6-trimethyl aniline. Environ Dematol, 7: 95-98 |
| 22) | Matsunaga K, et al.(1995): Occupational allergic contact dermatitis, - Experience from 26 cases in the past three years - . Environ Dematol, 2: 185-190 |
| 23) | �ӐU�ق�(2000): �E�Ɛ��ڐG���畆��.���W���[�i��,36(5)�F1305-1313 |
�i�ʓY�j
| 1) | Dahlquist I(1977): Allergic reactions to apomorphine. Contact Dermatitis, 3(6): 349-350S |
| 2) | Krepinsky A, et al.(1990): Comparison of three assays for genetic effects of antineoplastic drugs on cancer patients and their nurses. Environ Mol Mutagen, 15(2): 83-92 |
| 3) | Schaumburg I, Olsen J(1989): Time to pregnancy among Danish pharmacy assistants. Scand J Work Environ Health, 15(3): 222-226 |
| 4) | Schaumburg I, Olsen J(1990): Congenital malformations and death among the offspring of Danish pharmacy assistants. Am J Ind Med, 18(5): 555-564 |
| 5) | Casale GP, et al.(1989): Inhibition of human serum complement activity by diisopropylfluorophosphate and selected anticholinesterase insecticides. Fundam Appl Toxicol, 12(3): 460-468 |
| 6) | Foussereau J,(1989): Accidental occupational sensitization to p-nitrobenzoyl chloride in a chemistry student synthesizing procaine. Contact Dermatitis,20(5): 397-398 |
| 7) | Guinee EP, et al.(1991): Evaluation of genotoxic risk of handling cytostatic drugs in clinical pharmacy practice. Pharm Weekbl Sci,13(2): 78-82 |
| 8) | Sardas S, et al.(1991): Sister chromatid exchanges in lymphocytes of nurses handling antineoplastic drugs. Toxicol Lett, 55(3): 311-315 |
| 9) | Valanis BG, et al.(1993): Association of antineoplastic drug handling with acute adverse effects in pharmacy personnel. Am J Hosp Pharm , 50(3): 455-462 |
| 10) | Sessink PJ, et al.(1994): Urinary cyclophosphamide excretion and chromosomal aberrations in peripheral blood lymphocytes after occupational exposure to antineoplastic agents. Mutat-Res, 309(2): 193-199 |
| 11) | Ensslin AS, et al.(1994): Biological monitoring of cyclophosphamide and ifosfamide in urine of hospital personnel occupationally exposed to cytostatic drugs. Occup Environ Med,51(4): 229-233 |
| 12) | Sessink PJ, et al.(1994): Environmental contamination and assessment of exposure to antineoplastic agents by determination of cyclophosphamide in urine of exposed pharmacy technicians: Is skin absorption an important exposure route? Arch Environ Health,49(3): 165-169 |
| 13) | Ensslin AS,et al.(1994): Urinary platinum in hospital personnel occupationally exposed to platinum-containing antineoplastic drugs. Int Arch Occup Environ Health, 65(5): 339-342 |
| 14) | Schaumburg I, Olsen J(1991): Birth weight and gestational age among children of Danish pharmacy assistants. J Epidemiol Community Health, 45(1): 49-51 |
| 15) | Hansen J, Olsen JH(1994): Cancer morbidity among Danish female pharmacy technicians. Scand J Work Environ Health, 20(1): 22-26 |
| 16) | van-Toorenenbergen AW, et al.(1991): Occupational allergy to pancreatic powder; characterization of IgE-binding antigens in pancreatic extract by immunoblotting. J Allergy Clin Immunol,87(3): 650-654 |
| 17) | Vural N, Duydu Y(1995): Biological monitoring of lead in workers exposed to tetraethyl lead. Sci Total Environ, 171(1-3): 183-187 |
| 18) | Sardas S, et al.(1992): Sister-chromatid exchanges in operating room personnel. Mutat Res, 279(2): 117-120 |
| 19) | Karakaya A, et al.(1992): The effects of volatile anaesthetic agents on human immune system function via occupational exposure. Immunopharmacol Immunotoxicol: 251-259 |
| 20) | Burgaz S, et al.(1992): Thioethers in urine of sterilization personnel exposed to ethylene oxide. J Clin Pharm Ther, 17(3): 169-172 |
| 21) | Ensslin AS, et al.(1997): Biological monitoring of hospital pharmacy personnel occupationally exposed to cytostatic drugs; urinary excretion and cytogenetics studies. Int Arch Occup Environ Health, 70(3): 205-208 |
| 22) | Valanis B, et al.(1997): Occupational exposure to antineoplastic agents and self-reported infertility among nurses and pharmacists. J Occup Environ Med, 39(6): 574-580 |
| 23) | Undeger l, et al.(1999): Assessment of DNA damage in nurses handling antineoplastic drugs by the alkaline COMET assay. Mutat Res, 439(2): 277-285 |
| 24) | Valanis B, et al.(1999): Occupational exposure to antineoplastic agents self-reported miscarriages and stillbirths among nurses and pharmacists. J Occup Environ Med, 41(8): 632-638 |
| 25) | Burgaz S, et al.(1999): Urinary cyclophosphamide excretion and micronuclei frequencies in peripheral lymphocytes and in exfoliated buccal epithelial cells of nurses handling antineoplastics. Mutat Res,439(1): 97-104 |
| 26) | Bircher AJ, et al.(1999): Occupational airborne contact dermatitis from diphencyprone in a pharmacy employee. Contact Dermatitis,41(1): 52 |
| 27) | Dodds ES, Oberg KC(1998): Erythematous bullous lesions on the dorsa of the hands due to contact exposure to ibutilide fumarate for injection. Pharmacotherapy,18(4): 880-882 |
| 28) | Giavina-Bianchi PF Jr, et al.(1997):Occupational respiratory allergic disease induced by Passiflora alata and Rhamnus purshiana. Ann Allergy Asthma Immunol,79(5): 449-454 |
| 29) | Awara WM, et al.(1998): Assessment of vinyl chloride-induced DNA damage in lymphocytes of plastic industry workers using a single-cell gel electrophoresis technique. Toxicology, 128(1): 9-16 |
| 30) | Sardas S, et al.(1998): Use of alkaline comet assay (single cell gel electrophoresis technique) to detect DNA damages in lymphocytes of operating room personnel occupationally exposed to anaesthetic gases. Mutat Res, 418(2-3): 93-100 |
| 31) | Lee SK, et al.(2001): Occupational asthma and rhinitis caused by multiple herbal agents in a pharmacist. Ann Allergy Asthma Immunol, 86(4): 469-474 |
�Q�@�^���E�����͂��̉������ɂ�鎾�a
�@�l�ɑ��錒�N�e���i���Ǘ�j�ɂ��āABrockhaus��(1981)�́A�h�C�c�̃Z�����g�H��t�߂ɋ��Z���A���̒n��Ŏ��n�����ʕ��E���ێ悵�Ă���Z���ɂ��Ē����������ʁA������Q�A��J���A�s����ԁA���ɂ��̑��̐��_�Ǐ�A�_�o�E�؏Ǐ�������w�I���j�^�����O�l�ɐ��̑��ւ����������A�E�тɊւ��Ă͕��̑��ւł������B�@Ludolph��(1986)�́A�Z�����g�H��ɂĕ���22.9�N�Ԃ̃^���E�����I������Ǝ�36���̌��N�e���������B���҂�͒����_�o�n����і����_�o�n�̏Ǐ����݂�ꂽ�Əq�ׂĂ��邪�A���̒����ł͑ΏƌQ���ݒ肳��Ă��Ȃ��B
�@�����ɑ��錒�N�e���ɂ��āA��r�I���ʂ̃^���E�����^�ŁA�����E���B�Ő��A�_�o�Ő����Ɋւ����������[Roll and Matthiaschk 1981�ABornhausen and Hagen 1984�AFormigli�� 1986�AGibson and Becker 1970]�B
�@�ȏォ��A�����̐_�o�n��Q��������悤�����A���m�ɂ͂Ȃ��Ă��Ȃ��B�E�т͏]�����猾���Ă���A���a�̔��ǂ͖��m�ł���B
| 1) | Curtis DK.ed. Casatett and Doull's Toxicology(2001): The Basic Science of Poisons.6th edition, McGraw-Hill, New York: 855-856. |
| 2) | IPCS (International Programme in Chemical Safety) (1996): Environmental Health Criteria 182: Thallium. World Health Organization,Genev |
| 3) | Risk Assessment Information System: Toxicity Summary For Thallium(1994). http://risk.lsd.ornl.gov/tox/profiles/thallium_f_V1.shtml. |
| 4) | Talas A, Wellhoener H.H. (1983): Dose-dependency of thallium(1+) kinetics as studied in rabbits. Arch Toxicol, 53(1): 9-16. |
| 5) | Talas A, et al.(1983): Pharmacokinetic parameters for thallium (I)-ions in man. Arch Toxicol, 53(1): 1-7. |
| 6) | Rios C, et al. (1989): Brain regional thallium distribution in rats acutely intoxicated with Tl2SO4. Arch Toxicol. 63: 34-37 |
| 7) | Richelmi P, et al.(1980): Salivary levels of thallium in acute human poisoning. Arch Toxicol, 43: 321-325. |
| 8) | de Groot G, Van Heijst A.N.P. (1988): Toxicokinetic aspects of thallium poisoning. Methods of treatment by toxin elimination. Sci Total Environ. 71: 411-418 |
| 9) | Tabandeh H, et al. (1994): Ophthalmologic features of thallium poisoning, Am J Ophthal, 117: 243-245 |
| 10) | Aoyama H(1989): Distribution and excretion of thallium after oral and intraperitoneal administration of thallous malonate and thallous sulfate in hamsters. Bull Environ Contam Toxicol, 42: 456-463 |
| 11) | Woods JS, Fowler BA (1986): Alteration of hepatocellular structure and function by thallium chloride: Ultrastructural, morphometric, and biochemical studies. Toxicol Appl Pharmacol, 83: 218-229 |
| 12) | Roll R, Matthiaschk G (1981): Investigations on embryotoxic effects of thallium chloride and thallium acetate in mice and rats. Teratology, 24: 46A-47A |
| 13) | Formigli E, et al.(1986): Thallium induced testicular toxicity in the rat. Environ. Res, 40: 531 |
| 14) | Hall BK(1985): Critical periods during development as assessed by thallium-induced inhibition of growth of embryonic chick tibiae in vitro. Teratology, 31: 353-361 |
| 15) | Neubert D, Bluth U(1985): Effect of thallium on limb development in organ culture. Teratology, 32: 29A |
| 16) | Brockhaus A, et al.(1981): Intake and health effects of thallium among a population living in the vicinity of a cement plant emitting thallium containing dust. Int Arch Occup Environ Health, 48: 375-389 |
| 17) | Stokinger HE(1981): The metals. In: Patty's Industrial Hygiene and Toxicology, vol. 2A, G.D. Clayton and F.E. Clayton, Eds, 1749-1769 John Wiley & Sons, New York |
| 18) | Ludolph A, et al.(1986): Chronic thallium exposure in cement plant workers: Clinical and electrophysiological data. Trace Elem Med, S3: 121-125 |
�R�@�I�X�~�E�����͂��̉������ɂ�鎾�a
�@�I�X�~�E���̓Ő����A�E�Ɛ��̎��a�Ɋ֘A�����_���́A�_���̃f�[�^�x�[�X��ł͌����o���Ȃ������B���Y�ʂ����Ȃ��A�Y�ƓI�g�p�p�x����I�e���ɂ��Ă��܂茤������Ă��Ȃ��̂�����ł���B
�@�l�ɑ���e���Ƃ��āA�_���I�X�~�E���̍��Z�x�}�����I�ɂ��@�S���A�C���A��S���A�畆�ɑ��鋭���h���ɂ��A�ɂ݁A�P�A�C�ǎx���A�ċz����A�������A���܁A�畆�����̏Ǘ�͂��邪�A�������I�f�[�^�͌��������Ȃ������B
�@�����ɑ���e���ɂ����͓��L���ׂ������͂Ȃ������B
�@�ȏォ�玖�̓I�ɔ��������}�����I�ɂ��e���͖��炩�ł��邪�A�������I�Ƃ̈��ʊW�͖��m�ł͂Ȃ��B
| 1) | Venugopal B, Luckey TD (1978): Toxicity of group VIII metals. In Venugopal B, Lucy TD, eds. : Metal toxicity in mammals, vol 2. 273-305, Plenum Publishing, New York |
| 2) | Proctor NH, et al.(1988): Chemical hazards of the workplace. 393-436, JB Lippincott Co, Philadelphia |
| 3) | Seiler HG, Sigel H(1988): Handbook on toxicity of inorganic compounds. 341-344, 501-574, Marcel Dekker, New York |
| 4) | Goyer RA(19996): Toxic effects of metals. In: Klaassen CD, ed. Casarett and Doull's toxicology: the basic science of poisons, 5th ed. 725-726, McGraw-Hill, New York |
| 5) | Maugh TH(1981): New ways to use metals for arthritis. Science, 212: 430-431 |
| 6) | Hammond VR(1986): The elements. In East RC., Astle MJ, Beyer WH, eds.: CRC handbook of chemistry and physics.B5-B43, CRC Press,Boca Raton, FL |
| 7) | American Conference of Govermental Industial Hygienists(1996): Threshold limit values for chemical substances in the work environment. |
| 8) | National Institute for Occupational Safety and Health (NIOSH)(1981): Occupational health guidelines for osmium tetroxide: occupational health guide for chemical hazards. DHHS Pub No 81-123, National Institute for Occupational Safety and Health, Department of Health and Human Services. Rockville, Md |
| 9) | Eula B, et al.(1986): Patty's Tocxicology. Vol3 5th ed.John Wiley & Sons |
�S�@�����͂��̉������ɂ�鎾�a
�@�l�ɑ���e���i�Ǘ�������j�ɂ��āAGorell��(1999)��144���̃p�[�L���\���a���҂�464���̌���҂�ΏƂƂ����Ǘ�Ώƌ����ŁA20�N�ȏ�̂��I�ł́A���P�Ƃ��I�̃I�b�d�䂪2.49�A�}���K�����I10.6�A���E���̕������I5.2�A���E�S�̕������I2.8�A���E�S���I�̕������I3.7�ł������B���I�ʂ̏��͂Ȃ��B[�Q�ƕ����ԍ��P�P]
�@Nuyts��(2001)�͖����t�s�S����272���ƌ����272����ΏƂƂ����Ǘ�Ώƌ����ŁA�����I�ɂ��ăI�b�d�䂪2.5�ł������B���I�ʂ̏��͂Ȃ��B[�Q�ƕ����ԍ�12]�B
�@���������ɂ��ē��L���ׂ������͂Ȃ������B
�@����̃��r���[���[�N�̌��ʁA�Ǘ�Ώƌ����Ńp�[�L���\���a�i�P�ҁj�Ɩ����t�s�S�i�P�ҁj�œ����I�̃I�b�Y�䂪�����Ƃ̕����������A�e�X�P�҂ł��邱�ƁA�Ǘ�Ώƌ����ɂ����ẮA���ʊ֘A�ɂ��Ă̏��Ɍ��E�����邱�Ƃ���A�V���Ȍ��N�e���̒m���Ƃ͂����Ȃ��B
| 1) | �����T�j, ����K�q,�Ė� (1999): ���w�����Ő��n���h�u�b�NIII:161-164,�ۑP,���� |
| 2) | �a�c�U�ҏW (1991):�Ő������u��18 �Y�Ɖ��w�����A�����w����: 294-297,�n�l����,���� |
| 3) | Aaseth J, Norseth T(1986): Handbook on the Toxicology of Metals, Vol.II: 233-254 |
| 4) | Strickland G, et al.(1964): Absorption of copper in homozygotes and heterozygotes for Wilson's disease and controls; isotope tracer studies with 67 Cu and 64 Cu. Clin Sci,43: 617-625 |
| 5) | Cartwright GE, Wintrobe MM(1964): Copper metabolism in normal subjects. Am J Clin Nutr,14: 224-232 |
| 6) | Bentur Y,et al.(1988): An unusual skin exposure to copper; clinical and pharmacokinetic evaluation. J Toxicol Clin Toxicol,26(5-6): 371-380 |
| 7) | Jantsch W, et al.(1984-1985): Massive copper sulfate ingestion resulting in hepatotoxicity. J Toxicol Clin Toxicol,22(6): 585-588 |
| 8) | Ostiguy G, et al.(1995): Respiratory health of workers exposed to metal dusts and foundry fumes in a copper refinery. Occup Environ Med, 52(3): 204-210 |
| 9) | Romeu-Moreno A, et al.(1994): Rspiratory toxicity of copper. Environ Health Persp, 102(suppl3): 339-340 |
| 10) | Drummond G, et al.(1986): Comparative study of various methods used for determining health effects of inhaled sulfates. Environ Resr, 41: 514-528 |
| 11) | Gorell JM, et al.(1999): Occupational exposure to manganese, copper, lead, iron, mercury and zinc and the risk of Parkinson's disease. NeuroToxicology,20(2-3): 239-248 |
| 12) | Nuyts GD, et al.(2001): New occupational risk factors for chronic renal failure Lancet, 346: 7-11 |
| 13) | Gotteland M, et al.(2001): Effect of acute copper exposure on gastrointestinal permeability in healthy volunteers. Dig Dis Sci,46(9): 1909-1914 |
| 14) | Bahattin Adam, et al.(2001): The interaction between copper and coronary risk indicators. Jpn Heart J,42(3): 281-286 |
�T�@�X�Y���͂��̉������ɂ�鎾�a�i�����M�������j
�@�X�Y����т��̉������ɋN����������M�ȊO�̐E�Ɛ����a�Ƃ��āC���@�X�Y�x�����邪�A����͑g�D�������Ȃ��ǐ��̂���x�ł���B
�@�畆�Ǐ�Ƃ��āC���@�X�Y�ɂ��A�����M�[���ڐG���畆���C�t�b���g���t�F�j���X�Y�ɂ��h�����ѕ�C�g���t�F�j���X�Y�A�Z�e�[�g�ɂ���@���]�ƌ��ǐ�����C�g�����`���X�Y�ɂ��畆�M���C�_���g���u�`���X�Y�ɂ�鐅�v�E�т��`�����h�����畆���C�t�^���_�g���u�`���X�Y�ɂ��ڐG���畆��������Ă���B
�@�ӎ���Q�C�z���C�L����Q��_�Ǐ�悷�钆���_�o��Q���C�g�����`���X�Y��W���`���X�Y�ւ̐E�Ɛ����I�ɂ�萶�������Ƃ�����Ă���i��E�Ɛ����I�ł͂��������C�g���G�`���X�Y�ł������_�o��Q���������j�B
�@�d�ĂȑS�g�Ǐ�������ł��C�g���t�F�j���X�Y�A�Z�e�[�g�ƃg�����`���X�Y����уW���`���X�Y�ւ̐E�Ɛ����I�ɂ�萶���Ă���B�g�����`������уW���`���X�Y���I�ł́C�����_�o��Q�ɉ����āC�̕s�S�C�t�s�S�C�ċz�s�S�ɂ��1�������S���Ă���B
�@�_���g���u�`���X�Y���I�ɂ��C�ǎx�b����1�����Ă���B
�@�ȏォ��C���@����їL�@�X�Y�������ɂ��h�����畆���A����сC�L�@�X�Y�C���Ƀg���A���L���������̂����g�����`���X�Y�ւ̂��I�ɂ�鐸�_�E�_�o��Q���d�v�ł���Ǝv����B
| 1) | Sluis-Cremer GK, et al.(1989): Stannosis. A report of 2 cases. S Afr Med J, 75: 124-126 |
| 2) | de Fine Olivarius F, et al. (1993): Skin reactivity to tin chloride and metallic tin. Contact Dermatitis, 29: 110-111 |
| 3) | Menne T, et al. (1987): Tin; an overlooked contact sensitizer? Contact Dermatitis, 16: 9-10 |
| 4) | Nielsen NH, Skov L (1998): Occupational allergic contact dermatitis in a patient with a positive patch test to tin. Contact Dermatitis, 39: 99-100 |
| 5) | Fait A, et al. (1994): Organotin compounds. Toxicology, 91: 77-82 |
| 6) | Andersen KE, Petri M (1982): Occupational irritant contact folliculitis associated with triphenyl tin fluoride (TPTF) exposure. Contact Dermatitis, 8: 173-177 |
| 7) | Colosio C, et al. (1991): Occupational triphenyltin acetate poisoning; a case report. Br J Ind Med, 48: 136-139 |
| 8) | Fortemps E,et al. (1978): Trimethyltin poisoning. Report of two cases. Int Arch Occup Environ Health, 41: 1-6 |
| 9) | Ross WD,et al. (1981): Neurotoxic effects of occupational exposure to organotins. Am J Psychiatry, 138: 1092-1095 |
| 10) | Rey C, et al. (1984): Methyltin intoxication in six men; toxicologic and clinical aspects. Vet Hum Toxicol, 26: 121-122 |
| 11) | Feldman RG, et al. (1993): Trimethyltin encephalopathy. Arch Neurol, 50: 1320-1324 |
| 12) | Krinke GJ(2000): Triethyltin. In: Experimental and Clinical Neurotoxicology, 2nd ed. (Spencer PS & Schaumburg HH, ed), 1206-1208, Oxford Univ Press, New York |
| 13) | Goh CL (1985): Irritant dermatitis from tri-N-butyl tin oxide in paint. Contact Dermatitis, 12: 161-163 |
| 14) | Lewis PG, Emmett EA (1987): Irritant dermatitis from tri-butyl tin oxide and contact allergy from chlorocresol. Contact Dermatitis, 17: 129-132 |
| 15) | Grace CT, et al. (1991): Recurrent irritant contact dermatitis due to tributyltin oxide on work clothes. Contact Dermatitis, 25: 250-251 |
| 16) | Hamanaka S, et al.(1992): Phthalic acid dermatitis caused by an organostannic compound, tributyl tin phthalate. Dermatology, 184: 210-212 |
| 17) | Shelton D, et al. (1992): Occupational asthma induced by a carpet fungicide- tributyl tin oxide. J Allergy Clin Immunol, 90: 274-275 |
�U�@�������͂��̉������ɂ�鎾�a�i�����M�������j
�@��������т��̉������ɋN����������M�ȊO�̐E�Ɛ����a�Ƃ��āC�����q���[���z���ɂ��C�ǎx�b���i�����M�Ǐ�Ƃ̕����j����������B�܂��C���̑��̌ċz��ɑ���e���Ƃ��āC�Ĕ����̉ߕq���x������y�x�̉t���x�@�\��Q������Ă���B��Q�̒��x�́C���������̕����C�_������������ʂɏd���B
�@�ċz��n�ȊO�ւ̌��N�e���Ƃ��ẮC�����q���[���ɂ���@���]�ƌ��ǐ�����C�_�������ɂ��畆�Ώ��C���������ɂ��p�����Ɣ����Ⴊ�e�X1�Ⴘ����Ă���B��ʂɁC�畆�h���Ǐ�́C���������Ɛ|�_�����̕����C���_������_���������������B
�@�E�Ɛ��̈����q���[���z�����I�ł́C������n�C�_�o�n�C���t�E�����n����ю��ɋy�ڂ��d�ĂȌ��N�e���́C�����_�ł͖��炩�ł͂Ȃ��B
�@�ȏォ��C�����́C�����M�ɑ�������E�Ɛ��b���ւ̑d�v�ł���B
| 1) | Roto P (1980): Asthma, symptoms of chronic bronchitis and ventilatory capacity among cobalt and zinc production workers. Scand J Work Environ Health, 6(Suppl 1): 1-49 |
| 2) | Hong CS, et al. (1986): Occupational asthma caused by nickel and zinc. Korean J Intern Med, 1: 259-262 |
| 3) | Vogelmeier C, et al. (1987): Pulmonary involvement in zinc fume fever. Chest, 92: 946-948 |
| 4) | Weir DC, et al. (1989): Occupational asthma due to soft corrosive soldering fluxes containing zinc chloride and ammonium chloride. Thorax, 44: 220-223 |
| 5) | Malo JL,et al. (1990): Acute lung reaction due to zinc inhalation. Eur Respir J, 3: 111-114 |
| 6) | Ameille J, et al. (1992): Occupational hypersensitivity pneumonitis in a smelter exposed to zinc fumes. Chest, 101: 862-863 |
| 7) | Malo JL, et al. (1993): Occupational asthma due to zinc. Eur Respir J, 6: 447-450 |
| 8) | Pasker HG, et al. (1997): Short-term ventilatory effects in workers exposed to fumes containing zinc oxide; comparison of forced oscillation technique with spirometry. Eur Respir J, 10: 1523-1529 |
| 9) | Zerahn B, et al. (1999): Pulmonary damage after modest exposure to zinc chloride smoke. Respir Med, 93: 885-890 |
| 10) | Fuortes L , Schenck D (2000): Marked elevation of urinary zinc levels and pleural-friction rub in metal fume fever. Vet Hum Toxicol, 42: 164-165 |
| 11) | Hamdi EA (1969): Chronic exposure to zinc of furnace operators in a brass foundry. Br J Ind Med, 26: 126-134 |
| 12) | Schiffer RB (1994): Zinc and multiple sclerosis. Neurology, 44: 1987-1988 |
| 13) | Amr MM, et al. (1997): Neuropsychiatric syndromes and occupational exposure to zinc phosphide in Egypt. Environ Res, 73: 200-206 |
| 14) | Woods, JS (1995): Hematopoietic system. In: Metal Toxicology (Goyer RA, Klaassen CD & Waalkes MP, ed). Academic Press, New York, pp298-300 |
| 15) | Helander I, Makela A (1983): Contact urticaria to zinc diethyldithiocarbamate (ZDC). Contact Dermatitis, 9: 327-328 |
| 16) | Farrell FJ (1987): Angioedema and urticaria as acute and late phase reactions to zinc fume exposure, with associated metal fume fever-like symptoms. Am J Ind Med, 12: 331-337 |
| 17) | de Juan A, et al. (2000): Zinc burns; a rare burn injury. Burns, 26: 498-500 |
| 18) | Houle RE , Grant WM (1973): Zinc chloride keratopathy and cataracts. Am J Ophthalmol, 75: 992-996 |
| 19) | Skogedal O, et al. (1977): Pilot study on dental erosion in a Norwegian electrolytic zinc factory. Community Dent Oral Epidemiol, 5:248-251 |
| 20) | Remijn B, et al. (1982): Zinc chloride, zinc oxide, hydrochloric acid exposure and dental erosion in a zinc galvanizing plant in the Netherlands. Ann Occup Hyg, 25: 299-307 |
| 21) | Barceloux DG (1999):Zinc. J Toxicol Clin Toxicol, 37: 279-292 |
�V�@�I�]���ɂ�鎾�a
�@�l�{�����e�B�A�ɑ��錒�N�e���ɂ��āA�l�X�Ȏ��ԁA�l�X�ȔZ�x�Ŏ��{���ꂽ����{�����e�B�A�ɑ���P����I�����ɂ�����ċz�@�\�e���̍ŏ��Z�x�́A���Î��ɂ�0.5 ppm�Q���ԁA�^�������ɂ�0.1 ppm�Q���Ԃ�����Ă���ŏ��Z�x�ł�����[Folinsbee�� 1978�AHorvath�� 1979�AGoldsmith�� 1969�AKagawa 1984�AAvol�� 1984�ANieding�� 1979]�B
�@�E�Ƃ��I��z�肵���{�����e�B�A�������I�ł́A0.2�`0.5 ppm�A���I����2���ԁ`�R���ԁ^���A�R�`�T�����I�ŁA��ߐ��̌ċz�@�\�e���ɑ���K�����ۂ��ώ@����Ă���[Hackney�� 1977�AFarrell�� 1979�AKulle�� 1982�AHorvath�� 1981]�B
�@������ΏۂƂ������I�����ɂ��āA���I�Z�x0.2�`0.8 ppm�A���I���ԂV���`�X�O���͈̔͂ŋz�����I�������ʂ̕�������[Dungworth�� 1975�ACastleman�� 1977�ABoorman�� 1980�APlopper�� 1979�AGuth�� 1986]�B�C�ǎx�x�E���t�A�a����U���̏������Ɍċz�퉊�ǂ������������ώ@����Ă���B
�@��ߐ��̋@�\�ቺ�ɂƂǂ܂�B
| 1) | Seagle EF(1973): Ozone as an occupational health hazard. Occup Health Nurs, 21: 14-17 |
| 2) | Dungworth DL, et al.(1975): Effect of ambient levels of ozone on monkeys. Fed Proc, 34: 1670-1674 |
| 3) | Castleman WL, et al.(1977): Lesions in respiratory bronchioles and conducting airways of monkeys exposed to ambient levels of ozone. Exp Mol Pathol, 26: 384-400 |
| 4) | Boorman GA, et al.(1980): Pulmonary effects of prolonged ozone insult in rats. Lab Invest, 43: 108-115 |
| 5) | Plopper CG, et al.(1979): Pulmonary alterations in rats exposed to 0.2 and 0.1 ppm ozone�G a correlated morphological and biochemical study. Arch Environ Health, 34: 390-395 |
| 6) | Cavender FL, et al.(1977): Effects in rats and guinea pigs of short-term exposures to sulfuric acid mist, ozone, and their combination. J Toxicol Enviro Health, 3: 521-533 |
| 7) | Guth DJ, et al.(1986): Comparative sensitivity of measurements of lung damage made by bronchoalveolar lavage after short-term exposure of rats to ozone. Toxicol, 40: 131-143 |
| 8) | Holtzman MJ, et al.(1983): Importance of airway inflammation for hyperresponsiveness induced by ozone. Am Rev Respir Dis, 127: 686-690 |
| 9) | Fabbri LM, et al.(1984): Airway hyperresponsiveness and changes in cell counts in bronchoalveolar lavage after ozone exposure in dogs. Am Rev Respir Dis, 129: 288-291 |
| 10) | Folinsbee LJ, et al.(1978):The influence of exercise on the pulmonary function changes due to exposure to low concentrations of ozone. In Environmental stress, Individual human adaptation. 125-145, Academic Press, New York |
| 11) | Horvath SM, et al.(1979): Pulmonary function and maximum exercise responses following acute ozone exposure. Aviat Space Environ Med, 50: 901-905 |
| 12) | Kagawa J.(1984): Exposure-effect relationship of selected pulmonary function measurements in subjects exposed to ozone. Int Arch Ocup Environ Health, 53: 345-358 |
| 13) | Goldsmith JR et al.(1969): Experimental exposure of human subjects to ozone. J Air Poll Control Assoc, 19: 329-330 |
| 14) | Nieding G, et al.(1979): Controlled studies of human exposure to single and combined action of NO2, O3, and SO2. Int Arch Ocup Environ Health, 43: 195-210 |
| 15) | Avol EL, et al.(1984): Comparative respiratory effects of ozone and ambient oxidant pollution exposure during heavy exercise. J Air Poll Control Assoc, 34: 804-809 |
| 16) | Dimeo MJ, et al.(1981): Threshold concentration of ozone causing an increase in bronchial reactivity in humans and adaptation with repeated exposures. Am Rev Respir Dis, 124: 245-248 |
| 17) | Hackney JD, et al.(1977): Adaptation to short-term respiratory effects of ozone in men exposed repeatedly. J Appl Physiol, 43: 82-85 |
| 18) | Farrell BP, et al.(1979):Adaptation in human subjects to the effects of inhaled ozone after repeated exposure. Am Rev Resp Dis, 119: 725-730 |
| 19) | Kulle TJ, et al.(1982): Duration of pulmonary function adaptation to ozone in humans. Am Ind Hyg Assoc J, 43: 832-837 |
| 20) | Horvath SM, et al.(1981): Adaptation to ozone; duration of effect. Am Rev Resp Dis, 123: 496-499 |
| 21) | Holtzman MJ, et al.(1979): Effect of ozone on bronchial reactivity in atopic and nonatopic subjects. Am Rev Respir Dis, 120: 1059-1067 |
| 22) | Saito H, et al.(2000): Laboratory measurement of hazardous fumes and gases at a point corresponding to breathing zone of welder during a CO2 arc welding. Ind Health, 38: 69-78 |
| 23) | Dennis JH, et al.(2002): Control of exposure to hexavalent chromium and ozone in gas metal arc welding of stainless steels by use of a secondary shield gas. Ann Occup Hyg, 46: 43-48 |
| 24) | Tuomi T, et al.(2000): Emission of ozone and organic volatiles from a selection of laser printers and photocopiers. Appl Occup Environ Hyg, 15: 629-634 |
| 25) | Olin AC, et al.(1999): Exhaled nitric oxide among pulpmill workers reporting gassing incidents involving ozone and chlorine dioxide. Eur Respir J, 14: 828-831 |
| 26) | Hall RM , Page E(1999): Ozone exposure at a construction site. Appl Occup Environ Hyg, 14: 203-207 |
| 27) | Romieu I, et al.(1998): Antioxidant supplementation and respiratory functions among workers exposed to high levels of ozone. Am J Respir Crit Care Med, 158: 226-232 |
�W�@�x���]�L�m���ɂ�鎾�a
�@�l�ɑ���e���ɂ��āA�����܂��͒����̔畆�ւ̐ڐG�ɂ��A�畆�����N�������Ƃ�����B �畆�A��ɉe����^���A�ϐF�A���ǁA�p����瑹�����邱�Ƃ�����B0.1 ppm���x���̂��I�ł͑S�g�e���͊ώ@���ꂸ�A��ɑ���y�x�ň�ߐ��̎h����0.1 ppm�ȏ�ł͊ώ@����邱�Ƃ���AACGIH�iAmerican Conference of Government Industrial Hygienists,Inc.�j���E�Ƃ��I���E�l�iTLV-TWA�j�Ƃ���0.1 ppm���������Ă���B
�@�x���[���̑�ӎY���Ƃ��Ẵx���]�L�m���ɒ��ڂ�����`�q�Ő���זE�Ő��Ɋ֘A�����Ƃ��������Ǔ������̕����\����Ă���B�x���[���ɂ��ِ��{�̍זE�����̌������A��ӕ��ł���x���]�L�m����r�t�F�m�L�m���������ǒ`��(microtubule protein)�̃`�I�[����ɋ��L�������邱�Ƃɂ��a�����̕����ɋN�����邱�Ƃ����肳��Ă���[Pfeiffer E , et al. 1996]�B
�@Andreoli et al.�́A�q�g���������p���ɂ��R���b�g�A�b�Z�C�����{���A����0.3 mg/m3�̃x���[���ɂ��I���Ă���K�\�����X�^���h�]�ƈ��ŁA�N���i���Ƃ͓Ɨ��ɔ���I�҂ɔ䂵�ėL�ӂɍ���DNA�̃_���[�W���������BLee et al. (1991) �́A�x���[����ӎY���ł���x���]�L�m����1,2,4-�x���[���g���I�[����DNA���ؒf�������Ǔ������ł͔����������A�����ʂ̃x���[�����I��1, 24, 36���Ԍ�̎��Y�}�E�X�ł�DNA�ؒf���ώ@����Ȃ��������Ƃ���A�����̃x���[�����I�ɂ�钼�ڂ�DNA���ؒf�͔��������A�����Ǔ������̌��ʂ̓K�p�ɂ͒��ӂ�v����Əq�ׂĂ���B
�@�ȏォ��A���Q�Ɋւ��Ă̓I�X�~�E���Ɠ��l�ɁA���̓I�ɔ��������}�����I�ɂ��e���͖��炩�ł��邪�A�������I�Ƃ̈��ʊW�͖��m�ł͂Ȃ��B�x���[���̑�ӕ��Ƃ��Ă̍�p�́A��ς݂ł���B
| 1) | ���ۉ��w�������S���J�[�h(���{���)No. 0779(1993). |
| 2) | �㓡�f�A�r�c���V�A����Y��(1977).�Y�ƒ��ŕ֗�.881�㎕��o��.���� |
| 3) | Pederson DH, et al.(2001): Populations at risk. In Bingham E, Cohrssen B, Powell CH eds.: Patty's Toxicology. 5th ed. Vol 8, 995-996, John Wiley & Sons, Inc. New York |
| 4) | American Conference of Governmental Industrial Hyigienists. Documentation of the TLVs nd BEIs. ACGIH, Cincinnati(2001) |
| 5) | Seung SA, et al.(1998): The relative importance of oxidative stress versus arylation in the mechanism of quinone?induced cytotoxicity to platelets. Chem Biol Interact, 113(2): 133?144 |
| 6) | Tapper MA, et al.(2000):Depletion of cellular protein thiols as an indicator of arylation in isolated trout hepatocytes exposed to 1,4?benzoquinone. Toxicol Sci, 55(2): 327?334 |
| 7) | Misra UK, et al.(1998): Alterations in calcium metabolism in murine macrophages by the benzene metabolite 1,4?benzoquinone. Toxicol Appl Pharmacol,151(1): 1?8 |
| 8) | Pfeiffer E(1996): Interaction of p?benzoquinone and p?biphenoquinone with microtubule proteins in vitro. Chem Biol Interact, 102(1): 37?53 |
| 9) | Andreoli C, et al.(1997): Detection of DNA damage in human lymphocytes by alkaline single cell gel electrophoresis after exposure to benzene or benzene metabolites. Mutat Res, 377(1): 95?104 |
| 10) | Lee EW, Garner CD(1991): Effects of benzene on DNA strand breaks in vivo versus benzene metabolite?induced DNA strand breaks in vitro in mouse bone marrow cells. Toxicol Appl Pharmacol,108(3): 497?508 |
�X�@�V�f���[�V�X�i�S�����ǁj
�@���E�̋������Y�̂�����90���ȏオ�S�|���S�������ł���B�䂦�ɓS�������̐E�Ɛ����I�͍L�͈͂ɂ킽���Ă���B�S�z�R��S�|�֘A��Ƃł́A�S�̕��Ӎ�Ƃ�A�n�ڍ�ƁA�S�ܗL���̐ؒf�E�ό`��ƂȂǂœS������̂��I����B�������A�����S���I��Ƃ̑啔���ł́A�����ɑ��̑����̕����ɂ����I����Ă���A�S�z�������̌��N�e���ɒ��ڂ��������͂��������Ȃ��B
�@�P�Ȃ�S�����ɂ��x�V�f���[�V�X�݂̂ł́A���̕����ɂ�邶��x�ǂɌ�����ċz�@�\�ቺ��A���ې����B���ω��Ȃǂ̏����ɖR�����Ƃ���Ă������A�����H��S�z�R�v�ɂ����鍂�p�x�̔x���������̉u�w�I��A�����ߒ��ɂ����銈���_�f�̊֘A�����炩�ɂȂ��Ă���ɂ�āA�S�C�I�����̂��̖̂������d�v�������悤�ɂȂ����B
�@�������A���������u�w�����ɂ����Ă��A�x���̃��X�N�㏸���F�߂�ꂽ�͓̂S�|�J���҂ł���A�������鑼�̂��������I�̉e�������O���邱�Ƃ��ł��Ȃ��B�܂��A�K�Ȕ�r�ΏƂ�ݒ肷��ƗL�Ӎ������ł��邱�Ƃ�����ȂǁA��������̊W�ł��邱�Ƃ��ے�ł��Ȃ��B�V�f���[�V�X�Ɋւ��邱��܂ł́̕A�z�R�J���҂╲������I�J���҂Ɋւ�����̂ł���A�Ώێ҂̑啔���͊��ɂ���x���̑����m�̗L�Q�������I�ɑ��錒�N�Ǘ��̑ΏۂƂȂ��Ă���̂ŁA����͕������I�ɂ�����S�̍�p���𖾂��邱�Ƃ��K�v�ł���ƍl������B
| 1) | Nemery B(1998): Lung disease from metal exposure. In Occupational Lung Disease, edited by Banks DE. and Parker JE. 292-293,Chapman & Hall, Lippincott Williams & Wilkins Publishers, Philadelphia |
| 2) | Funahashi et al.(1988): Welders'pneumoconiosis;tissue elemental microanalysis by energy dispersive X-ray analysis. Br J Ind Med, 45: 14-18 |
| 3) | Lasfargues et al.(1991): Siderose pulmonaire et risques respiratories a long terme du soudage a l'arc. Rev Mal Res, 8: 304-306 |
| 4) | Billings and Howard(1993): Occupational siderosis and welder's lung ; a review Monaldi Arch Chest Dis, 48: 304-314 |
| 5) | Nestor S(1999), Inhalation of Inorganic Dust. Fraser and Pare's Diagnosis of Diseases of The Chest,4th ed., 2452-2454, W.B.Sanders Co,Philadelphia |
| 6) | Smith GH, et al.(1987): Respiratory cancer and air pollution from iron foundries in a Scottish town: An epidemiological and environmental study. Br J Ind Med, 44: 95-802 |
| 7) | Kelleher, et al.(2000): Inorganic dust pneumonias; the metal-related parenchymal disorders. Environ Health Perspect, 108 (Suppl 4): 685-96 |
| 8) | Weinberg ED(1999): The development of awareness of the carcinogenic hazard of inhaled iron. Oncol Res, 11(3): 109-113 |
| 9) | Dreyfus JR(1936): Lungencarcinom bei Geschwuste nach Inhalation von eisenoxyhaltigem Staub in der Jugend. Zeit Klin Med, 130: 256-260 |
| 10) | Boyd JT, et al.(1970): Cancer of the lung in iron ore (haematite) miners. Br J Ind Med, 27: 275-280 |
| 11) | Icso J, et al.(1994): Lung cancer among iron ore miners in east Slovakia: A case control study. Occup Environ Med, 51: 642-643 |
| 12) | Antoine D, et al.(1979): Le cancer bronique des mineurs de fer de Lorraine peut-il etre considere comme une maladie professionelle? Rev Fr Mal Respir, 7: 63-65 |
| 13) | Turner HM, Grace HG(1993):An investigation into cancer mortality among males in certain Sheffield trades.J Hyg, 838: 90-103 |
| 14) | Blot WJ, et al.(1983): Lung cancer among steel workers. Am J Epidemiol, 117: 706-715 |
| 15) | Sherson D, et al.(1991): Cancer incidence among foundry workers in Denmark. Arch Environ Health, 46: 75-81 |
| 16) | Gibson ES, et al.(1977): Lung cancer mortality in a steel foundry. J Occup Med, 19: 807-812 |
| 17) | Guest L(1978): The endogenous iron content, by Mossbauer spectroscopy, of human lungs-II. Lungs from various occupational groups. Ann Occup Hyg, 21: 151-157 |
| 18) | Corhay JL, et al.(1992): Iron content in human alveolar macrophages. Eur Respir J, 5: 804-809 |
| 19) | Campbell JA(1940): Effects of precipitated silica and of iron oxide on the incidence of primary lung tumors in mice. Br Med J, 2: 275-280 |
| 20) | Pott F, et al.(1987): Carcinogenecity studies on fibres, metal compounds, and some other dust in rats. Exp Pathol, 32: 129-152 |
| 21) | Steinhoff D, et al.(1991): Carcinogenesis studies with iron oxides. Exp Pathol, 43: 189-194 |
| 22) | Castranova V, et al.(1997): Augmentation of pulmonary reactions to quartz inhalation by trace amounts of iron-containing particles. Environ Health Perspect, 105(Suppl. 5): 1319-1324 |
| 23) | Ghio AJ, et al.(1992): Role of surface complexed iron in oxidant generation and lung inflammation induced by silicates. Am J Physiol, 263: L511-L518 |
| 24) | Goodglick LA, Kane AB(1986): Role of reactive oxygen metabolites in crocidolite asbestos toxicity to mouse macrophages. Cancer Res, 46: 5558-5566 |
| 25) | Keeling B, et al.(1994): Iron enhances uptake of mineral particles and increases lipid peroxidation in tracheal epithelial cells. Am J Respir Cell Mol Biol, 10: 683-688 |
| 26) | Lay JC, et al.(1996): Alveolar macrophages accumulate iron ferritin after in vivo exposure to iron or tungsten dusts. J Lab Clin Med, 127: 401-409 |
| 27) | Stokinger HE(1984): A review of world literature finds iron oxides noncarcinogenic. Am Ind Hyg Assoc J, 45: 127-133 |
| 28) | Zhang Q, et al.(2002): Roles of bioavailable iron and calcium in coal dust-induced oxidative stress; possible implications in coal workers' lung disease. Free Radical Research, 36(3): 285-294 |
| 29) | Xu Z., et al.(1996): Cancer risks among iron and steel workers in Anshan, China. Part I: Proportional mortality ratio analysis, Part II: Case-control studies of lung and stomach cancer. Am J Ind Med, 30: 1-6,7-15 |
| 30) | Stern FB, et al.(1997): Proportionate mortality among unionized construction ironworkers. Am J Ind Med, 31: 176-187 |
| 31) | Danielsen TE, et al.(1998): Incidence of lung cancer among shipyard welders investigated for siderosis. Int J Occup Environ Health, 4(2): 85-88 |
10 �����ǐ��x�����i�b�n�o�c�j
�@�����ǐ��x����(chronic obstructive pulmonary disease: COPD)�Ƃ́A�����C�ǎx���A�x�C��܂��͗��҂̕����ɂ���N�����ǐ����C��Q������Ƃ��鎾���ł���B�ʏ�ACOPD�ɂ��ǐ����C��Q�͂������Ɛi�s���A���Âɔ��������A�s�t�I�ł��邱�Ƃ������ł���B
�@����̕��������̌��ʁA�����_�ɂ�����E�Ɛ�COPD�ɂ��Ă̒m���͉��L�̂悤�ɗv���B
�P�D����̕������K�X���ւ̐E�Ƃ��I��COPD�̗U���ƂȂ肤��B
�Q�D���̊�^�x�͋i���ɂ���^�x�����i�������Ȃ�j�������B
�R�D�i���ƍ�Ɗ��̑��݊֘A�́i�����j���݂���B
�S�D�P��̌����ł͂Ȃ����d�q�b�g�imultiple hit�j �������Ó��ł���B
�T�D���̐i�W�ɂ͚b���̊֗^������ꍇ�Ɩ����ꍇ�Ƃ���B
�U�D�b�����i�������Ȃ��Ǘ�͂܂�ł���B
�@Medline ����{�Ƃ����_���̃f�[�^�x�[�X�i1965?2002�j�ɂ��A�uOccupational disease�v�ƁuCOPD�v�Ō��������Ƃ���254�̘_�����������ꂽ�B�������A�����ɂ́u�p��_���v�Ƃ������������A�����Ǔ������Ɋւ�����̂͏��O�����B
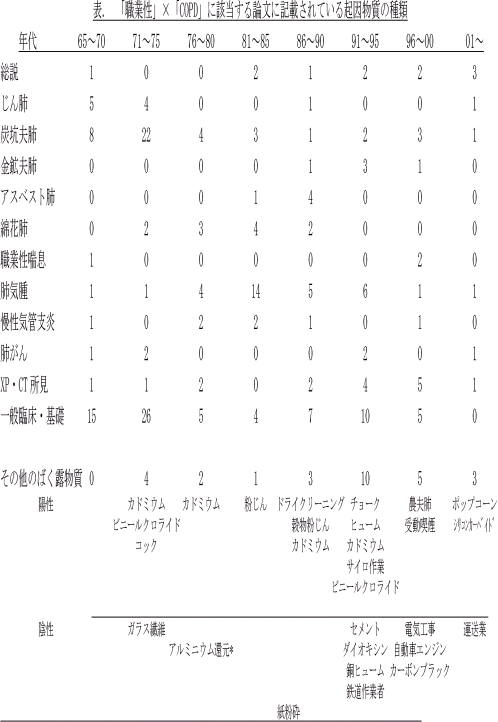
�@�ʓY �\�iP.47�j�ɂT�N���̘_���̌X���Ƃ��Ď����B�a���w�I���x�C�����̂Ƃ���COPD�̊T�O���蒅�����̂�1960�N��ł���B�u�E�Ɛ��v�ƁuCOPD�v�̌����ɊY������_����1965�`1970�N�A1971�`1975�N�́u����x�v�A�u�Y�B�v�x�v�A�u���z�v�x�v�Ɋւ��錤���E����̂ƂȂ�B
�@����̕������r���[�Œ��ڂ��ꂽ�ACOPD�̌����ƂȂ肤��E�Ƃ���I�����́A�ÓT�I�ɒm���Ă���J�h�~�E���A�����r�j�[���⍒��������ȊO�ł́A�|�b�v�R�[���܋l�ߍ�ƁA�t�@�[�X�g�t�[�h�X�̃R�b�N�A���t�̃`���[�N���A�h���C�N���[�j���O�A�i���A�V���R���J�[�o�C�h���ł������B�������Ȃ���A��������������ʊW�ɂ��Ċm�����ꂽ���̂Ƃ͂����Ȃ��B���ɁA�|�b�v�R�[���A�R�b�N�A�`���[�N�ɂ��ẮA�Y����Ǝ҂̐��ɔ䂵�ĕႪ���Ȃ��A���ʊW�ɂ��Ă͋^�₪�c��B
| 1) | �k���@�@(1999)�F COPD?�����ǐ��x�����D�ʍ��E��w�̂���݁A�ċz�펾��Ver.3: 345-347 |
| 2) | Hendrick DJ (1996): 0ccupation and chronic obstructive pulmonary disease (COPD). Occupational lung disease 9. Thorax, 51: 947-955 |
| 3) | Burge PS (1994): 0ccupation and chronic obstructive pulmonary disease (COPD). Eur Respir J, 7: 1032-1034 |
| 4) | Schachter EN, et al. (2001): Occupational airway diseases. Reviews on Environmental Health, 16(2): 87-95 |
| 5) | Romundstad P, et al. (2002): Non-malignant mortality among Norwegian silicon carbide smelter workers. Occup Environ Med, 59:(5): 345-347 |
| 6) | Parmer AJ, Essen SV(2002): Rapidly progressive, fixed airway obstructive disease in popcorn workers; a new occupational pulmonary illness? J Occup Environ Med, 44(3): 216-218 |
| 7) | Mak GK, et al.: Occupational inhalant exposure and respiratory disorders among never-smokers referred to a hospital pulmonary function laboratory. Am J Med Sci, 322(3): 121-126 |
| 8) | Fleming DM, Charlton JR (2001): The prevalence of asthma and heart disease in transport workers: a practice-based study. Br J Gen Pract, 51(469): 638-643 |
| 9) | Nurminen M, Karjalainen A (2001): Epidemiologic estimate of the proportion of fatalities related to occupational factors in Finland. Scand J Work Environ Health, 27(3): 161-213 |
| 10) | Erkinjuntti-Pekkanen R, et al (1998): Long-term risk of emphysema in patients with farmer's lung and matched control farmers. Am J Respir Crit Care Med, 158(2): 662-665 |
| 11) | Kelsh MA, Sahl JD (1997): Mortality among a cohort of electric utility workers. Am J Ind Med, 31(5): 534-544 |
| 12) | Casale R, Pasqualetti P (1997): Cosinor analysis of circadian peak expiratory flow variability in normal subjects, passive smokers, heavy smokers, patients with COPD and patients with interstitial lung disease. Respiration, 64(4): 251-256 |
| 13) | Park RM, Mirer FE(1996): A survey of mortality at two automotive engine manufacturing plants. Am J Ind Med, 30(6): 664-673 |
| 14) | Reid PJ, Sluis-Cremer GK (1996): Mortality of white South African gold miners. Occup Environ Med, 53: 11-16 |
| 15) | Kupper HU, et al. (1996): Effects on the lung function of exposure to carbon black dusts. Int Arch Occup Environ Health, 68: 478-483 |
| 16) | Chatterjee S, et al.(1995): Pulmonary function of different categories of chronic obstructive pulmonary disease in railway workers of Eastern India.J UOEH, 17(3): 173-189 |
| 17) | Ohtsuka Y, et al.(1995): Three cases of idiopathic interstitial pneumonia with bullae seen in schoolteachers. Am J Ind Med, 28(3): 425-435 |
| 18) | Ostiguy G, et al.(1995): Respiratory health of workers exposed to metal dusts and foundry fumes in a copper refinery. Occup Environ Med, 52(3): 204-210 |
| 19) | Vestbo J (1993): Predictors of mortality, COPD morbidity and respiratory cancer?with special reference to respiratory symptoms, lung function, and occupational exposure to cement dust. Dan Med Bull, 40(1): 1-16 |
| 20) | Calvert GM, et al. (1991): Evaluation of chronic bronchitis, COPD, and ventilatory function among workers exposed to 2,3,7,8- tetrachlorodibenzo-p-dioxin. Am Rev Respir Dis, 144(6): 1302-1306 |
| 21) | Wong O, et al.(1991): An industry-wide epidemiologic study of vinyl chloride workers, 1942-1982, Am J Industrial Med, 20: 317-334 |
| 22) | Toren K, et al. (1991): Mortality from asthma, COPD, respiratory system cancer, and stomach cancer among paper mill workers; a case-referent study. Am J Ind Med, 19(6): 729-37 |
| 23) | Blair A, et al. (1990): Cancer and other causes of death among a cohort of dry cleaners. Br J Ind Med, 47(3): 162-168 |
| 24) | Becklake MR(1989): Occupational exposures: evidence for a casual association with chronic obstructive pulmonary disease. Am Rev Respir Dis, 140: S85-91 |
| 25) | Milham S (1979): Mortality in aluminum reduction plant workers. J Occup Med, 21(7): 475-480 |
| 26) | Horne SL, et al. (1986): Pulmonary function in Pi�l and MZ grainworkers. Chest, 89(6): 795-9 |
| 27) | Miller A, et al. (1975): Changes in pulmonary function in workers exposed to vinyl chloride and polyvinyl chloride. Ann NY Acad Sci, 246:42-52 |
| 28) | Irwin L Stoloff (1973): Bullous lung disease in short order cooks. J Occup Med, 15(3): 202-203 |
| 29) | Gross P, et al. (1971): Lungs of workers exposed to fiber glass. Arch Environ Health, 23: 67-76 |
| 30) | Morgan JM, et al. (1971): Tissue cadmium and zinc content in emphysema and bronchogenic carcinom. J Chron Dis, 24: 107-110 |
�i�ʓY�j
11�@�؍ނ̐o���ɂ�邪��
�@IARC���m�O���t�V���[�Y62�uWood Dust and Formaldehyde�v�i1995�N���s�j�ɂ��A�@�o����ѕ��@�o�̑B���́A�؍ޕ�����A���Ɍ��ؕ�������I�ƈ��ʊW�����邱�ƁA�@�o����ѕ��@�o�̝G��������́A�B���ɔ�ׂ�Ƃ��I�ɂ�郊�X�N�㏸�͏��Ȃ��A���ʊW�͎x������Ȃ����ƁA�@�����Ɩ؍ޕ�����ւ̐E�Ƃ��I�Ƃ̊֘A�����������ꂽ���Ƃ��L�ڂ���Ă���B�Ȃ��A���������A�����A�����A�x�A�����p����ё����n�A�݁A�咰�܂��͒����̂���ɂ��ẮA�؍ޕ�����̐E�Ƃ��I�Ƃ̈��ʊW�͏ؖ�����Ȃ������Ƃ���Ă���B
�@IARC���m�O���t���o�ł��ꂽ�ȍ~�̌����ł��A�؍ޕ�������I�ƕ@�o����ѕ��@�o�����Ƃ̊֘A��F�߂�������B�܂��A��r�I��Z�x�̖؍ޕ�������I�Ɠ��������ې��x�E���iCFA�j�Ƃ̊֘A����F�߂������A�X�Ȃ錟���̕K�v������B
�@�܂��A���{�ɂ�����؍ޕ�����̔�����e���̉u�w�I�����ɂ��ẮA��H�E�l��Ƌ���E�l�ł̕��@�o���̗L�ӂȃ��X�N�㏸���������ꂽ�Ǘ�Ώƌ����̕��U���������x�ŃR�z�[�g�����͌�������Ȃ������B�m�F�ł��������ōł��V�����������\��1989�N�ɏo���ꂽ���̂ŁA����Ȍ�͕������悤�ł���B�킪���̕��@�o����̉u�w�I�ȓ����Ƃ��āA�j���Ƃ���{���̝G�������������A���Ă�⿍����̑B�����������ƂƑΏƓI�ł��邪�A���̗��R�͖��炩�ł͂Ȃ��B
�@����A�؍ނ̎�ޕʂɌ������I�̒��x�A�l���Ȃǂ�����ƂƂ��ɁA���ڍׂȉu�w�����̎��{���]�܂��B
| 1) | International Agency for Research on Cancer�i1995�j�F IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. Wood Dust and Formaldehyde. Volume 62, 94-165, 191-194,IARC, Lyon |
| 2) | Van den Oever R�i1996�j�F Occupational exposure to dust and sinonasal cancer. An analysis of 386 cases reported to the N.C.C.S.F. Cancer Registry. Acta Otorhinolaryngol Belg, 50: 19-24 |
| 3) | Szadkowska-Stanczyk I and Szymczak W�i2001�j�F Nested case-control study of lung cancer among pulp and paper workers in relation to exposure to dusts. Am J Industr Med, 39: 547-556 |
| 4) | Weiderpass E, et al�i2001�j�F Occupational exposures and cancers of the endometrium and cervix uteri in Finland. Am J Industr Med, 39: 572-580 |
| 5) | Kauppinen T, at al�i2001�j�F Occupational exposure to carcinogens in Estonia, Latvia, Lithuania and the Czech Republic in 1997. Scand J Work Environ Health, 27: 343-345 |
| 6) | Hubbard R�i2001�j�FOccupational dust exposure and the aetiology of cryptogenic fibrosing alveolitis. Eur Respir J, 18(Suppl.32): 119s-121s |
| 7) | Fukuda K, et al.�i1987�j�FSquamous cell cancer of the maxillary sinus in Hokkaido, Japan; a case-control study. Br J Industrial Med, 44: 263-266 |
| 8) | Fukuda K, Shibata A�i1988�j�FA case-control study of past history of nasal diseases and maxillary sinus cancer in Hokkaido, Japan. Cancer Res, 48: 1651-1652 |
| 9) | Shimizu H, et al �i1989�j�FChronic sinusitis and woodworking as risk factors for cancer of the maxillary sinus in northeast Japan. Laryngoscope, 99: 58-61 |
| 10) | Takasaka T, et al.�i1987�j�FA case-control study of nasal cancers. An occupational survey. Acta Otolaryngol (Stockh), 435(Suppl.): 136-142 |
| 11) | Yoshimura T, et al.�i1983�j�FNasal cancer mortality in areas with a high proportion of wood and furniture workers in Japan. J UOEH, 5(4): 433-439 |
| 12) | �������i2002�j�F��90��ILO����ō̑����ꂽ���E�����E�c�菑�D(1)�J�����S�q�����i155���j�́Z��N�c�菑�A(2)�E�ƕa�ꗗ�\�Ȃ�тɋƖ��ЊQ�E�E�ƕa�̋L�^�ƕɊւ��銩���i194���j�D���E�̘J���@52�i8�j�F44-49 |
| 13) | �Y�ƈ�ȑ�w�Y�Ɛ��ԉȊw�������Ė�i2002�j�F�J���ЊQ����ѐE�Ɛ����a�̋L�^�ƒʒm�|ILO�s���w�j�|�D76-86, �J��������C���� |