| (1) |
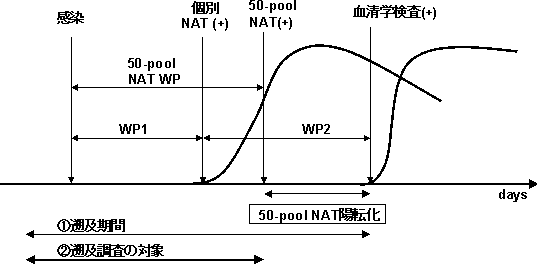
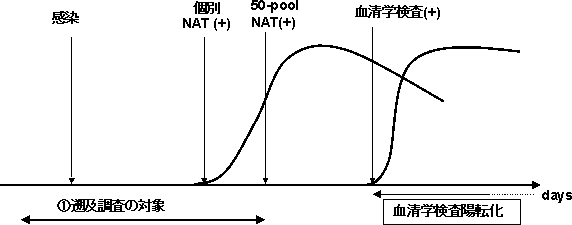
遡及調査期間
病原体はその種類によって生体内での増殖速度、ウインドウ期間、検査法によって陽性になる期間がそれぞれ異なる。したがって、病原体の種類及び検査法による陽性時期等に基づいて遡及調査期間を設定した(資料添付)。
| 病原体 |
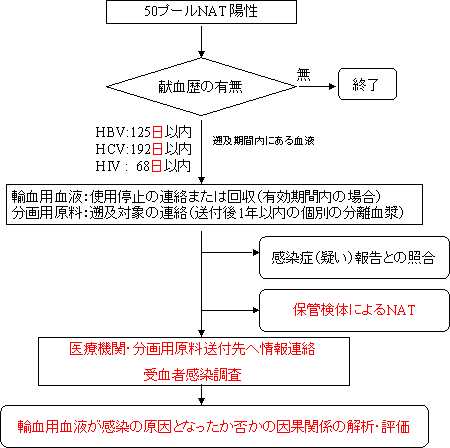
50プールNAT陽転時 |
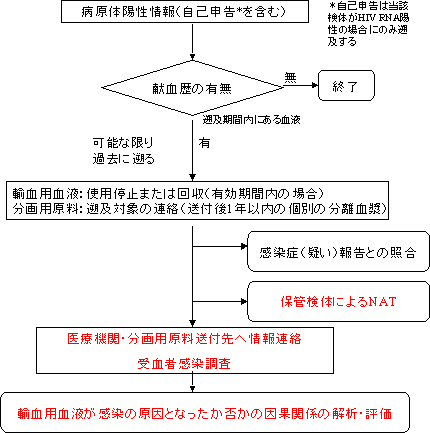
血清学的検査陽転時 |
| HBV |
最長遡及期間は125日以内とする。
過去の直近(前回)及び前回から過去92日以内のすべての輸血用血液、原料血漿を遡及する。 |
可能な限り過去に遡り、過去の直近(前回)及び前回から過去92日以内のすべての輸血用血液、原料血漿を遡及する。 |
| HCV |
最長遡及期間は192日以内とする。
過去の直近(前回)及び前回から過去50日以内のすべての輸血用血液、原料血漿を遡及する。 |
可能な限り過去に遡り、過去の直近(前回)及び前回から過去50日以内のすべての輸血用血液、原料血漿を遡及する。 |
| HIV |
最長遡及期間は68日以内とする。
過去の直近(前回)及び前回から過去58日以内のすべての輸血用血液、原料血漿を遡及する。 |
可能な限り過去に遡り、過去の直近(前回)及び前回から過去58日以内のすべての輸血用血液、原料血漿を遡及する。 |
| 梅毒 |
|
可能な限り過去に遡り、過去の直近(前回)及び前回から過去35日以内のすべての輸血用血液、原料血漿を遡及する(ただし、FFPと4日以上冷蔵保存されていたMAPを除く)。 |
|
| (2) |
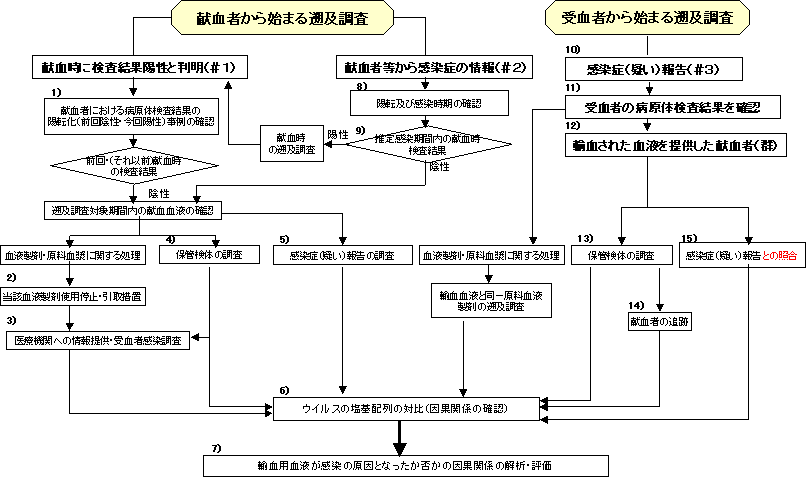
検体及び記録の保管
本ガイドラインに示す遡及調査措置がとれるよう、献血血液の検体、原料血漿の保管を行うこととする。また、献血者、輸血用血液、原料血漿の供給及び使用に関する記録等を保管することとする。なお、献血血液の検体及び記録の保管期間は、法令等の規定によるものとする。
|
| (3) |
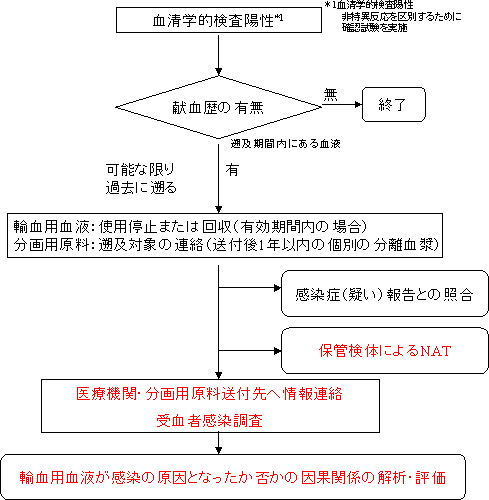
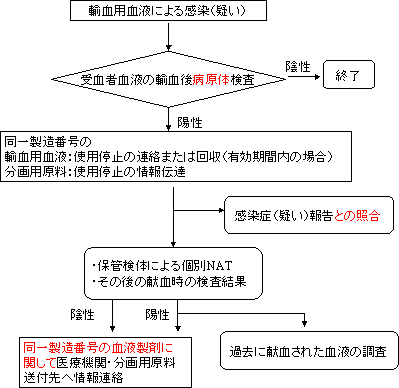
感染・伝播拡大防止のための通知
遡及調査が必要となる事実を知り得た時点で、当該輸血用血液の供給を中止するなど、当該輸血用血液の使用による感染・伝播の拡大防止を講ずることとする。
また、遡及調査対象となった輸血用血液や原料血漿が供給されている関連医療機関や分画製剤製造業者には、速やかに通知することとする。
|
| (4) |
感染に係る検査方法
保管検体を使用した感染に係る検査及びその評価は、その時機における最新の適切な技術を用いて行わなければならない。
|
| (5) |
プライバシーの保護
遡及調査を行うにあたり、献血者、輸血用血液を投与した受血者(患者)に係る情報等の取扱いに関し十分に配慮し、そのプライバシーの保護を確保することとする。
|
| (6) |
遡及調査の記録と保存
遡及調査の結果はすべて記録し、保存しなければならない。
|
| (7) |
遡及調査体制の整備
本ガイドラインの実施にあたり適切な体制を整備することとする。
|
| (8) |
医療機関の協力
この遡及調査を効果的に実施するためには、医療機関における輸血用血液の記録の作成が必須であり、また、輸血前患者検体を保管し、輸血後の感染症検査を実施することが必須である。 |