| 資料NO.2 |
| 薬事・食品衛生審議会医薬品等安全対策部会 伝達性海綿状脳症調査会 事務局 |
| 1 米国産原材料の現状 |
| (1) | 医薬品原材料における米国産の割合は、例えば、遺伝子組換え医薬品、ワクチンなどの培養に用いるウシ血清全体の45%、ゼラチンカプセルでは30%、胆汁酸では50%を占めている。医薬品等の製造原料は大きく米国に依存している状態。 |
| (2) | 米国産ウシ原料を含む製品の製造を予防的に直ちに禁止すれば、約2600品目の製品に支障が生ずる。(HIV治療薬、遺伝子組換え凝固因子製剤等を含む多数の製品) |
| (3) | 米国でのBSE発生以前から、日本の医薬品規制では、脳、脊髄、眼、腸等のリスクの高い部位の使用は禁止されており、医薬品等において直ちに保健衛生上のリスクがあるとは考えられていない。 |
| 2 今後の措置の考え方 |
| (1) | これまでの安全対策の基本を踏まえ、米国産の原材料の使用状況からみた原材料の切替えによる医療上のデメリットの発生を防止しつつ、米国産の原材料から他の原材料への切替えを速やかに進める。 |
| (2) | 大供給国の米国のBSE発生を機に、ウシ由来原材料自体を除去し、ウシ以外、動物以外の原材料を使用した製品への転換を進める(政策的に優先審査とする)。 |
| (3) | ウシ由来原材料の除去が困難な製品は、BSEの相対リスクの評価に基づく優先順位に従い、他の原産国等の原材料への切替えを進める。 |
| 3 製品の切替え等の措置 |
| (1) | ウシ由来原材料を除去等の製品の切替えにつき、一部変更承認申請を優先審査扱いとして切替えを促進する。(下図に期限の詳細) 例えば、遺伝子組換え医薬品の製造培地からのウシ血清除去
|
||||||||||||||
| (2) | ウシ由来原材料の除去が困難な場合は、原材料−製造工程−投与経路−使用期間によるリスクを定量的に評価し、BSEの理論的伝播リスクが高いものから、すみやかに、米国産原材料からの原産国等(※)の切替えの措置を実施することとする。以下は、切替え期限。
|
(参考) 切替えに関するタイムフレーム
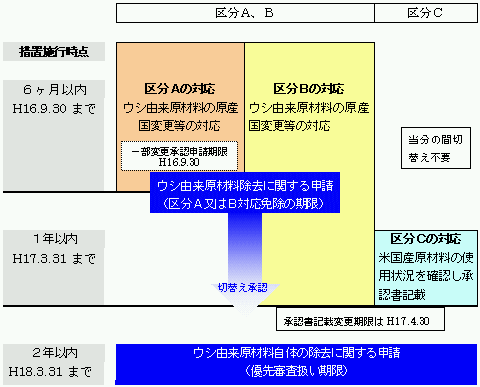
| ※ | 原料の切替えに不可避的に時間を要する場合は、切替え時期を明示し、リスク評価を個別に行い(要一部変更承認)、使用者に対して情報提供と理解を求める。 |
| 4 医薬品等のリスク分類 |
| 区分 | 製品類別 | 牛原料の用途 ウシの成分 |
経路 | リスク値 | |
| リスクの目安 : 感染動物の危険部位 | 脳内 | 1 | |||
| 区分A 71品目 |
1 | 遺伝子組換え品(細胞培養) 例:血栓溶解剤、血液凝固因子 |
細胞培養培地等 血清、インスリン等 |
注射 | 1/10万〜 1/10億 程度 |
| 2 | 成分抽出製剤 例:コンドロイチン硫酸 |
抽出成分 気管軟骨、アプロチニン(肺)等 |
注射 | ||
| 3 | 植込み用具 例:組織補填コラーゲン |
成分・組織 皮又は骨由来コラーゲン |
植込 | ||
| 区分B1 1754品目 |
4 | ゼラチン 例:HIV治療薬、インフルエンザ薬等を含む各種医薬品のカプセル基材 |
カプセル・安定剤 骨又は皮由来ゼラチン |
経口等 注射 |
1/100億以上 (脊柱骨リスクを加味) |
| 区分B2 306品目 |
5 | 成分抽出製剤 例: 胆汁末、臓器エキス |
抽出成分 胆汁、胆石、肝臓、心臓、気管軟骨等 |
経口等 | 1/100億 〜 1/1000億 程度 |
| 6 | 低分子製剤(*)例:コール酸類 | 粗原料 胆汁酸誘導体 |
注射 | ||
| 7 | 菌培養による製剤 例 ワクチン、ステロイド剤 |
培養培地 肉エキス、血清、肝臓エキス、乳等 |
注射 | ||
| 区分C 449品目 |
8 | 遺伝子組換え品(細胞培養)菌培養による製剤 例:血栓溶解剤、成長ホルモン、インスリン |
セルバンク・シード 血清等 |
注射 | 1/1000億 未満 |
| 9 | 菌培養による製剤 例 ホルモン剤、ステロイド、抗生物質 |
培養培地等 肉エキス、血清、肝臓エキス、乳等 |
経口等 | ||
| 10 | 低分子製剤(*)例:コール酸類 | 粗原料 胆汁酸誘導体 |
経口 | ||
| 11 | 外用製剤 例:抗生物質、ステロイド、消炎剤 |
基材、成分等 コラーゲン、肉エキス、血清、肝臓エキス、乳等 |
経皮 | ||
原料中のプリオンが製品にすべて移行すると仮定した最悪のシナリオに基づくリスク評価
|
| 5 制度化までの日程等 |
| (1) | 平成16年2月13日 薬事・食品衛生審議会伝達性海綿状脳症調査会 |
| (2) | 平成16年2月23日 薬事・食品衛生審議会生物由来技術部会 |
| (3) | 平成15年度内に改正基準の告示予定(薬事法第42条「生物由来原料基準」改正) |
| 6 その他規制上の取扱い |
| (1) | 1986年以前に採取されたウシ原料は、本措置の対象としない。 |
| (2) | 区分Bであっても、1年以内の切替え期間中は、原料動物に動物性飼料が使用されていないことを製造業者等においても、確認に努める。 |
| (3) | 原材料のすみやかな切替えを優先するため、改正予定の「生物由来原料基準」(法第42条)が担保される限り、承認書上の原産国記載等については、切替え事後での変更手続きを可とする。 |
| 資料 |
| 区分 | 類別 | ウシ原料使用方法 | 投与 経路 |
リスク 合計値 |
|
| リスクの目安 : 感染動物のリスクの高い部位 | 脳内 | +7 | |||
| 区分A | 1 | 遺伝子組換え・細胞培養医薬品 | 細胞培養等(*1) | 注射 | +2 |
| 2 | 遺伝子組換え・細胞培養医薬品 | 親和性カラム(*1) | 注射 | -2 | |
| 3 | 成分抽出製剤 | 抽出成分 | 注射 | 0 | |
| 4 | 植込み用具 | 成分・組織 | 植込 | -1 | |
| 区分B1 | 5 | 経口製剤(ゼラチン) | カプセル等 | 経口 | 0〜−4 |
| 6 | 注射剤(ゼラチン) | 安定剤 | 注射 | 0〜−4 | |
| 区分B2 | 7 | 成分抽出製剤 | 抽出成分 | 経口 | -3 |
| 8 | 低分子製剤(*2) | 成分粗原料 | 注射 | -4 | |
| 9 | 菌培養医薬品/ワクチン | 培養 | 注射 | -4 | |
| 区分C | 10 | 細胞培養医薬品 | MCB/WCBのみ | 注射 | −4− |
| 11 | 菌培養医薬品/ワクチン | シードのみ | 注射 | -6 | |
| 12 | 菌培養医薬品/ワクチン | 培養 | 経口 | -7 | |
| 13 | 低分子製剤(*2) | 成分粗原料 | 経口 | -7 | |
| 14 | 外用製剤 | 基材、成分等 | 経皮 | −4< | |
| ※ | 上記のリスク計算は、原材料の中にプリオンが仮に存在した場合、プリオンが失われずに製品まで至ると仮定したもの。(平成15年7月開催伝達性海綿状脳症調査会資料を元に計算) | |
| ※ | (*1)は製造工程で原材料の濃縮の可能性がある工程を含むもの | |
| ※ | (*2)製造工程の一定のリスク減少効果が認められているもの |
表2 具体的な区分毎の製品群について
| 区分 | 類別 | ウシ原料使用方法 | 経路 | 品目数 | ||
| 区分A | 1 | 細胞培養医薬品 | 培養(*) | 注射 | 48 | |
| 2 | 細胞培養医薬品 | アフィニティカラム(*) | 注射 | |||
| 薬 | 血栓溶解剤(遺伝子組換え) | 血液凝固因子製剤 | ||||
| 抗悪性腫瘍抗体医薬品(遺伝子組換え) | 再生不良性貧血治療薬(遺伝子組換え) | |||||
| 腎性貧血改善剤(遺伝子組換え) | インターフェロン(遺伝子組換え) | |||||
| 抗リウマチ薬(遺伝子組換え) | 免疫抑制剤(遺伝子組換え) | |||||
| G−CSF製剤(遺伝子組換え) | インスリン(遺伝子組換え) | |||||
| 3 | 成分製剤 | 抽出成分 | 注射 | 9 | ||
| 薬 | 抗悪性腫瘍剤 | 高カロリー輸液用微量元素製剤 | ||||
| 血栓溶解剤 | 組織接着剤 | |||||
| コンドロイチン硫酸(注射・点眼) | ||||||
| 4 | 植込み用具 | 成分・組織 | 植込 | 14 | ||
| 具 | 組織補填等コラーゲン | |||||
| ウシ心のう膜 | ||||||
| 区分B1 | 5 | 経口製剤 | カプセル | 経口 | 1749 | |
| 薬 | 抗生物質、抗菌剤 | 神経障害治療薬 | ||||
| 癌治療薬 | パーキンソン病治療薬 | |||||
| HIV治療薬 | 精神分裂病治療薬 | |||||
| 免疫抑制剤 | 抗うつ剤 | |||||
| 抗インフルエンザ薬 | 自律神経剤 | |||||
| 血栓溶解剤 | 抗てんかん薬 | |||||
| 不整脈薬 | カルシウム拮抗薬 | |||||
| 心房細動等治療薬 | 高脂血症改善薬 | |||||
| 虚血性心疾患治療薬 | 降圧剤 | |||||
| 狭心症治療薬 | 抗アレルギー薬 | |||||
| 不整脈薬 | 真菌症治療薬 | |||||
| 心不全治療薬 | 甲状腺機能検査薬 | |||||
| 強心配当体 | 利胆及び鎮痙 | |||||
| 循環改善薬 | ビタミン欠乏症 | |||||
| 微小循環系賦活剤 | 解熱鎮痛剤 | |||||
| 抗プラスミン剤 | 鎮痙薬 | |||||
| ウイルソン病 | 骨粗鬆症 | |||||
| 抗炎症薬 | 肝機能改善薬 | |||||
| 抗潰瘍薬 | 止しゃ薬 | |||||
| 代謝異常治療薬 | β作動薬 | |||||
| リウマチ薬 | 感冒薬 | |||||
| 子宮内膜症治療薬 | 滋養強壮剤 | |||||
| 6 | 注射剤 | 安定剤(ゼラチン) | 注射 | 5 | ||
| 薬 | 癌昇圧化学療法剤 | |||||
| 抗悪性腫瘍剤 | ||||||
| 区分B2 | 7 | 成分製剤 | 抽出成分 | 経口 | 249 | |
| 薬 | ゴオウ | 肝臓エキス | ||||
| 胆汁末 | 心臓エキス | |||||
| 胆汁エキス | 精巣エキス | |||||
| コンドロイチン硫酸 | ||||||
| 8 | 低分子成分製剤 | 成分原料 | 注射 | 9 | ||
| 薬 | G−CSF製剤 | |||||
| ウルソデソキシコール酸類(急性白血病治療薬、好中級減少治療薬) | ||||||
| 9 | 菌培養医薬品/ワクチン | 培養 | 注射 | 48 | ||
| 薬 | 肺炎球菌ワクチン | 抗悪性腫瘍溶連菌製剤 | ||||
| 乾燥弱毒生麻しんワクチン | 抗悪性腫瘍剤 | |||||
| 乾燥弱毒生風しんワクチン | ステロイド剤(リウマチ、抗炎症) | |||||
| 乾燥弱毒生おたふくかぜワクチン | 抗生物質 | |||||
| 日本脳炎ワクチン | ||||||
| 区分C | 10 | 細胞培養医薬品 | MCB/WCBのみ | 注射 | 15 | |
| 薬 | 抗生物質 | ゴーシェ病治療薬(遺伝子組換え) | ||||
| 眼瞼痙攣治療薬 | ファブリー病治療薬(遺伝子組換え) | |||||
| 血栓溶解剤(遺伝子組換え) | ||||||
| 11 | 菌培養医薬品/ワクチン | シードのみ | 注射 | 44 | ||
| 薬 | インスリン製剤 | 成長ホルモン | ||||
| 12 | 低分子成分製剤 | 成分原料 | 経口 | 167 | ||
| ウルソデオキシコール酸類 | ||||||
| 13 | 菌培養医薬品/ワクチン | 培養 | 経口 | 45 | ||
| 薬 | 子宮内膜症治療薬 | 薬 | 喘息薬(吸入) | |||
| ステロイド剤(経口、坐剤、点眼) | 合成ホルモン剤 | |||||
| 抗パーキンソン病薬 | 利尿薬 | |||||
| ヒアルロン酸(手術用) | ポリオワクチン | |||||
| 14 | 外用製剤 | 基材、成分等 | 経皮 | 178 | ||
| 薬 | ステロイド剤(抗炎症薬・クリーム等) | 化 | コンドロイチン硫酸 | |||
| 消炎鎮痛貼付剤 | 化 | コラーゲン | ||||
| 抗リウマチ薬 | ||||||