

![]()
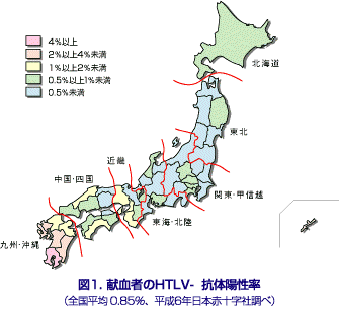
我が国における献血者のHTLV-I抗体陽性率(ゼラチン粒子凝集法すなわちPA法による陽性率)は、昭和61年に抗体検査を開始した当初は2.8%であった(日本赤十字社調べ)。しかし、平成2年4月の検査試薬改良によって偽陽性率が大幅に低下し(平成3年陽性率は1.05%)、その後も徐々に低下してきている。現在は、表1に示すように0.64%(平成9〜10年平均)であるが、西日本地域、特に南九州・沖縄で高い傾向は変わっていない(図1)。ブロック別で見ても、陽性率は九州・沖縄、近畿、中国・四国、北海道、関東・甲信越、東海・北陸、東北の順に低下し、その差は8倍近い。
一方、抗体陽性者は年間延べ39,000人程度存在するが(注5)、その46%が九州・沖縄地域で見いだされ、次いで近畿17%、関東・甲信越15%、中国・四国8%、東海・北陸8%、北海道4%、東北3%という分布になっている。
九州地域における最近のデータでは、PA法陽性献血者のうち89%が間接蛍光抗体法(IF法)および酵素免疫法(EIA法)で陽性であり、通知対象になり得るという。経験的には献血者の約7割は検査結果通知を希望するとされ、実際、平成6〜9年に鹿児島県において20歳以上の初回献血者693名を対象に実施したパイロット・スタディでは、その92%が検査結果通知を希望したという。
抗体検査導入以降、その抗体陽性血液は血液製剤原料とせず、その血球部分については処分するとともに、血漿部分は北海道千歳市にある日本赤十字社血漿分画センターへ送付し、当分の間保管することとされた[9, 10]。このような血漿は年間8,000L程度(平成6年)であり、検査開始以降で合計10万L規模になると推定される。これら血漿のうち原料血漿としての有効期間(4年)を経過したものは既に処分されているが、一部はHTLV-I抗体陽性血漿の有効利用に関する研究などに有効活用されてきたという。
![]()
HTLV-I抗体陽性血漿については、検査導入当時から分画製剤原料として有効利用できるのではないかとの議論があり(注6)、実際、HTLV-I抗体陽性血漿を原料として製造した血漿分画製剤(アルブミン製剤、人免疫グロブリン製剤)のウサギへの投与実験あるいは培養細胞への感染実験で感染性が認められなかったことが報告されている[11, 12]。このようにHTLV-I抗体陽性血漿の安全性に関する検討が行われていたことを背景としつつ、献血者への抗体陽性結果の通知については、(1)キャリアからのATL発症率が低いこと、(2)ATLについては根治的治療法がないこと、(3)通知によってキャリアが精神的苦痛を受ける可能性があること、(4)キャリアに対する社会的偏見があること、(5)カウンセリング体制が十分整っていないこと等を勘案して現在まで行われてこなかった。実際、昭和63〜平成2年度厚生省心身障害研究「成人T細胞白血病(ATL)の母子感染防止に関する研究」(班長:重松 逸造 日本公衆衛生学会理事長)でも、抗体陽性の通知を受けた妊婦の精神的、社会的苦痛が指摘されている。
献血血液のHTLV-I抗体検査結果通知の是非についての検討は、平成4〜6年度厚生科学研究「献血におけるATL抗体陽性血液の利用などに関する研究」(班長:井形 昭弘 鹿児島大学学長)で行われた。本研究では、「抗体陽性血の取り扱いに関する検討班」(班長:三好 勇夫 高知医大教授)および「献血陽性者への告知に関する検討班」(班長:納 光弘 鹿児島大学医学部教授)の2つのワーキング・グループで検討が行われ、三好班では、高力価のHTLV-I抗体陽性血漿から製造した免疫グロブリン製剤によってHTLV-I感染が予防できることから、HTLV-I抗体陽性血液の一部は有効利用できることが示された。一方、通知については、カウンセリング体制の確立が前提とされ、パイロット・スタディ実施の可能性などについて検討されたが結論は得られていない。
平成7〜9年度厚生科学研究「献血におけるATL抗体陽性血液の利用などに関する研究」(主任研究者:納 光弘 鹿児島大学医学部教授)では、鹿児島県及び福岡県においてHTLV-I抗体陽性献血者への通知に関するパイロット・スタディが実施され、10名の抗体陽性献血者へ行われた通知結果を踏まえ、「抗HTLV-I抗体陽性献血者には、インフォームド・コンセントのもとにおいて結果を通知すべきである」旨が提言されている。この背景には、HTLV-I関連疾患のうちHAMについてはその病態と治療についてかなりのことが解明され、治療法も確立されつつあり、抗体陽性通知によるHAMの早期発見、早期治療のメリットも生まれて来ていることがある。また、情報公開(知る権利)の重要性が叫ばれる時代背景なども考慮された。
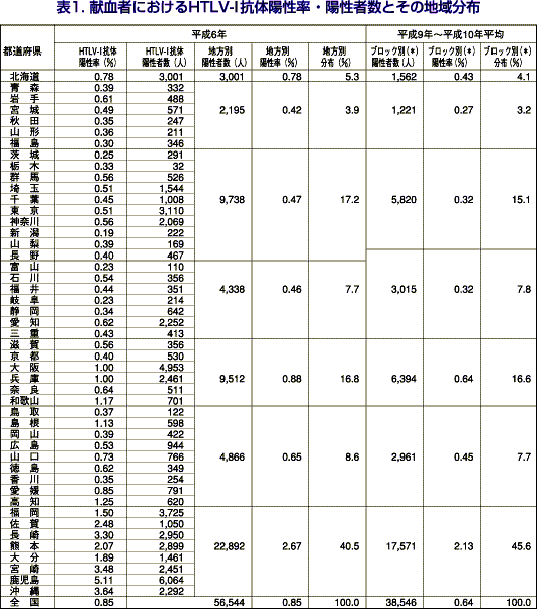
平成6年:日本赤十字社調べ(平成10年7月、中央薬事審議会血液製剤特別部会資料より)
平成9年〜10年:日本赤十字社調べ(平成11年5月、HTLV-I抗体検査陽性献血者への結果通知に関する関係者会議(近畿ブロック)資料より)
(*)基幹血液センターブロック別
平成10年7月の中央薬事審議会血液製剤特別部会(部会長:山中 學 国家公務員共済組合連合会横須賀共済病院顧問)では、同月、これに先立ち開催された安全技術調査会(座長:小室 勝利 国立感染症研究所安全性研究部長)における検討結果を踏まえながら、HTLV-I抗体陽性血漿由来の分画製剤の安全性について審議した結果、「(1)現状では不活化・除去が行われているものの、安全性を評価できる根拠が十分でないことから、当面、HTLV-I抗体検査陽性血液は使用しない、(2)HTLV-I抗体検査陽性血液の安全性の評価等については、引き続き検討する」こととされた。また、抗体陽性者への結果通知の是非については、「HTLV-I抗体検査陽性血液は使用しない方針が明確になった以上、使用できない血液を献血していただくべきではないため、今後は本人の希望を聞いた上で、陽性者にその結果を通知する」とされた。
このように抗体陽性血液を当面使用しないという結論が出されたことに伴い、抗体陽性者に通知することの利点、すなわち、(1)善意の献血を無駄にしないで済むこと、(2)発症者を早期に発見し治療できること等を理由として通知が実施されることとなったのである。また、HTLV-IキャリアからのATL発症率は、B型やC型肝炎ウイルス・キャリアからの肝硬変・肝ガン発症率と比較して低く、むしろ、肝炎ウイルス・キャリアと同様に通知することに問題はないとする、従来とは異なった考え方も一部にあった。
| (注5) | 献血者の約7割は再来献血者であり、これを考慮すると実質的に25,000人前後と推定される。 |
| (注6) | 実際、米国で分画用原料血漿としてプラズマ・フェレーシスで採取された血漿(ソース・プラズマ)についてはHTLV-I抗体検査が実施されていない。 |
[参考資料]
| 9. | 昭和61年9月10日、厚生省薬務局生物製剤課長通知、薬生第105号 |
| 10. | 昭和61年10月1日、日本赤十字社血液事業部長通知、血技第253号 |
| 11. | 明石 克ら「HTLV-I抗体陽性血漿を原料としたアルブミン製剤およびグロブリン製剤のHTLV-I感染性について」, 新薬と 臨床, 37(8), 59(1988) |
| 12. | 宮本寛治ら「成人T細胞白血病ウイルス(HTLV-1)抗体陽性血漿から分画したアルブミン製剤およびグロブリン製剤のin vitro感染実験について」, 新薬と臨床, 38(9), 89 (1989) |