|
CIRBの概要 各IRBで行っていた治験審査を一括してNCIに設けるCentral IRBで実施し、各IRBは迅速審査によりCIRBの受け入れを決定する。より多くの患者・医師の参加及び治験審査の迅速化を主目的とする CIRBの生ずる背景 現在の治験審査の問題点 Review too much, too quickly, with too little expertise
なぜこのような事態を招いたか 1970年代以降、時代の進歩に乗り遅れ
|
|
CIRBの利点・業務 利点(迅速審査の登場)
NCI治験プロトコールの特徴
CIRBの業務
各IRBの役割 迅速審査によるプロトコールの承認判定
各IRBの役割 治験が安全かつ適切に実施されているかどうかを確認
|
|
CIRBの構成
CIRBの現状・実績
初年度の状況:
2002年3月時点での現況:
CIRBの将来 CIRBを行う上での困難さ・複雑さ 各IRB、データ・安全性評価委員会、治験責任医、協力団体、NCIとCIRB間の連携が極めて重要 CIRB成功へのかぎ
将来の課題 治験に参加した患者の安全に関する責任の所在を明確にすること |
|
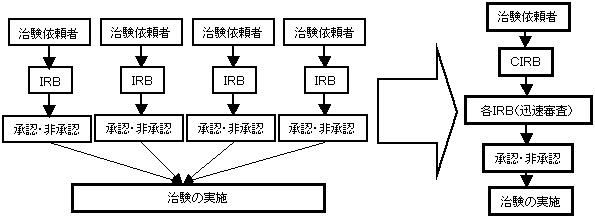
従来の審査方法
|
|
CIRB
|