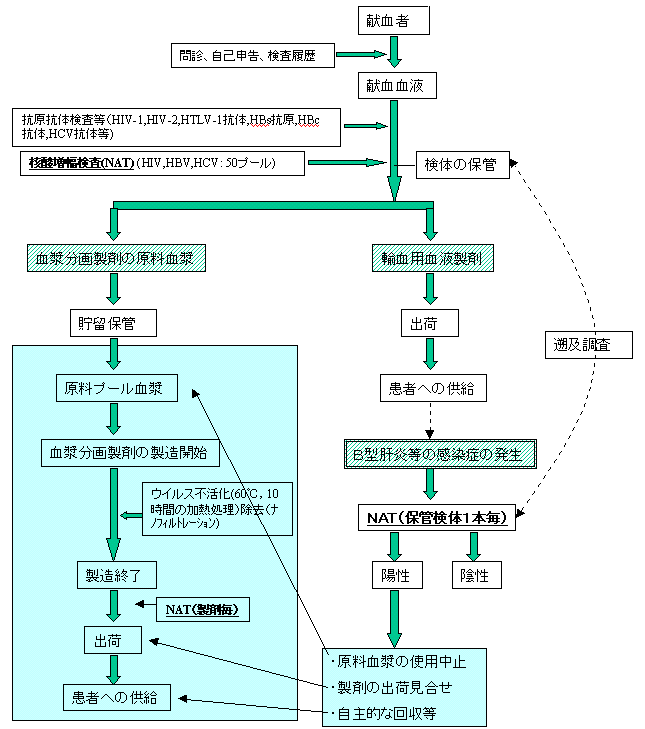
今般、輸血用血液製剤によりB型肝炎ウイルスに感染したとの報告があったため、遡及調査(別紙参照)を行ったところ、原因となった献血者に由来する原料血漿が血漿分画製剤の製造に供され、また、一部の製剤については既に出荷されていることが判明しました。
血漿分画製剤は、製造工程においてB型肝炎ウイルスの不活化処理が実施され、最終製品について核酸増幅検査(NAT)も行われている点で、加熱処理等の不活化を行っていない輸血用血液製剤とは異なりますが、現在薬事・食品衛生審議会安全技術調査会でウイルス混入血漿分画製剤の取扱いについて検討中であることから、念のため、
2.医療機関に対し情報を提供すること
照会先:医薬局血液対策課
丈達(内線2907)
医薬局安全対策課
倉持(内線2750)
|
医薬安発第0220001号 医薬監麻発第0220001号 医薬血発第0220001号 平成14年2月20日 |
|
厚生労働省医薬局安全対策課長
厚生労働省医薬局監視指導・麻薬対策課長 厚生労働省医薬局血液対策課長 |
今般、日本赤十字社より貴社に供給された血漿分画製剤用原料血漿(バッグNo.44-9135)中にB型肝炎ウイルスに係る核酸増幅検査で陽性の血液が混入していることが遡及調査により判明した旨の報告を受けたところですが、当該原料血漿を用いて製造された血漿分画製剤(別添参照)の安全性に関して現時点において十分な評価がされていないことから、下記のとおり対応することが適当であると考えられますので、至急対応願います。
なお、本件に関する貴社の対応について、随時、文書でご報告願います。
| 1 | 当該血漿分画製剤のうち出荷されていないものについては出荷しないこと。また、既に出荷されたものについては医療機関の在庫も含めて自主的に回収すること。 | ||||||
| 2 | 当該血漿分画製剤を出荷した医療機関に対し、次の情報提供を行うこと。
|
| 製品名 (一般名) |
規格 | Lot No. (サブロット) |
有効期限 |
| 献血ヴェノグロブリン−IHヨシトミ (ポリエチレングリコール処理人免疫グロブリン) |
2,500mg | H223VX | 平成15年10月11日 |
| 献血アルブミン−Wf (人血清アルブミン) |
12.5g 50mL |
H555PX | 平成15年6月10日 |
| H556PX | |||
| H557PX | |||
| ノイアート (乾燥濃縮人アンチトロンビンIII) |
500単位 | H095NX (A/B/C) |
平成15年7月24日 |
| H096NX (A/B) |
平成15年8月12日 |
|
献血受け入れから血漿分画製剤の供給に至るまでの流れ 及び B型肝炎等感染症発生時の遡及調査の流れ |

報道関係各位
三菱ウェルファーマ株式会社(本社:大阪市中央区、社長:飯田 晉一郎)は、当社が 製造販売しております血漿分画製剤の一部について、本日より自主回収を行なうこととしましたのでお知らせ致します。
この度、当社血漿分画製剤の原料血漿の供給元より、遡及調査の結果、当社に供給された原料血漿の1保管検体からB型肝炎ウイルス核酸が検出されたとの連絡を受けました。当社にて、この血漿から製造された製品を確認したところ、下記規格・ロットの製剤が 該当することが判明しました。
当該製剤は、製造工程でウイルス不活化を目的とした液状加熱処理等を行ない、また 最終製剤において核酸増幅検査(NAT)で陰性を確認した上で出荷しております。さらに、いずれの製剤についても、発売以来、因果関係が確認されたB型肝炎ウイルス感染の報告がないことより、安全性は確保されていると判断しておりますが、万全を期するため、
今回自主回収を実施することと致しました。
当該原料血漿を用いて製造された当社製品
| 製品名 | 規格 | ロット番号 | 有効期限 | |||
| 献血アルブミン‐Wf | 25% 50mL (12.5g) |
H555PX, H556PX, H557PX |
2003/06/10 | |||
|
500単位 | H095NXA,H095NXB, H095NXC |
2003/07/24 | |||
| H096NXA,H096NXB | 2003/08/12 | |||||
| 献血ヴェノグロブリン-IHヨシトミ | 2,500mg | H223VX | 2003/10/11 |
|
本件に関するお問い合わせは 本社総務部 広報・IR室 TEL:06-6201-1696までお願い致します。 |