平成13年3月29日
文部科学省、厚生労働省及び経済産業省においてヒトゲノム・遺伝子解析研究を行う際の一般的な倫理指針の策定作業を行ってきたところですが、この度確定し、本日官報への指針本文の掲載及び文部科学省研究振興局長、厚生労働省大臣官房厚生科学課長及び経済産業省製造産業局長の連名による通知を発出いたしましたのでお知らせいたします。
指針は4月1日より施行とし、指針の適切な運用に努めるとともに、研究の推進や社会の動向を踏まえながら適切な指針となるよう、注意を払っていくこととしております。
●御意見募集について
また、御意見募集の結果については整理表としてとりまとめ、指針本文とともに情報公開室において一定期間閲覧できるよう設置しており、別途厚生労働省ホームページにも掲載しておりますことお知らせいたします。
(HP https://www.mhlw.go.jp/houdou/0103/h0329-2.htmlをご覧ください。)
照会先 厚生労働省大臣官房厚生科学課 中垣(内線3803)野口(内線3804) (代表)03(5253)1111 (直通)03(3595)2171
| 写 |
| 文部科学省研究振興局長 遠藤 昭雄
厚生労働省大臣官房厚生科学課長
経済産業省製造産業局長 |
ヒトゲノム・遺伝子解析研究においては、人間の尊厳及び人権を尊重し、社会の理解と協力を得て、適正に研究を実施するための規範づくりが緊急の課題となっている。
そのため、文部科学省、厚生労働省及び経済産業省の三省が共同して、今般、ヒトゲノム・遺伝子解析研究一般に適用されるべき倫理指針として、「ヒトゲノム・遺伝子解析研究に関する倫理指針(平成13年3月文部科学省・厚生労働省・経済産業省告示第1号)」(以下「指針告示」という。)を告示した。
また、指針告示の運用に資するため、指針告示の「15 細則」に基づき、別添のとおり、細則及び注を定めたので通知する。
1.三省指針運用窓口の設置について
指針運用上の疑義照会等がある場合には、次に示す三省のいずれにおいても受け付け、適宜三省で協議を行った上で回答することとする。特に医学的又は技術的に専門的な事項にわたる内容については、厚生労働省において受理し、専門家の意見も踏まえて対応する。また、疑義照会に対する主な回答については、関係三省のホームページに掲載することにより情報提供する。
| (1) | 文部科学省研究振興局ライフサイエンス課生命倫理・安全対策室 | |
| 住所: | 〒100-8966 東京都千代田区霞が関2-2-1 | |
| 電話: | 03-3581-5271(代表)内線5451 03-3509-1268(直通) |
|
| FAX: | 03-3509-1269 | |
| ホームページ: | http://www.mext.go.jp/a_menu/shinkou/seimei/index.htm. | |
| (2) | 厚生労働省大臣官房厚生科学課 | |
| 住所: | 〒100-8916 東京都千代田区霞が関1-2-2 | |
| 電話: | 03-5253-1111(代表)内線3815 03-3595-2171(直通) |
|
| FAX: | 03-3503-0183 | |
| ホームページ: | https://www.mhlw.go.jp | |
| (3) | 経済産業省製造産業局生物化学産業課 | |
| 住所: | 〒100-8901 東京都千代田区霞が関1-3-1 | |
| 電話: | 03-3501-1511(代表)内線3741 03-3501-8625(直通) |
|
| FAX : | 03-3501-0197 | |
| ホームページ: | http://www.meti.go.jp/policy/bio/main_01.html | |
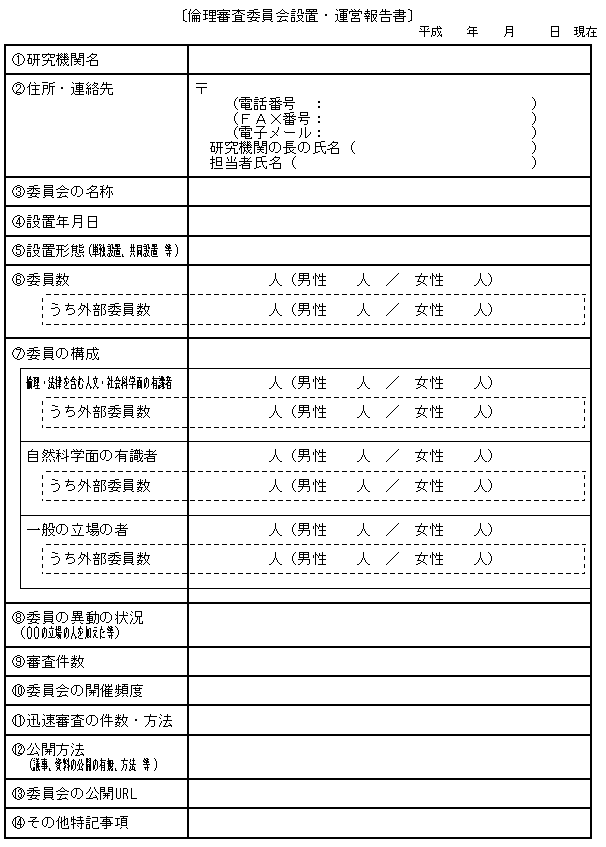
2.倫理審査委員会の設置及び運営の状況の把握について
ヒトゲノム・遺伝子解析研究の適正な推進を図る上で、倫理審査委員会の役割は非常に重要である。そのため、本指針の施行後、各研究機関における倫理審査委員会の設置及び運営の状況を把握し、今後の本指針の適正な運用のための参考資料を得ることとしたい。ついては、本指針に基づきヒトゲノム・遺伝子解析研究を実施する研究機関においては、倫理審査委員会の設置及び運営の状況について、[別紙様式]により、上記1.の窓口のいずれかに対し、本指針に基づく倫理審査委員会を設置したときは速やかに、及びその後は毎年3月末時点の状況を速やかに報告願いたい。なお、寄せられた情報は今後の施策の検討材料とするほか、国民に対する情報提供の一環として一般に公開することもあり得ることを、あらかじめ御了解願いたい。
(注)倫理審査委員会の設置及び運営に関する報告については、上記1.(1)、(2)及び(3)に掲げるホームページに掲載しているフォーマットを用いた電子媒体による提出又はFAXによる提出をお願いする。

| ※1 : | 委員会設置後、速やかな提出をお願いします。なお、その後は毎年3月末時点の状況について速やかに提出をお願いします。 |
| ※2 : | (8)~(14)については、委員会設置後最初に提出する報告書には記載する必要はありません。 |
| ※3 : | 委員名簿、運営規則、組織細則等がある場合には、添付をお願いします。 |
1 基本方針
2 本指針の適用範囲
3 すべての研究者等の基本的な責務
4 研究機関の長の責務
5 研究責任者の責務
6 個人情報管理者の責務
7 倫理審査委員会の責務及び構成
8 インフォームド・コンセント
9 遺伝情報の開示
10 遺伝カウンセリング
11 研究実施前提供試料等の利用
12 試料等の保存及び廃棄の方法
13 見直し
14 用語の定義
15 細則
16 施行期日
科学研究の推進は、人々が健やかで心豊かに生活できる社会を実現するための重要な課題である。その中で、20世紀後半に開始されたヒトゲノム・遺伝子解析研究は、生命科学及び保健医療科学の進歩に大きく貢献し、人類の健康や福祉の発展、新しい産業の育成等に重要な役割を果たそうとしている。
一方、ヒトゲノム・遺伝子解析研究は、個人を対象とした研究に大きく依存し、また、研究の過程で得られた遺伝情報は、提供者(ヒトゲノム・遺伝子解析研究のための試料等を提供する人)及びその血縁者の遺伝的素因を明らかにし、その取扱いによっては、様々な倫理的、法的又は社会的問題を招く可能性があるという側面がある。そこで、人間の尊厳及び人権を尊重し、社会の理解と協力を得て、適正に研究を実施することが不可欠である。そのため、世界医師会によるヘルシンキ宣言等に示された倫理規範を踏まえ、提供者個人の人権の保障が、科学的又は社会的な利益に優先されなければならないことに加えて、この側面について、社会に十分な説明を行い、その理解に基づいて研究を実施することが求められる。しかしながら、ヒトゲノム・遺伝子解析研究一般に関して、我が国では上記のような要請にこたえることのできる規範は十分には確立されていないことから、人間の尊厳が尊重され、提供者及びその家族又は血縁者の人権が保障され、研究が適正に実施されるための具体的な指針の策定が緊急の課題となっている。
本指針は、国際連合教育科学文化機関(ユネスコ)の「ヒトゲノムと人権に関する世界宣言」等を踏まえて策定された「ヒトゲノム研究に関する基本原則」(平成12年6月14日科学技術会議生命倫理委員会取りまとめ)に示された原則に基づき、また、「遺伝子解析研究に付随する倫理問題等に対応するための指針」(平成12年4月28日厚生科学審議会先端医療技術評価部会取りまとめ)を参考としつつ、ヒトゲノム・遺伝子解析研究一般に適用されるべき倫理指針として、文部科学省、厚生労働省及び経済産業省において共同で作成し、社会に提示するものである。
<注>
1 基本方針
本指針は、ヒトゲノム・遺伝子解析の特色を踏まえ、すべてのヒトゲノム・遺伝子解析研究に適用され、研究現場で遵守されるべき倫理指針として策定されたものである。本指針は、人間の尊厳及び人権が尊重され、社会の理解と協力を得て、研究の適正な推進が図られることを目的とし、次に掲げる事項を基本方針としている。
<注>
(1)人間の尊厳の尊重
(2)事前の十分な説明と自由意思による同意(インフォームド・コンセント)
(3)個人情報の保護の徹底
(4)人類の知的基盤、健康及び福祉に貢献する社会的に有益な研究の実施
(5)個人の人権の保障の科学的又は社会的利益に対する優先
(6)本指針に基づく研究計画の作成及び遵守並びに独立の立場に立った倫理審査委員会による事前の審査及び承認による研究の適正性の確保
(7)研究の実施状況の第三者による実地調査と研究結果の公表を通じた研究の透明性の確保
2 本指針の適用範囲
本指針は、ヒトゲノム・遺伝子解析研究を対象とし、その研究に携わる研究者等に遵守を求めるものである。
なお、診療において実施され、解析結果が提供者及びその血縁者の診療に直接生かされることが医学的に確立されている臨床検査及びそれに準ずるヒトゲノム・遺伝子解析は、医療に関する事項として、今後、慎重に検討すべき課題であり、本指針の対象としない。ただし、これらのヒトゲノム・遺伝子解析についても、診療を行う医師の責任において、関係学会等において作成される指針等を参考に、本指針の趣旨を踏まえた適切な対応が望まれる。
3 すべての研究者等の基本的な責務
(1)すべての研究者等は、生命現象の解明、疾病の予防、診断及び治療の方法の改善、健康の増進等を目的として、ヒトゲノム・遺伝子解析研究を実施しなければならない。
(2)すべての研究者等は、ヒトゲノム・遺伝子解析研究の社会的有益性を確認するとともに、個人の人権の保障を科学的又は社会的な利益に優先して配慮しなければならない。
(3)すべての研究者等は、提供者又は代諾者等への事前の十分な説明とその自由意思による同意(インフォームド・コンセント)を受けて、ヒトゲノム・遺伝子解析研究を実施することを基本としなければならない。
(4)すべての研究者等は、職務上知り得た個人情報を正当な理由なく漏らしてはならない。その職を辞した後も、同様である。
(5)すべての研究者等は、個人情報の保護を図るとともに、個人情報の取扱いに関する苦情等に誠実に対応しなければならない。
(6)すべての研究者等は、個人情報の予期せぬ漏洩等の提供者等の人権の保障の観点から重大な懸念が生じた場合には、速やかに研究機関の長及び研究責任者に報告しなければならない。
(7)すべての研究者等は、倫理審査委員会の承認を得て、研究機関の長により許可された研究計画書に従って研究を実施する等、本指針を遵守し、人間の尊厳及び人権を尊重して、適正にヒトゲノム・遺伝子解析研究を実施しなければならない。
(8)すべての研究者等は、研究実施に当たっての適正な手続の確保、外部の有識者による実地調査、提供者等からの研究の進捗状況の問い合わせへの的確な対応、研究結果の公表等、研究の透明性の確保を図らなければならない。
(9)すべての研究者等は、試料等の提供が善意に基づくものであることに留意し、既に提供されている試料等を適切に保存し、及び活用すること等により、人からの試料等の提供を必要最低限とするよう努めなければならない。
4 研究機関の長の責務
(1)研究機関の長は、その機関におけるヒトゲノム・遺伝子解析研究の実施に関する最終的な責任を有し、研究責任者及び研究担当者が研究計画に従って適正に研究を実施するよう監督しなければならない。その際、研究機関の長は、提供者等の人権を最大限保障すべきこと及び本指針、研究計画等に反した場合に懲戒処分等の不利益処分がなされ得ることについて、その機関の関係者に対する周知徹底を図らなければならない。
(2)研究機関の長は、個人情報の漏洩防止のための十分な措置を講じなければならない。
(3)試料等の提供が行われる機関等の個人情報を取り扱う研究機関の長は、ヒトゲノム・遺伝子解析研究において、個人情報の保護を図るため、個人情報管理者を置かなければならない。また、必要に応じ、指揮命令系統を明確にした上で、分担管理者又は個人情報管理者の監督の下に実際の業務を行う補助者を置くことができる。
(4)研究機関の長は、ヒトゲノム・遺伝子解析研究実施の可否等を審査するため、その諮問機関として、倫理審査委員会を設置しなければならない。ただし、試料等の提供が行われる機関が小規模であること等により、倫理審査委員会の設置が困難である場合には、共同研究機関、公益法人又は学会によって設置された倫理審査委員会をもってこれに代えることができる。
(5)研究機関の長は、すべての研究計画又はその変更について、倫理審査委員会の意見を尊重し、許可するか否かを決定しなければならない。この場合において、倫理審査委員会が不承認の意見を提出した研究については、その実施を許可してはならない。
(6)研究機関の長は、研究責任者から研究の実施状況について1年に1回以上定期的な報告を受けるほか、外部の有識者による定期的な実地調査を1年に1回以上実施する等、ヒトゲノム・遺伝子解析研究の実施状況を把握し、必要に応じ、又は倫理審査委員会が研究の変更若しくは中止の意見を述べた場合にはその意見を踏まえ、その変更又は中止を命じなければならない。
(7)研究機関の長は、許可した研究計画書の写し、研究の実施状況に関する定期的な報告書の写し及び外部の有識者による実地調査結果の写しを個人情報管理者に送付しなければならない。
(8)研究機関の長は、倫理審査委員会に、研究の実施状況に関する定期的な報告書の写し及び外部の有識者による実地調査結果の写しを送付しなければならない。
(9)研究機関の長は、提供者等からの苦情等の窓口を設置する等、提供者等からの苦情や問い合わせ等に適切に対応しなければならない。
(10)試料等の提供が行われる機関の長は、試料等を外部の機関(試料等の提供が行われる機関において、同時にヒトゲノム・遺伝子解析研究も行う場合は、その研究部門は外部の機関とみなす。)に提供する際には、原則として試料等を匿名化しなければならない。
(11)試料等の提供が行われる機関の長は、必要に応じ、適切な遺伝カウンセリング体制の整備又は遺伝カウンセリングについての説明及びその適切な施設の紹介等により、提供者及びその家族又は血縁者が遺伝カウンセリングを受けられるよう配慮しなければならない。
5 研究責任者の責務
(1)研究責任者は、ヒトゲノム・遺伝子解析研究の実施に当たって、あらかじめ研究計画書を作成し、研究機関の長に許可を求めなければならない。研究計画書を変更しようとする場合も、同様である。
(2)研究責任者は、研究計画書の作成に当たり、実施しようとしているヒトゲノム・遺伝子解析研究に伴い提供者等に予想される様々な影響等を踏まえ、研究の必要性、提供者等の不利益を防止するための研究方法等を十分考慮しなければならない。
(3)研究責任者は、ヒトゲノム・遺伝子解析研究の特殊性に十分配慮して研究計画書を作成しなければならない。特に、インフォームド・コンセントの手続及び方法、個人情報の保護の方法、研究により予測される結果及びその開示の考え方、試料等の保存及び使用の方法並びに遺伝カウンセリングの考え方については、明確に記載しなければならない。
(4)研究責任者は、許可された研究計画書に盛りこまれた事項を、すべての研究担当者に遵守させる等、研究担当者が適正にヒトゲノム・遺伝子解析研究を実施するよう監督しなければならない。
(5)研究責任者は、ヒトゲノム・遺伝子解析研究の実施状況について、研究機関の長に1年に1回以上、定期的に文書で報告しなければならない。
(7)研究責任者は、匿名化されていない試料等又は遺伝情報を原則として外部の機関に提供してはならない。
(8)研究責任者は、ヒトゲノム・遺伝子解析研究の業務の一部を委託する場合には、受託者に対しては、試料等又は遺伝情報を原則として匿名化しなければならない。
(9)研究責任者は、ヒトゲノム・遺伝子解析研究の進捗状況及びその結果を、定期的に及び提供者等の求めに応じて、分かりやすく説明し、又は公表しなければならない。ただし、提供者等の人権の保障や知的財産権の保護に必要な部分については、この限りでない。
6 個人情報管理者の責務
(1)個人情報管理者(分担管理者を含む。以下6において同じ。)は、原則として、研究責任者からの依頼に基づき、ヒトゲノム・遺伝子解析研究の実施前に試料等又は遺伝情報を匿名化しなければならない。ただし、研究担当者等が補助者として匿名化作業を行う場合にあっては、それが適正に行われるよう、監督しなければならない。
(2)個人情報管理者は、匿名化の際に取り除かれた個人情報を、原則として外部の機関に提供してはならない。
(3)個人情報管理者は、匿名化作業の実施のほか、匿名化されていない試料等を使用する研究担当者を適切に監督する等、個人情報が含まれている情報が漏洩しないよう厳重に管理しなければならない。
7 倫理審査委員会の責務及び構成
(1)倫理審査委員会は、本指針に基づき、研究計画の実施の適否等について、倫理的観点とともに科学的観点も含めて審査し、研究機関の長に対して文書により意見を述べなければならない。
(2)倫理審査委員会は、研究機関の長に対して、実施中の研究に関して、その研究計画の変更、中止その他必要と認める意見を述べることができる。
(3)倫理審査委員会の委員は、職務上知り得た情報を正当な理由なく漏らしてはならない。その職を辞した後も、同様である。
(4)倫理審査委員会は、独立の立場に立って、学際的かつ多元的な視点から、様々な立場からの委員によって、公正かつ中立的な審査を行えるよう、適切に構成し運営されなければならない。
(5)倫理審査委員会は、その決定により、委員長があらかじめ指名した委員又はその下部組織による迅速審査手続を設けることができる。迅速審査の結果については、その審査を行った委員以外のすべての委員又は上部組織である倫理審査委員会に報告されなければならない。
(6)倫理審査委員会については、その組織に関する事項や運営に関する規則が公開されるとともに、議事の内容についても原則として公開されなければならない。
8 インフォームド・コンセント
(1)研究責任者(他の研究機関から試料等の提供を受けて研究を実施する者を除く。以下8((4)及び(7)を除く。)において同じ。)は、試料等の提供の依頼を受ける人を、不合理、不当又は不公平な方法で選んではならない。
(2)研究責任者は、提供者に対して、事前に、その研究の意義、目的、方法、予測される結果、提供者が被る可能性のある不利益、試料等の保存及び使用方法等について十分な説明を行った上で、自由意思に基づく文書による同意を受けて、試料等の提供を受けなければならない。
(3)研究責任者は、提供者本人から(2)によるインフォームド・コンセントを受けることが困難な場合には、その実施しようとしている研究の重要性が高く、かつ、その人からの試料等の提供を受けなければ研究が成り立たないと倫理審査委員会が承認し、研究機関の長が許可した場合に限り、提供者本人の代諾者等からインフォームド・コンセントを受けることができる。
(4)提供者又はその代諾者等は、自らが与えたインフォームド・コンセントについて、いつでも不利益を受けることなく文書により撤回することができる。
(5)研究責任者は、提供者又はその代諾者等からインフォームド・コンセントの撤回があった場合には、原則として、当該提供者に係る試料等及び研究結果を匿名化して廃棄しなければならない。
(6)研究責任者は、提供者又は代諾者等からのインフォームド・コンセントを受ける手続においては、提供者又は代諾者等に対し、十分な理解が得られるよう、必要な事項を記載した文書を交付して説明を行わなければならない。提供者が単一遺伝子疾患等である場合には、遺伝カウンセリングの利用に関する情報を含めて説明を行うとともに、必要に応じて遺伝カウンセリングの機会を提供しなければならない。
(7)他の研究機関から試料等又は遺伝情報の提供を受ける研究責任者は、当該試料等又は遺伝情報に関するインフォームド・コンセントの内容を当該他の研究機関からの文書等によって確認しなければならない。
(8)研究責任者は、ヒトゲノム・遺伝子解析研究の実施前に、ヒトゲノム・遺伝子解析研究又は関連する医学研究に使用することを想定して、提供者又は代諾者等からインフォームド・コンセントを受ける場合には、その時点において予想される具体的研究目的を明らかにするとともに、個人情報が、匿名化の可能性を含めて、どのように管理され、かつ、保護されるかを説明し、理解を得なければならない。
9 遺伝情報の開示
(1)研究責任者は、個々の提供者の遺伝情報が明らかとなるヒトゲノム・遺伝子解析研究に関して、提供者が自らの遺伝情報の開示を希望している場合には、原則として開示しなければならない。ただし、遺伝情報を提供する十分な意義がなく、開示しないことについて提供者のインフォームド・コンセントを受けている場合には、この限りでない。
(2)研究責任者は、個々の提供者の遺伝情報が明らかとなるヒトゲノム・遺伝子解析研究に関して、提供者が自らの遺伝情報の開示を希望していない場合には、開示してはならない。
(3)研究責任者は、提供者本人の同意がない場合には、提供者の遺伝情報を、提供者本人以外の人に対し、原則として開示してはならない。
(4)研究責任者は、単一遺伝子疾患等に関する遺伝情報を開示しようとする場合には、医学的又は精神的な影響等を十分考慮し、診療を担当する医師との緊密な連携の下に開示するほか、必要に応じ、遺伝カウンセリングの機会を提供しなければならない。
10 遺伝カウンセリング
(1)目的
ヒトゲノム・遺伝子解析研究における遺伝カウンセリングは、対話を通じて、提供者及びその家族又は血縁者に正確な情報を提供し、疑問に適切に答え、その人たちの遺伝性疾患等に関する理解を深め、ヒトゲノム・遺伝子解析研究や遺伝性疾患等をめぐる不安又は悩みにこたえることによって、今後の生活に向けて自らの意思で選択し、行動できるように支援し、又は援助することを目的とする。
(2)実施方法
遺伝カウンセリングは、遺伝医学に関する十分な知識を有し、遺伝カウンセリングに習熟した医師、医療従事者等が協力して実施しなければならない。
11 研究実施前提供試料等の利用
(1)研究機関において、ヒトゲノム・遺伝子解析研究の実施前に提供され、かつ、保存されている試料等の利用の可否は、提供者又は代諾者等の同意の有無又はその内容及び試料等が提供された時期を踏まえ、(2)から(4)までに定めるところにより、倫理審査委員会の承認を得た上で、研究機関の長が決定する。
(2)本指針の施行後に提供された研究実施前提供試料等については、本指針の理念を踏まえて、研究機関の長及び研究責任者は、その利用について慎重に判断し、また、倫理審査委員会は、研究における利用の可否を慎重に審査しなければならない。
(3)A群試料等(試料等の提供時に、ヒトゲノム・遺伝子解析研究における利用を含む同意が与えられている試料等)については、その同意の範囲内でヒトゲノム・遺伝子解析研究に利用することができる。
(4)B群試料等(試料等の提供時に、ヒトゲノム・遺伝子解析研究における利用が明示されていない研究についての同意のみが与えられている試料 等)及びC群試料等(試料等の提供時に、研究に利用することの同意が与えられていない試料等)については、原則として、本指針において定める方法等に従って新たに提供者又は代諾者等の同意を得ない限り、ヒトゲノム・遺伝子解析研究に利用してはならない。
12 試料等の保存及び廃棄の方法
(1)保存の一般原則
研究責任者は、研究機関内で試料等を保存する場合には、提供者又は代諾者等の同意事項を遵守し、研究計画書に定められた方法に従わなければならない。
(2)ヒト細胞・遺伝子・組織バンクへの提供
研究責任者は、試料等をヒト細胞・遺伝子・組織バンクに提供する場合には、当該バンクが試料等を一般的な研究用試料等として分譲するに当たり、連結不可能匿名化がなされることを確認するとともに、バンクに提供することの同意を含む提供者又は代諾者等の同意事項を遵守しなければならない。
(3)試料等の廃棄
研究責任者は、研究計画書に従い自ら保存する場合及びヒト細胞・遺伝子・組織バンクに提供する場合を除き、試料等の保存期間が研究計画書に定めた期間を過ぎた場合には、提供者又は代諾者等の同意事項を遵守し、匿名化して廃棄しなければならない。
13 見直し
この指針は、必要に応じ、又は施行後5年を目途としてその全般に関して検討を加えた上で、見直しを行うものとする。
14 用語の定義
(1)試料等
ヒトゲノム・遺伝子解析研究に用いようとする血液、組織、細胞、体液、排泄物及びこれらから抽出したDNA等の人の体の一部並びに提供者の診療情報(死者から提供されたものを含む。)をいう。ただし、学術的な価値が定まり、研究実績として十分に認められ、研究用に広く一般に利用され、かつ、一般に入手可能な組織、細胞、体液及び排泄物並びにこれらから抽出したDNA等は、含まれない。
(2)診療情報
診断及び治療を通じて得られた疾病名、投薬名、検査結果等の情報をいう。
(3)ヒトゲノム・遺伝子解析研究
提供者の個体を形成する細胞に共通して存在し、その子孫に受け継がれ得るヒトゲノム及び遺伝子の構造又は機能を、試料等を用いて明らかにしようとする研究をいう。本研究に用いる試料等の提供のみが行われる場合も、含まれる。
(4)遺伝情報
試料等を用いて実施されるヒトゲノム・遺伝子解析研究の過程を通じて得られ、又は既に試料等に付随している個人の遺伝的特徴や体質を示す情報をいう。
(5)個人情報
個人に関する情報であって、当該情報に含まれる氏名、生年月日その他の記述等により特定の個人を識別することができるもの(他の情報と容易に照合することができ、それにより特定の個人を識別することができることとなるものを含む。)をいう。
(6)匿名化
ある人の個人情報が法令、本指針又は研究計画に反して外部に漏洩しないように、その個人情報から個人を識別する情報の全部又は一部を取り除き、代わりにその人と関わりのない符号又は番号を付すことをいう。試料等に付随する情報のうち、ある情報だけでは特定の人を識別できない情報であっても、各種の名簿等の他で入手できる情報と組み合わせることにより、その人を識別できる場合には、組合せに必要な情報の全部又は一部を取り除いて、その人が識別できないようにすることをいう。匿名化には、次に掲げるものがある。
(7)個人情報管理者
試料等の提供が行われる機関を含め、個人情報を取り扱う研究機関において、研究機関の長の指示を受け、提供者等の個人情報がその機関の外部に漏洩しないように個人情報を管理し、かつ、匿名化する責任者をいう。
(8)インフォームド・コンセント
試料等の提供を求められた人が、研究責任者から事前にヒトゲノム・遺伝子解析研究に関する十分な説明を受け、その研究の意義、目的、方法、予測される結果や不利益等を理解し、自由意思に基づいて与える試料等の提供及び試料等の取扱いに関する同意をいう。本指針においては、文書によることが求められる。
(9)代諾者等
試料等の提供を求められた本人にインフォームド・コンセントを与える能力がない場合に、その人の代わりにインフォームド・コンセントを与える人をいう。提供者本人が死者である場合にあっては、遺族をいう。なお、遺族を含めずに使用する場合は、「代諾者」という。
(10)未成年者
婚姻をしていない満20歳未満の人をいう。
(11)研究機関
ヒトゲノム・遺伝子解析研究を実施する機関(試料等の提供が行われる機関を含む。)をいう。
(12)試料等の提供が行われる機関
研究機関のうち、医療機関や保健所のように、人々から試料等の提供が行われる機関をいう。
(13)共同研究機関
研究計画書に記載されたヒトゲノム・遺伝子解析研究を共同して行う大学を含む国公立又は民間の研究機関をいう。ある研究機関がその機関以外の試料等の提供が行われる機関から試料等の提供を受ける場合には、その試料等の提供が行われる機関を含む。
(14)外部の機関
所属する研究機関以外の研究機関等をいう。なお、試料等の提供が行われる機関がその機関内の別の部門において当該試料等を用いてヒトゲノム・遺伝子解析研究も実施する場合には、その研究部門は、外部の機関とみなす。
(15)倫理審査委員会
ヒトゲノム・遺伝子解析研究の実施の適否その他の事項について、提供者等の人権の保障等の倫理的観点とともに科学的観点を含めて調査審議するため、研究機関の長の諮問機関として置かれた合議制の機関をいう。
(16)研究者等
研究機関において、研究責任者、研究担当者(試料等の提供を受ける業務を行う者を含む。)、遺伝カウンセリングを実施する者、個人情報保護の業務を行う者、研究機関の長その他のヒトゲノム・遺伝子解析研究に携わる関係者をいう。
(17)研究責任者
個々の研究機関において、ヒトゲノム・遺伝子解析研究を遂行するとともに、その研究に係る業務を統括する者であって、ヒトゲノム・遺伝子解析研究の有用性と限界及び生命倫理について十分な知識を有する研究者をいう。
(18)研究担当者
研究責任者の指示や委託に従ってヒトゲノム・遺伝子解析研究を実施する者であって、業務の内容に応じて必要な知識と技能を持つ研究者、医師、薬剤師、看護婦(士)、臨床検査技師等をいう。
(19)提供者
ヒトゲノム・遺伝子解析研究のための試料等を提供する人をいう。なお、提供者の家族、血縁者、代諾者等のように、提供者の遺伝情報に関わりがあると考えられる人を含める場合には、「提供者等」という。
(20)遺伝カウンセリング
遺伝医学に関する知識及びカウンセリングの技法を用いて、対話と情報提供を繰り返しながら、遺伝性疾患をめぐり生じ得る医学的又は心理的諸問題の解消又は緩和を目指し、支援し、又は援助することをいう。
(21)研究実施前提供試料等
研究機関において、ヒトゲノム・遺伝子解析研究の実施前に提供され、かつ、保存されている試料等をいう。試料等の提供時における同意の状況に応じて、次に掲げるものに分かれる。
(22)ヒト細胞・遺伝子・組織バンク
提供されたヒトの細胞、遺伝子、組織等について、研究用資源として品質管理を実施して、不特定多数の研究者に分譲する非営利的事業をいう。
15 細則
本指針に定めるもののほか、本指針の施行に関し必要な事項は、別に定める。
16 施行期日
本指針は、平成13年4月1日から施行する。
[目次]
(参考2)ヒトゲノム・遺伝子解析研究の過程に沿った基本的な要点
(参考4)「ヒトゲノム・遺伝子解析研究に関する倫理指針」の策定の背景、経緯等について
(参考5)「ヒトゲノム・遺伝子解析研究に関する倫理指針」策定担当3省事務局名簿
○ ヘルシンキ宣言(1964年6月第18回世界医師会採択)、「ヒトゲノム研究に関する基本原則」(平成12年6月14日科学技術会議生命倫理委員会取りまとめ)等を踏まえ、すべてのヒトゲノム・遺伝子解析研究に適用され、研究現場で遵守されるべき倫理指針として策定
○ 人間の尊厳及び人権が尊重され、社会の理解と協力を得て、ヒトゲノム・遺伝子解析研究の適正な推進が図られることを目的
2.「ヒトゲノム・遺伝子解析研究」の定義
試料等の提供者の個体を形成する細胞に共通して存在し、その子孫に受け継がれ得るヒトゲノム及び遺伝子の構造又は機能を、試料等を用いて明らかにしようとする研究をいう。本研究に用いる試料等の提供のみが行われる場合も含まれる。
3.主な内容
前文
ヒトゲノム・遺伝子解析研究に関わるすべての関係者においてこの指針を遵守することが求められる。
「遺伝子解析研究に付随する倫理問題等に対応するための指針」については、本指針の施行に伴い、廃止され、本指針に一本化されるものである。
第1 基本的考え方
本指針においては、研究の過程で得られる遺伝情報が提供者本人及び血縁者の遺伝的素因を明らかにすることがある結果、様々な問題を提起する可能性があるというヒトゲノム・遺伝子解析研究の特色を踏まえ、14(3)において、本指針の対象とすべき研究の定義及び範囲を定めている。
第2 研究者等の責務
研究機関の長とは、例えば、以下のとおりである。
・ 保健所の場合は、保健所長
・ 大学医学部の場合は、医学部長
・ 企業等の研究所の場合は、研究所長
(6)研究責任者は、原則として、匿名化された試料等又は遺伝情報を用いて、ヒトゲノム・遺伝子解析研究を実施しなければならない。
・ 会議の成立要件
・ 議決方法
・ 審査記録の保存期間
・ 公開に関する事項
・ 委員の氏名、所属及びその立場
第3 提供者に対する基本姿勢
・ 有効な治療法の有無と提供者の健康状態
・ 血縁者が同一の疾患等に罹患している可能性
・ インフォームド・コンセントに際しての研究結果の開示に関する説明内容
b 血縁者の生命に及ぼす影響
c 有効な治療法の有無と血縁者の健康状態
d インフォームド・コンセントに際しての研究結果の開示に関する説明内容
第4 試料等の取扱い
第5 見直し
第6 用語の定義
試料等の提供時に、ヒトゲノム・遺伝子解析研究における利用を含む同意が与えられている試料等をいう。
試料等の提供時に、「医学的研究に用いることに同意する」等のように、ヒトゲノム・遺伝子解析研究における利用が明示されていない研究についての同意のみが与えられている試料等をいう。
試料等の提供時に、研究に利用することの同意が与えられていない試料等をいう。
第7 細則
第8 施行期日
ヒトゲノム・遺伝子解析研究に関する倫理指針
(参考資料)
1.趣旨及び目的
研究の有益性等の判断
○ 実施しようとする研究が、社会的有益性があり、かつ、個人の人権の保障が優先されているかを判断
○ 実施しようとする研究が、本指針に定めるヒトゲノム・遺伝子解析研究に該当するかどうかを判断
研究計画書の作成
○ インフォームド・コンセントの方法、研究により予測される結果とその開示の考え方、匿名化の方法を含む個人情報の保護の方法、試料等の保存及び使用方法などを記載
○ 単一遺伝子疾患等の場合は、研究の必要性、本人の利益保護のための措置を慎重に判断し、解析結果が試料等の提供者に開示される場合においては、遺伝カウンセリングを実施する体制を確保し、それらの考え方、方法等を研究計画書に記載
○ 研究実施前に提供された試料等を研究に利用する場合には、その必要性、インフォームド・コンセントの状況等を研究計画書に記載
倫理審査委員会における審査
○ 研究計画書の倫理審査委員会における審査
研究機関の長の決定
○ 研究計画書に対する倫理審査委員会の意見に基づき、研究機関の長が研究実施を許可するか否かを決定
研究の実施
○ 研究は、研究計画書に従って原則として匿名化された試料等を用いて実施
○ 実施状況については、研究機関の長に定期的に報告。また、外部の有識者による実地調査の実施
研究結果の公表
○ 研究の進捗状況及びその結果を定期的に又は求めに応じて公表
○研究実施前提供試料等の利用の可否は、以下を踏まえ、倫理審査委員会の承認を得た上で、研究実施機関の長が決定。本指針施行後に提供されたものについては、特に慎重に判断。
|

○ その一方で、ヒトゲノム・遺伝子解析研究は、個人を対象とした研究に大きく依存し、また、研究の過程で得られた遺伝情報は試料等提供者やその血縁者の遺伝的素因を明らかにし、その取扱いによっては様々な倫理的、法的、社会的問題を招く可能性があるという側面がある。
○ そこで、人間の尊厳及び人権を尊重し、社会の理解と協力を得て、適正に研究を実施することが不可欠であり、そのためのルールづくりが求められてきた。
○ この点に関しては、既に
○ このような状況の下、文部科学省、厚生労働省及び経済産業省の3省が共同して、今般、ヒトゲノム・遺伝子解析研究一般に適用されるべき倫理指針として、「ヒトゲノム・遺伝子解析研究に関する倫理指針」を策定するものである。
○ この倫理指針案の策定については、検討委員会[別紙1]における原案の作成過程において、アンケート調査の実施や、作業委員会[別紙2]の設置による意見交換、パブリック・コメントの募集(昨年12月20日~本年1月31日)、3省関係者会議[別紙3]、関係審議会における審議[別紙4]等の経過を経て、可能な限り様々な意見を反映するよう努めてきた。
○ この倫理指針の位置付けについては、関係する国の研究機関において、又は国の補助金の交付を受けて実施されるヒトゲノム・遺伝子解析研究については、遵守が義務付けられることとなるが、それ以外の民間の研究機関等で実施されるヒトゲノム・遺伝子解析研究についても、遵守されるよう周知に努めていきたいと考えている。
策定の背景、経緯等について
○ 20世紀後半に開始されたヒトゲノム・遺伝子解析研究は、生命科学及び保健医療科学の進歩に大きく貢献し、人類の健康や福祉の発展、新しい産業の育成などに重要な役割を果たそうとしている。
特に、パブリック・コメントについては、計92の個人・団体から、延べ 577件の意見が寄せられ[別紙5]、そのうち約2割に当たる 108件の意見を踏まえ、修文が行われた。
| 雨宮 浩 | 国立小児病院小児医療研究センター長 | |
| 位田 隆一 | 京都大学大学院法学研究科教授 | |
| 上田 國寛 | 京都大学化学研究所教授 | |
| 宇都木 伸 | 東海大学法学部法律学科教授 | |
| 小幡 純子 | 上智大学法学部教授 | |
| ◎ | 垣添 忠生 | 国立がんセンター中央病院長 |
| 金澤 一郎 | 東京大学大学院医学系研究科教授(神経内科学) | |
| 具嶋 弘 | 山之内製薬株式会社研開経営部理事 | |
| 黒木 登志夫 | 昭和大学腫瘍分子生物学研究所長 | |
| 櫻井 秀也 | 社団法人日本医師会常任理事 | |
| 笹月 健彦 | 九州大学生体防御医学研究所長 | |
| 清野 進 | 千葉大学大学院医学研究科教授 | |
| 高芝 利仁 | 弁護士 | |
| 地神 芳文 | 工業技術院生命工学工業技術研究所次長 | |
| 福嶋 義光 | 信州大学医学部教授(衛生学) | |
| 町野 朔 | 上智大学法学部教授 | |
| 丸山 英二 | 神戸大学法学部教授 | |
| 南 砂 | 讀賣新聞社編集局解説部次長 | |
| 山口 建 | 国立がんセンター研究所副所長 |
<平成13年3月現在。五十音順(敬称略)。◎は委員長>
作業委員会名簿
| 青野 由利 | 毎日新聞社科学環境部編集委員 | |
| 味木 和喜子 | 大阪府立成人病センタ-調査部調査課集検整合係長 | |
| 油谷 浩幸 | 東京大学先端科学技術研究センター助教授 | |
| 池田 恭治 | 国立療養所中部病院長寿医療研究センター老年病研究部長 | |
| 稲田 俊也 | 国立精神・神経センター精神保健研究所老化研究室長 | |
| 内野 眞也 | 野口病院外科医師 | |
| 浦川 道太郎 | 早稲田大学法学部教授 | |
| 大山 真未 | 科学技術政策研究所上席研究官 | |
| 岡 慎一 | 国立国際医療センターエイズ治療・研究開発センター臨床研究開発部長 | |
| 掛江 直子 | 早稲田大学人間総合研究センター助手 | |
| 菊池 裕 | 国立医薬品食品衛生研究所衛生微生物部 主任研究官 | |
| 蔵田 伸雄 | 三重大学人文学部助教授 | |
| 黒崎 雅之 | 東京医科歯科大学助手 | |
| 斎藤 博久 | 国立小児病院免疫アレルギー研究部長 | |
| 齋藤 有紀子 | 北里大学医学部医学原論研究部門 | |
| 佐藤 恵子 | 国立がんセンター中央病院臨床試験管理室 | |
| 菅野 純夫 | 東京大学医科学研究所助教授 | |
| 菅野 康吉 | 栃木県立がんセンターがん遺伝子研究室・がん予防研究室 | |
| 玉井 真理子 | 信州大学医療技術短期大学部 | |
| 塚田 俊彦 | 国立がんセンター研究所細胞増殖因子研究部室長 | |
| 津金 昌一郎 | 国立がんセンター研究所臨床疫学研究部長 | |
| 辻 省次 | 新潟大学脳研究所教授 | |
| 外口 崇 | 医薬品副作用被害救済・研究振興調査機構研究振興部長 | |
| 戸田 達史 | 大阪大学大学院医学系研究科バイオメディカル教育研究センター教授 | |
| 中川 徹 | 日立製作所日立健康管理センター | |
| 橳島 次郎 | 三菱化学生命科学研究所社会生命科学研究室主任研究員 | |
| 橋本 雄之 | 国立感染症研究所遺伝子資源室(遺伝子バンク)室長 | |
| 長谷川 知子 | 静岡こども病院染色体科医長 | |
| 二見 仁康 | 国立がんセンター研究所細胞増殖因子研究部室長 | |
| 松浦 幸男 | バイオ産業情報化コンソーシアム(JBIC)情報化推進部長 | |
| 松本 恒雄 | 一橋大学大学院法学研究科教授 | |
| 水澤 博 | 国立医薬品食品衛生研究所変異遺伝部第三室(細胞バンク)室長 | |
| 宮本 真司 | 年金福祉事業団資金運用事業部運用管理課長 | |
| 森川 功 | 早稲田大学人間総合研究センター客員研究員 | |
| 森崎 隆幸 | 国立循環器病センターバイオサイエンス部長 | |
| 山内 正剛 | 放射線医学総合研究所第2研究グループ主任研究官 | |
| 山縣 然太郎 | 山梨医科大学医学部教授(保健学講座) | |
| ○ | 山口 建 | 国立がんセンター研究所副所長 |
| 吉田 輝彦 | 国立がんセンター研究所分子腫瘍学部長 | |
| 吉村 義信 | 武田薬品工業(株)創薬研究本部薬物機能第一研究所所長 |
| (専門家)(五十音順) | ||
| 位田 隆一 | (京都大学大学院法学研究科教授) | |
| 岡部 喜代子 | (東洋大学法学部教授) | |
| 金澤 一郎 | (東京大学大学院医学系研究科教授) | |
| 木村 利人 | (早稲田大学人間科学部教授) | |
| 高久 史麿 | (自治医科大学学長) | |
| 高芝 利仁 | (弁護士) | |
| 寺田 雅昭 | (国立がんセンター総長) | |
| 松村 外志張 | (日本組織培養学会倫理委員会委員長) |
|
| (原案作成検討委員会) | ||
| 委員長 垣添 忠生 | (国立がんセンター中央病院長) |
|
| (原案作成作業委員会) | ||
| 座長 山口 建 | (国立がんセンター研究所副所長) |
|
| (事務局) | ||
| 田中 敏 | (文部科学省研究振興局ライフサイエンス課長) | |
| 佐柳 進 | (厚生労働省大臣官房厚生科学課長) | |
| 塚本 芳昭 | (経済産業省製造産業局生物化学産業課長) | |
4.開催日
平成13年3月15日(於 経済産業省別館8階 第827号会議室)
についての関係審議会等の審議経過
| 関係審議会等 | 12年8月 | 9月 | 10月 | 11月 | 12月 | 13年1月 | 2月 | 3月 |
| 3省関係者会議 | 15日 | |||||||
| 検討委員会 | 14日 | 5日 18日 | 12日 26日 | 16日 | 7日 | |||
| 科学技術会議(平成13年1月6日廃止) | ||||||||
| 生命倫理委員会 | 21日 | |||||||
| ヒトゲノム研究小委員会 | 20日 | 11日 | ||||||
| 文部科学省 (旧 文部省) 科学技術・学術審議会生命倫理・安全部会 (旧 学術審議会 バイオサイエンス部会) |
||||||||
| (旧 学術審議会 がん研究部会) | 24日 (合同部会) |
|||||||
| 厚生労働省 (旧 厚生省) |
||||||||
| 厚生科学審議会 科学技術部会 | 26日 | 19日 | ||||||
| (旧 厚生科学審議会 先端医療技術評価部会) | 22日 | 13日 24日 | 22日 | |||||
| 経済産業省 (旧 通商産業省) 産業構造審議会 化学・バイオ部会 (旧 化学品審議会 個人遺伝情報保護部会) |
2日 | 16日 | 13日 | 4日 |
1.意見募集の概要
(1)期間 平成12年12月20日~平成13年1月31日
(2)告知方法:関係省庁ホームページ、記者発表等
(3)意見送付方法:電子メール又は郵送
2.受付意見件数
(1)意見提出者数
(2)延べ意見数
3.受付意見の概要
(1)指針(案)に対する意見の内訳は以下のとおり。
いただいた意見の概要及びそれに対する考え方については、整理表の形で取りまとめ、関係3省(文部科学省・厚生労働省・経済産業省)のホームページで公表している。
(3)意見本文等の公開
いただいた意見については、提出者の意向を踏まえ匿名化を行った上で、その全文を、(2)の整理表とともに、文部科学省研究振興局ライフサイエンス課、厚生労働省大臣官房総務課情報公開文書室、経済産業省製造産業局生物化学産業課において公開している。
○ 文部科学省(研究振興局 ライフサイエンス課)
○ 厚生労働省(大臣官房 厚生科学課)
○ 経済産業省(製造産業局 生物化学産業課)
に対する意見募集の結果概要について
※ 省庁再編のため、受付期間は平成13年1月9日~平成13年1月末
92件 (個人61件 団体31件)
577件 (提出意見の中で複数の項目について意見が述べられているものがあるため)
(2)意見の概要及びそれに対する考え方
総論
主な項目
146件
全般的意見
27件
表現方法
28件
人権の観点
14件
他の規範との関係
13件
経済的側面
11件
前文
18件
1. 基本方針
17件
2. 本指針の適用範囲
35件
3.すべての研究者等の基本的な責務
17件
4.研究実施機関の長の責務
55件
5. 研究責任者の責務
39件
6. 個人識別情報管理者の責務
6件
7. 倫理審査委員会の責務及び構成
61件
8. 試料等提供者等のI.C.
79件
9. 遺伝情報の試料等提供者等への開示
19件
10. 遺伝カウンセリング
16件
11. 研究実施前提供試料等の利用
17件
12. 試料等の保存及び廃棄の方法
5件
13. 見直し
5件
14. 用語の定義
42件
3省事務局名簿
住所 :
〒100-8966 東京都千代田区霞が関2-2-1
電話 :
03-3581-5271(代表)内線5451
03-3509-1268(直通)
FAX :
03-3509-1269
室長
菱山 豊
室長補佐
郡 健次
調査員
小郷 克幸
住所 :
〒100-8916 東京都千代田区霞が関1-2-2
電話 :
03-5253-1111(代表)内線3804、3807
03-3595-2171(直通)
FAX :
03-3503-0183
研究企画官
中垣 俊郎
課長補佐
野口 尚
課長補佐
坂本 大輔
係長
安藤 公一
主査
岡田 千鶴
住所:
〒100-8901 東京都千代田区霞が関1-3-1
電話:
03-3501-1511(代表)内線3741
03-3501-8625(直通)
FAX:
03-3501-0197
e-mail:
qfsc@meti.go.jp
事業環境整備室長
後藤 久典
製造産業専門官
福島 伸享
係長
山本 耕市
[参考]
トップへ
報道発表資料
トピックス
厚生労働省ホームページ